Clear Sky Science · ar
تعزيز فعالية العلاج الضوئي-الحراري عبر التصفية البصرية للأنسجة البيولوجية بمادة التارترازين
جعل علاجات السرطان المعتمدة على الضوء تعمل بشكل أفضل
يزداد اعتماد الأطباء على الضوء لتسخين وتدمير الأورام العميقة داخل الجسم، في استراتيجية تُعرف بالعلاج الضوئي-الحراري. لكن هناك عقبة رئيسية: الأنسجة تشتت الضوء، لذلك يصل إلى الهدف جزء صغير فقط من الطاقة، بينما قد تتعرض المناطق السليمة لفرط التسخين. تستكشف هذه الدراسة مساعداً غير متوقع — صبغة غذائية صفراء شائعة تُدعى التارترازين — التي يمكن أن تجعل الأنسجة مؤقتاً أكثر شفافية للضوء العلاجي، وبالتالي تجعل علاجات تسخين السرطان أكثر أماناً وفعالية.
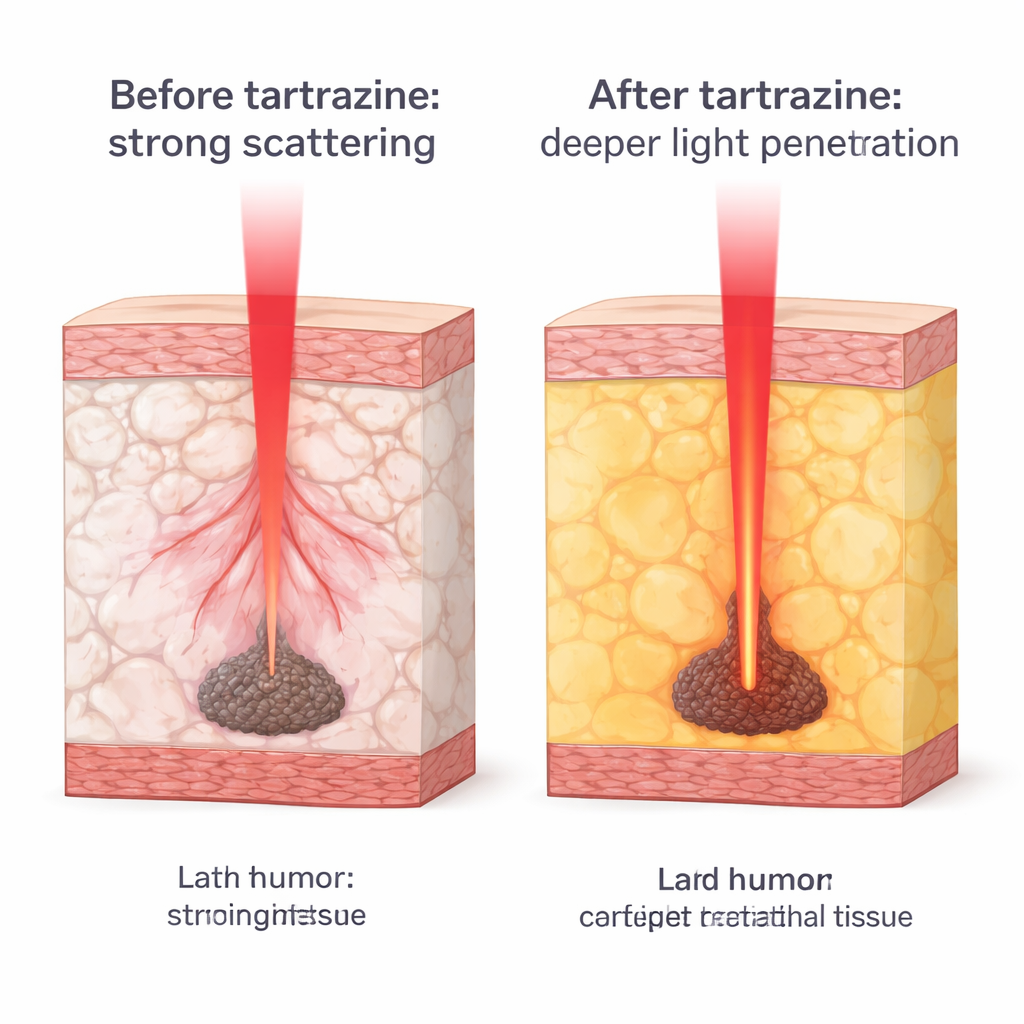
صبغة غذائية ذات موهبة مخفية
يُستخدم التارترازين على نطاق واسع لتلوين الأطعمة والمشروبات وله سجل أمني موثَّق عند الجرعات الغذائية. استند الباحثون إلى أعمال فيزياء حديثة أظهرت أنه عندما يُذاب التارترازين في الماء، يغير كيفية انتقال الضوء عبر ذلك السائل عند الأطوال الموجية القريبة من الأشعة تحت الحمراء المستخدمة عادة في العلاجات الطبية. بدلاً من تمزيق أو تجفيف الأنسجة كما تفعل العديد من «عوامل التصفية» التقليدية، يضبط التارترازين بشكل دقيق كيفية انكسار الضوء في الفراغات المائية بين الدهون والبروتينات. من خلال جعل الخصائص البصرية لهذه المكونات أكثر تشابهاً، تقلل الصبغة كمية الضوء الذي ينكسر ويتشتت.
تحويل الأنسجة المعاتمة إلى نافذة أوضح
لاختبار هذه الفكرة، أنشأ الفريق أولاً «أشباح أنسجة» مُتحكم بها — كتل هلامية تحتوي على حبيبات بلاستيكية دقيقة تحاكي كيفية تشتت الأنسجة الحقيقية للضوء. باستخدام محاكاة حاسوبية وتجارب، أظهروا أن إضافة التارترازين يمكن أن تقلل التشتت بما يصل إلى نحو ثلثي الكمية، خاصة في العينات المملوءة بجسيمات أكبر ومكتظة بكثافة، التي تشبه الهياكل البيولوجية الحقيقية. عند تراكيز مختارة بعناية، زاد التارترازين من مقدار الضوء العلاجي الذي يمر عبر هذه الأشباح دون أن يجعلها داكنة للغاية بسبب لون الصبغة نفسها. كانت النقطة المثالية حوالى 0.3–0.5 مول لكل لتر من الصبغة، حيث كان التوازن بين تقليل التشتت والامتصاص الإضافي في أحسن حال.
من الجِيلات النموذجية إلى أنسجة حيوانية حقيقية
بعد ذلك انتقل الباحثون من الجِيلات الاصطناعية إلى شرائح من لحم الدجاج، كمحاكٍ أقرب للأنسجة الحية. بعد نقع العينات في التارترازين، قاسوا كمية الضوء المرئي والقريب من الأشعة تحت الحمراء التي يمكنها المرور. أصبحت الأنسجة المعالجة أكثر شفافية بشكل ملحوظ، مما سمح بمرور ما يصل إلى نحو 1.7 مرة ضوء أكثر عند أطوال موجية معينة. ومن المهم أن هذه التصفية كانت قابلة للانعكاس: عندما أُعيدت الأنسجة المنقوعة في التارترازين إلى الماء العادي، عادت تدريجياً إلى حالتها الأصلية الأكثر تعتماً. أظهرت اختبارات الصور أن أنماطاً دقيقة موضوعة خلف الأنسجة المعالجة ظهرت أكثر حدة وتبايناً أعلى، مما يدل على أن الضوء كان يسافر بشكل أسترight بدلاً من أن يشتت في جميع الاتجاهات.
توصيل حرارة أكثر إلى حيث تهم
لا يهم تحسّن اختراق الضوء إلا إذا أدى إلى علاج أفضل. للتحقق من ذلك، بنى الفريق نموذج ورم واقعي باستخدام هياكل مطبوعة ثلاثية الأبعاد مُحشوة بخلايا جليوبلاستوما بشرية (سرطان الدماغ)، ثم وضعوا طبقات «أنسجة» معالجة بالتارترازين أو غير معالجة بين ليزر قريب من الأشعة تحت الحمراء ونماذج الورم. مع وجود التارترازين في المسار، وصل المزيد من طاقة الليزر إلى منطقة الورم، رافعاً درجات الحرارة بما يصل إلى نحو 10 درجات مئوية مقارنة بالإعدادات غير المعالجة. هذا التسخين الأعلى والأكثر تجانساً حوّل التأثيرات من متواضعة إلى قتل قوي للخلايا الورمية. في الظروف المعالجة بالتارترازين، حتى قدرات ليزر متوسطة أدت إلى زيادات واضحة في موت خلايا السرطان، وارتفاع في الانتحار الخلوي المبرمج (الاستماتة)، وتزايد في الجزيئات المؤذية مثل أنواع الأكسجين التفاعلية — وكلها علامات على فعالية العلاج الضوئي-الحراري.
لماذا يهم هذا لعلاجات المستقبل
بشكل عام، تشير الدراسة إلى أن «تصفية» الأنسجة مؤقتاً باستخدام صبغة آمنة غذائياً قد تساعد علاجات السرطان المعتمدة على الضوء على الوصول إلى أهداف أعمق باستخدام طاقات ليزر أقل، أو أوقات علاج أقصر، أو كلاهما. وبما أن التارترازين يعمل أساساً عن طريق ضبط حركة الضوء عبر الأنسجة بلطف — بدلاً من إتلافها كيميائياً — فإن تأثيراته قابلة للانعكاس وربما أكثر أماناً من العديد من المواد الكيماوية المستخدمة حالياً في التصفية. ومع الحاجة إلى دراسات حيوانية وسلامة إضافية، يشير هذا العمل إلى وسيلة بسيطة ومنخفضة التكلفة لتحويل الجسم من عقبة تشتت الضوء إلى شريك أكثر تعاوناً، مما يجعل العلاج الضوئي-الحراري أكثر دقة وأقل إلحاقاً بالضرر بالأنسجة السليمة المحيطة.
الاستشهاد: Minopoli, A., Evangelista, D., Marras, M. et al. Enhancing photothermal therapy effectiveness via tartrazine-induced optical clearing of biological tissues. Sci Rep 16, 7553 (2026). https://doi.org/10.1038/s41598-026-38616-2
الكلمات المفتاحية: العلاج الضوئي-الحراري, التارترازين, التصفية البصرية, علاج السرطان بالضوء, شفافية الأنسجة