Clear Sky Science · ar
الرنا طويل السلاسل FTX يعزز تليف القلب عن طريق امتصاص miR-335-3p لتنظيم إشارة TFEC/ILK
لماذا يهم تندب القلب
يصيب فشل القلب عشرات الملايين من الناس حول العالم وغالبًا ما يتطور بصمت على مدى سنوات. أحد المحركات الرئيسية لهذا التدهور هو تليف عضلة القلب—تكوّن ندبات بطيء وتقدمي في نسيج القلب يجعلها أكثر صلابة وأقل قدرة على ضخ الدم. تبحث هذه الدراسة في «الأسلاك» الجزيئية التي تأمر خلايا القلب بتكوين نسيج ندبي زائد، وتحدد سلسلة جزيئية جديدة قد تكون هدفًا لتثبيط أو حتى عكس هذه العملية الضارة.
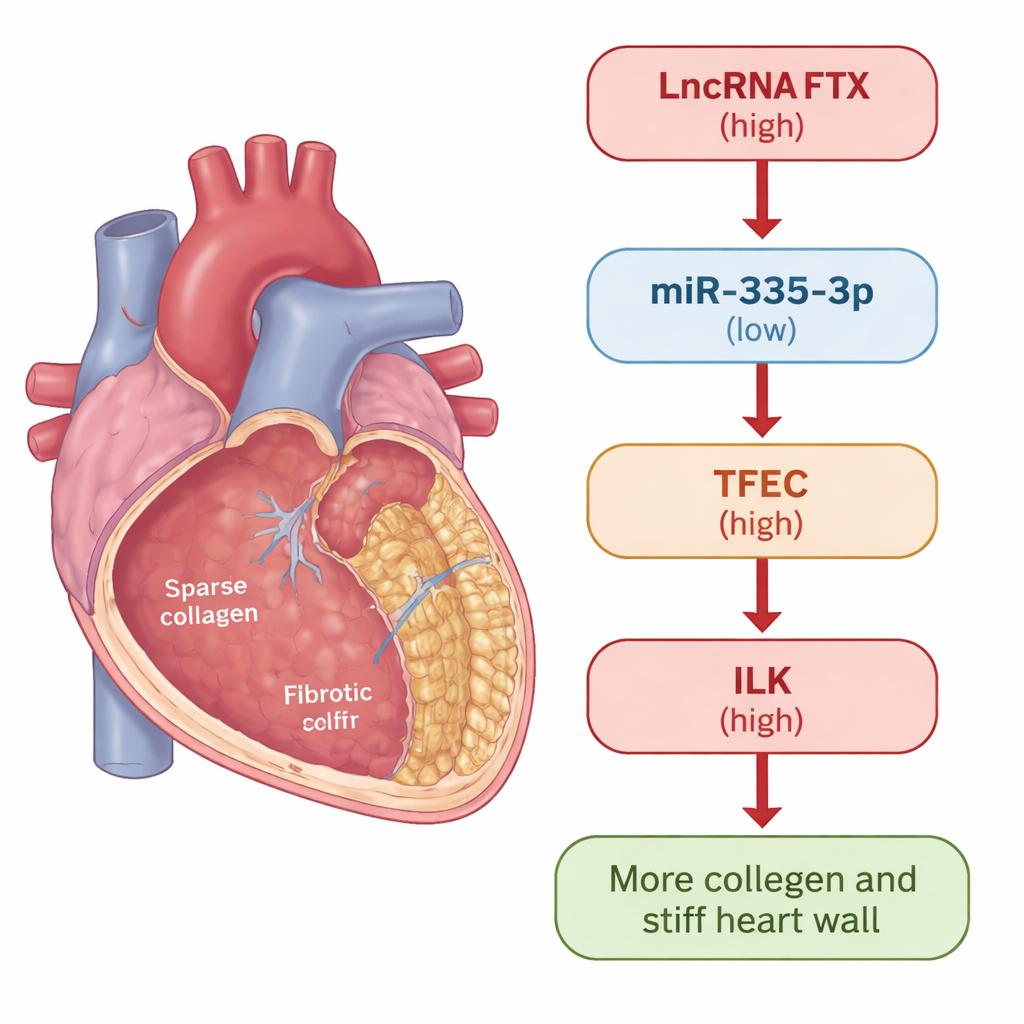
نظرة أدق على تندب القلب
عندما يصاب القلب أو يتعرض للإجهاد، تنشط خلايا داعمة تُسمى الخلايا الليفية القلبية. في الإصلاح الصحي، تساعد هذه الخلايا على ترقيع الضرر. لكن في الأمراض المزمنة قد تتحول إلى حالة مفرطة النشاط، فتنتج كميات زائدة من الكولاجين ومكونات أخرى للمصفوفة خارج الخلوية، مما يؤدي في النهاية إلى تَصلّب جدار القلب. استخدم الباحثون نموذجين لدراسة هذه العملية: فئران عولجت بمادة الإيزوبروتيرينول التي تحفز تليف القلب بشكل موثوق، وخلايا ليفية قلبية بشرية تعرّضت للمولِّد الإشاري TGF-β1 المعروف بتحفيز التندب. في كلتا الحالتين قاسوا كيف تغيرت جينات وبروتينات محددة مع تطور التليف.
تفاعل سلسلة ضار داخل الخلايا
ركّز الفريق على عامل نسخ يُدعى TFEC، وهو بروتين يقع في نواة الخلية ويشغّل جينات أخرى. وجدوا أن TFEC، جنبًا إلى جنب مع بروتين آخر يُسمى كيناز مرتبط بالإنتجرين (ILK)، ارتفع مستواهما باستمرار عندما دُفعَت الخلايا الليفية نحو حالة تليفية مكوِّنة للندبات. أدى إخماد TFEC أو ILK إلى خفض حاد في علامات التليف الكلاسيكية مثل أكتين العضلات الملساء α والكولاجينات I وIII، كما قلّل من مسار التحكم في النمو (إشارات Akt/GSK3β وHippo) المعروف بتعزيز تندب الأنسجة. أظهرت تجارب تحديد ارتباط الحمض النووي أن TFEC يرتبط مباشرة بمروِّج جين ILK ويعزّز نشاطه، ما يضع TFEC بوضوح في موقع أعلى من ILK ضمن سلسلة إشارات تروّج للتليف.
مفاتيح رنوية تتحكم في المنظم الرئيسي
لفهم ما يتحكم في TFEC نفسه، لجأ الباحثون إلى الرنا غير المشفّر—جزيئات رنا لا تصنع بروتينات لكنها تعمل كضوابط دقيقة لنشاط الجينات. حددوا رنا صغيرًا، miR‑335‑3p، الذي كان منخفضًا في القلوب والخلايا المتليفَة. رفع مستوياته خفض TFEC، بينما أدى حظره إلى زيادة TFEC، وأكدت اختبارات المراسل أن miR‑335‑3p يرتبط مباشرة برسائل TFEC لكبحها. ثم وجدوا رنا طويلًا غير مشفّر يُدعى FTX، ارتفع في التليف وتفاعل فعليًا مع miR‑335‑3p. عمل FTX كإسفنجة جزيئية: امتصّ miR‑335‑3p، مانعًا هذا الرنا الصغير من كبح TFEC. نتيجة لذلك، ارتفعت مستويات TFEC وILK، وأنتجت الخلايا الليفية كولاجينًا أكثر مكوّنًا للندبات.
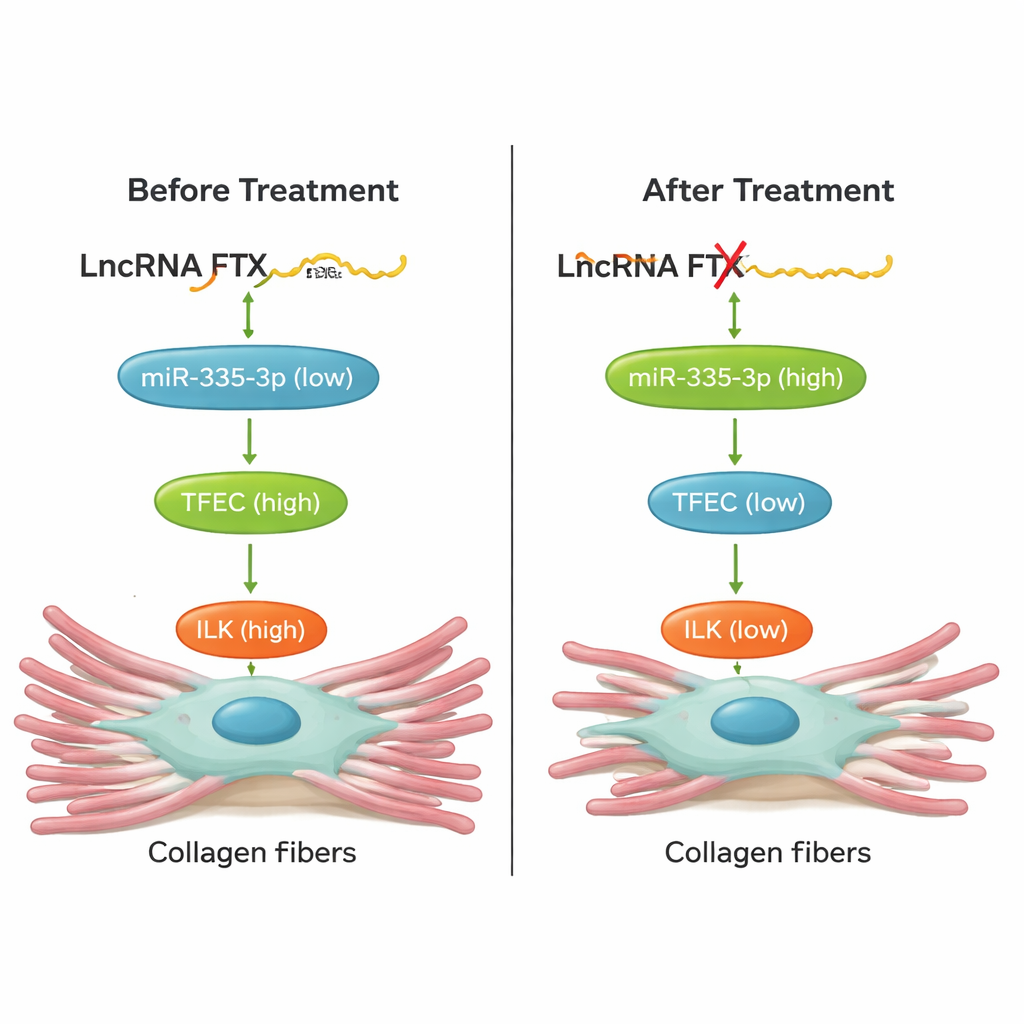
من مزرعة الخلايا إلى قلوب حية
ومن الأهمية أن الفريق اختبر ما إذا كان تعطيل هذه السلسلة يمكن أن يحمي القلوب في الحيوانات فعليًا. في فئران تعرّضت للإيزوبروتيرينول، أدت خفض TFEC أو تقليل FTX في القلب باستخدام ناقل علاج جيني AAV9، أو تعزيز miR‑335‑3p بواسطة جزيء "أغومير" مستقر كيميائيًا، إلى تقليل تراكم الكولاجين وانخفاض مستويات علامات التليف في نسيج القلب. حسّنت هذه التدخّلات أيضًا وظيفة القلب: عاد حجم الضربة الكمية ونسبة القذف باتجاه القيم الطبيعية، وتلاشت الزيادات الضارة في معدل ضربات القلب. أظهرت تجارب الإنقاذ في الخلايا أن تغيير مكوّن واحد من محور FTX/miR‑335‑3p/TFEC/ILK بدّل المكونات الأخرى بشكل متوقع، مؤكدة أن هذا مسار مترابط بإحكام وليس مجرد علاقة مصادفة.
ماذا يعني هذا لعلاجات المستقبل
بالنسبة لغير المتخصصين، الخلاصة أن المؤلفين حددوا "رافعة تحكّم" جديدة لتندب القلب. يرفع رنا طويل يُدعى FTX المكابح (miR‑335‑3p) عن مفتاح رئيسي (TFEC)، الذي يشغّل بعد ذلك ILK وإشارات تروّج للتندب، مما يدفع إلى ترسّب كولاجين مفرط وتصلّب القلب. عن طريق خفض FTX أو استعادة miR‑335‑3p أو حجب TFEC مباشرة، تمكنوا في الفئران من تقليل التندب وتحسين وظيفة الضخ. بينما هناك حاجة لمزيد من العمل لتأكيد هذا المسار في المرضى البشر وتطوير علاجات آمنة، يقدم هذا المحور التنظيمي القائم على الرنا عدة نقاط واعدة للتدخل في فشل القلب المدفوع بالتليف.
الاستشهاد: Yao, F., He, Z., Zheng, C. et al. LncRNA FTX promotes myocardial fibrosis by sponging miR-335-3p to regulate TFEC/ILK signaling. Sci Rep 16, 7340 (2026). https://doi.org/10.1038/s41598-026-38615-3
الكلمات المفتاحية: تليف عضلة القلب, فشل القلب, الرنا غير المشفّر, الخلايا الليفية القلبية, إشارات التليف