Clear Sky Science · ar
تأثير طفرة DNMT3A p.R882C على التكاثر ومقاومة الموت المبرمج في خلايا سرطان البنكرياس
لماذا يهم هذا البحث لسرطان البنكرياس
يشتهر سرطان البنكرياس بالاكتشاف المتأخر، والانتشار السريع، والاستجابة الضعيفة للعلاج. يُشخّص معظم المرضى بسرطان قنوات البنكرياس الغدي (PDAC)، وهو شكل عدواني من المرض. تدرس هذه الدراسة تغييرًا طفيفًا في جين واحد يسمى DNMT3A، وتسأل سؤالًا كبيرًا: هل يمكن لهذا التغيير البسيط أن يفسر لماذا تنمو بعض سرطانات البنكرياس بسرعة أكبر وتقاوم موت الخلايا؟ فهم مثل هذه التغييرات قد يفتح الباب للكشف المبكر وعلاجات أكثر دقة واستهدافًا.
نظرة أقرب على سرطان قاتل
يشكل PDAC أكثر من 90% من سرطانات البنكرياس ومعدل البقاء على قيد الحياة لخمس سنوات يقل عن 13%. عادة ما يقوده جينات سرطانية معروفة مثل KRAS وTP53، لكن العديد من المرضى لا يستفيدون من العلاجات المستهدفة الحالية. تشير أعمال حديثة إلى أن ليس فقط طفرات الجينات، بل أيضًا التغيرات «الوراثية فوق الجينية» — أي العلامات الكيميائية على الحمض النووي التي تتحكم في تشغيل أو إيقاف الجينات — تلعب دورًا رئيسيًا في هذا السرطان. DNMT3A هو واحد من الإنزيمات الرئيسية التي تضيف هذه العلامات، وقد رُبطت عيوبه بالفعل بسرطانات الدم مثل اللوكيميا النخاعية الحادة.
البحث عن تغييرات DNA خطرة
جمع الباحثون عينات أورام ونسيجًا غير سرطاني مجاورًا من ثلاثة مرضى يعانون PDAC متوسط إلى ضعيف التمايز. استخدموا تسلسل الإكسوم الكامل، وهي تقنية تقرأ جميع مناطق الترميز البروتيني في الجينوم، ثم طبّقوا مرشحات حاسوبية صارمة لفصل التباينات الحميدة عن تلك المرجح أن تضر بسلوك الخلايا. من بين مئات التغييرات، ضيقوا القائمة إلى 68 تغييرًا عالي الخطورة. من بينها برزت نادرة في DNMT3A، المعروفة باسم p.R882C، لأنها تكاد لا تظهر في قواعد بيانات سكانية كبيرة وكانت مُصنّفة باستمرار كمضرة بواسطة عدة أدوات تنبؤية.
ماذا تفعل هذه الطفرة داخل الخلايا
DNMT3A هو بروتين مكوّن من 912 حمضًا أمينيًا يساعد في تأسيس أنماط مثيلة الحمض النووي — علامات كيميائية تعمل كمفاتيح «تشغيل» أو «إيقاف» للجينات. تقع تغيرة p.R882C في منطقة تشغيلية حاسمة من DNMT3A، حيث قد تعطل نشاط الإنزيم. باستخدام نماذج ثلاثية الأبعاد حاسوبية، وجد الفريق أن الشكل العام للبروتين لم يتغير بشكل درامي، مما يوحي بأن المشكلة قد تكمن في كيفية عمل الإنزيم أكثر من كيفية طيه. لاختبار ذلك، صنعوا خطوط خلايا سرطان البنكرياس (PANC‑1 وPaTu 8988t) لإنتاج إما DNMT3A الطبيعي أو النسخة p.R882C، وقارنّوها بخلايا تحمل ناقل تحكم فارغ.
نمو أسرع، حركة أكبر، وموت خلوي أقل
بشكل مفاجئ، لم تغير طفرة p.R882C كمية DNMT3A المصنوعة على مستوى الحمض النووي الريبي أو البروتين؛ بقيت كمية الإنزيم تقريبًا كما هي. ومع ذلك، كان لوجودها تأثيرات ملفتة على سلوك الخلايا. في تجارب تكوين المستعمرات والنمو، كونت الخلايا الحاملة للطفرة DNMT3A المزيد من المستعمرات وأظهرت إشارات نمو أعلى من تلك الحاملة للنسخة الطبيعية. اختبارات التئام الجروح وTrans‑well، التي تقيس سرعة حركة الخلايا، كشفت أن الخلايا الحاملة للطفرات هاجرت أسرع. وعند فحص الموت المبرمج للخلايا (الاستماتة) باستخدام تأبير الخلايا بالتدفق، كانت الخلايا ذات طفرة p.R882C تحتوي على خلايا ميتة أقل بشكل ملحوظ، سواء في مراحل الاستماتة المبكرة أو المتأخرة، مما يشير إلى ميزة بقاء قوية.
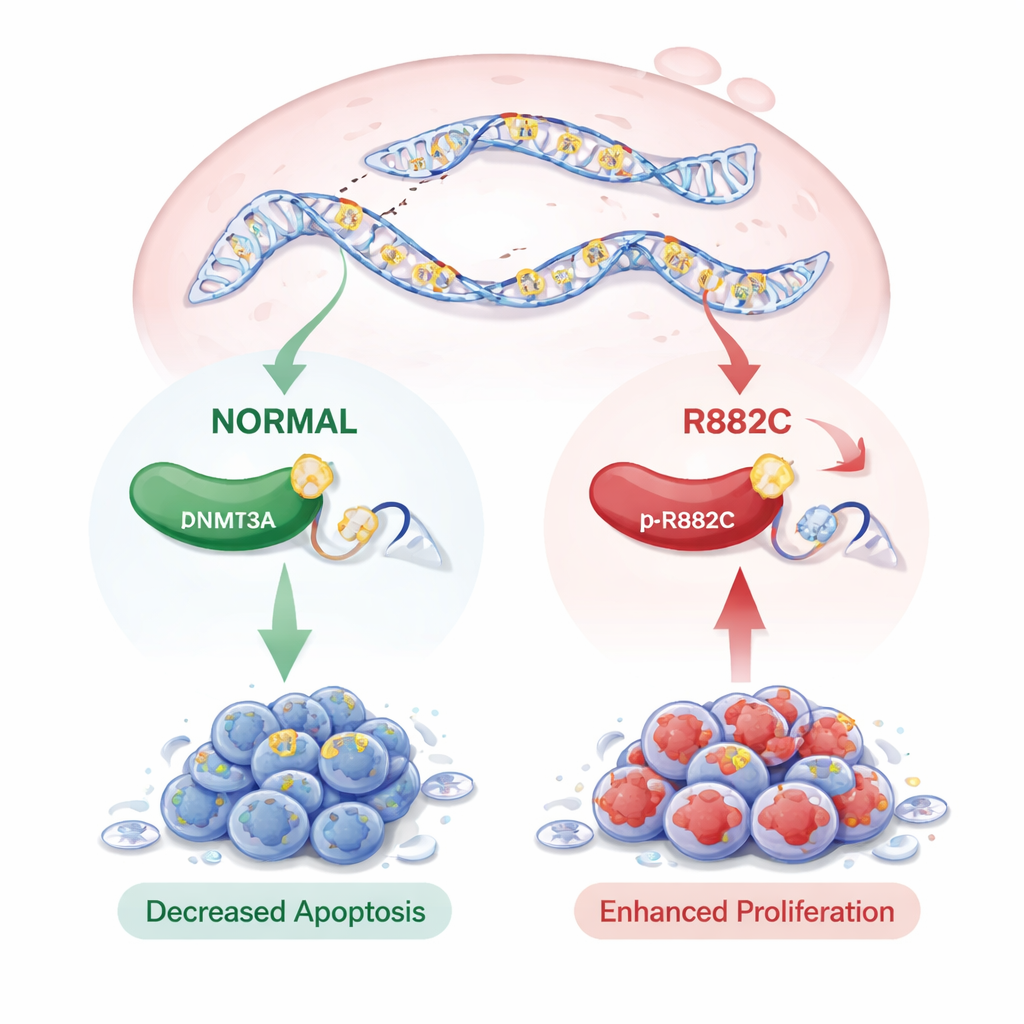
ما قد يعنيه هذا للرعاية المستقبلية
بجمع هذه النتائج، تقترح الدراسة أن طفرة DNMT3A النادرة p.R882C تساعد خلايا سرطان البنكرياس على النمو أسرع، والتحرك بسهولة أكبر، ومقاومة الانتحار الخلوي — صفات قد تسهم في تقدم السرطان. على الرغم من أن الطفرة لا تزيد من مستويات DNMT3A، فمن المحتمل أنها تغير نشاط الإنزيم ونمط العلامات على الحمض النووي عبر الجينوم، ما يعكس ما لوحظ في بعض سرطانات الدم. يلاحظ المؤلفون أن هذه التغيرة نادرة ولم تظهر بعد روابط واضحة مع بقاء المرضى في مجموعات البيانات العامة، جزئيًا لأن الدراسات المتاحة صغيرة وغالبًا لا تشمل DNMT3A. ومع ذلك، يبرز اكتشاف هذه الطفرة في PDAC لاعبًا جديدًا محتملاً مهمًا في المرض ويثير إمكانية أن تصبح DNMT3A p.R882C مستقبلاً علامة خطر أو هدفًا لعلاجات أكثر تفصيلًا.
الاستشهاد: Qu, Z., Mao, J., Qian, Y. et al. DNMT3A p.R882C driven proliferation and anti-apoptotic effects in pancreatic cancer cells. Sci Rep 16, 7659 (2026). https://doi.org/10.1038/s41598-026-38613-5
الكلمات المفتاحية: سرطان البنكرياس, طفرة DNMT3A, PDAC, مثيلة الحمض النووي, علاج مستهدف