Clear Sky Science · ar
الخلايا التائية المنشَّطة تُحفِّز الاستماتة في خلايا غُدِّيّة سرطان الرئة A549 عبر تدفق الكالسيوم الوسيط بواسطة TRPV4
لماذا يهم هذا البحث لسرطان الرئة
لا يزال سرطان الرئة من أخطر أنواع السرطان، جزئياً لأن الأورام غالباً ما تتعلم كيف تقاوم العلاجات القياسية مثل العلاج الكيميائي والإشعاع. في السنوات الأخيرة، أعطى استثمار جهاز المناعة في الجسم أملاً جديداً. يستكشف هذا الدراسة لمسة جديدة على الفكرة: إنها توضح كيف أن نوعاً محدداً من خلايا المناعة، يُسمى الخلايا التائية المنشَّطة، يمكنه دفع خلايا سرطان الرئة إلى تدمير نفسها عن طريق إجبارها على امتصاص الكالسيوم عبر «بوّابة» جزيئية تعرف باسم TRPV4. فهم هذا المسار قد يساعد العلماء على تصميم علاجات مناعية أقوى وأكثر دقة.
جنود جهاز المناعة يلتقون خلايا الورم الرئوي
ركز الباحثون على خلايا غُدِّيّة سرطان الرئة البشرية المعروفة باسم خلايا A549، وهو نموذج مستخدم على نطاق واسع لسرطان الرئة غير صغير الخلايا. قاموا بمزاوجة هذه الخلايا السرطانية مع خلايا Jurkat التائية، كنموذج بديل لخلايا القاتل التائية في الجسم، التي تبحث عادة عن الخلايا المصابة أو الخبيثة وتدمرها. من خلال تنشيط خلايا Jurkat كيميائياً، قلَّد الفريق حالة اليقظة العالية للخلايا التائية المشاركة في استجابة مناعية حقيقية. ثم خلطوا الخلايا التائية المنشَّطة أو غير المنشَّطة مع خلايا سرطان الرئة بنسب مختلفة ورصدوا ما يحدث على مدى يوم إلى ثلاثة أيام، مع إيلاء اهتمام خاص لعدد الخلايا السرطانية التي نجت وعدد الخلايا التي دخلت في موت مبرمج، أو الاستماتة.
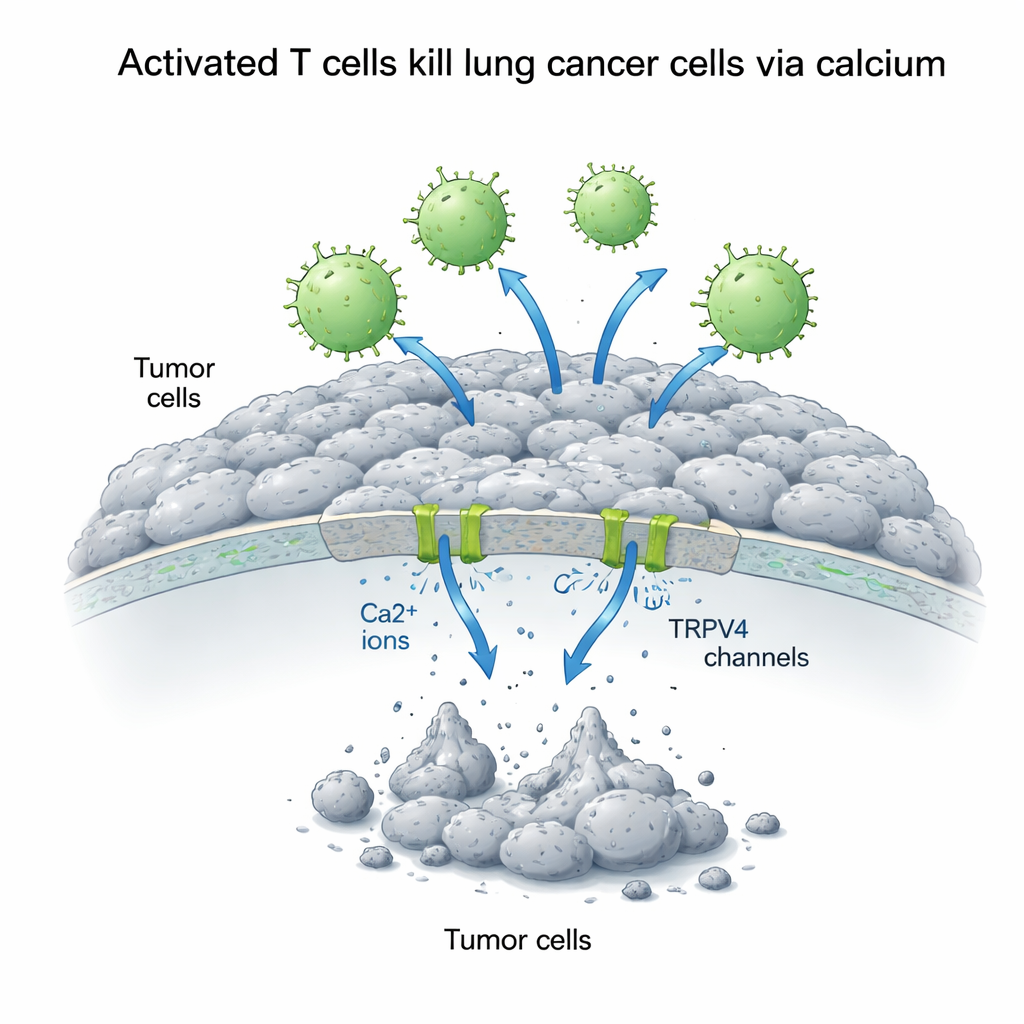
الكالسيوم إشارة ذات حدين للخلايا السرطانية
يعمل الكالسيوم داخل الخلايا كمفتاح إشارة متعدد الاستخدامات يمكنه أن يعزز النمو أو يُطلق الموت، اعتماداً على كيفية التعامل معه. زاد العلماء كمية الكالسيوم خارج خلايا A549 وقاسوا كيف أثر ذلك في الصراع بين الخلايا التائية وخلايا الورم. والمفاجئ أن الكالسيوم الزائد بمفرده جعل خلايا سرطان الرئة تنمو بشكل أفضل، مما يوحي بأن الكالسيوم في ظروف الهدوء يغذي مسارات البقاء. ولكن عند وجود الخلايا التائية المنشَّطة، انقلبت القصة: عزز الكالسيوم الخارجي الأعلى بشكل كبير القتل الذي تقوده الخلايا التائية. على مدى 72 ساعة، انخفضت بقاء الخلايا السرطانية إلى أقل من ثلث الحالة العادية عندما توافرت كلٌّ من الخلايا التائية المنشَّطة والكالسيوم الإضافي، في حين أن الخلايا التائية غير المنشَّطة كان تأثيرها ضئيلاً وربما تدعم النمو عند إضافة الكالسيوم.
«بوابة» الكالسيوم مرتبطة بالإجهاد والموت الخلوي
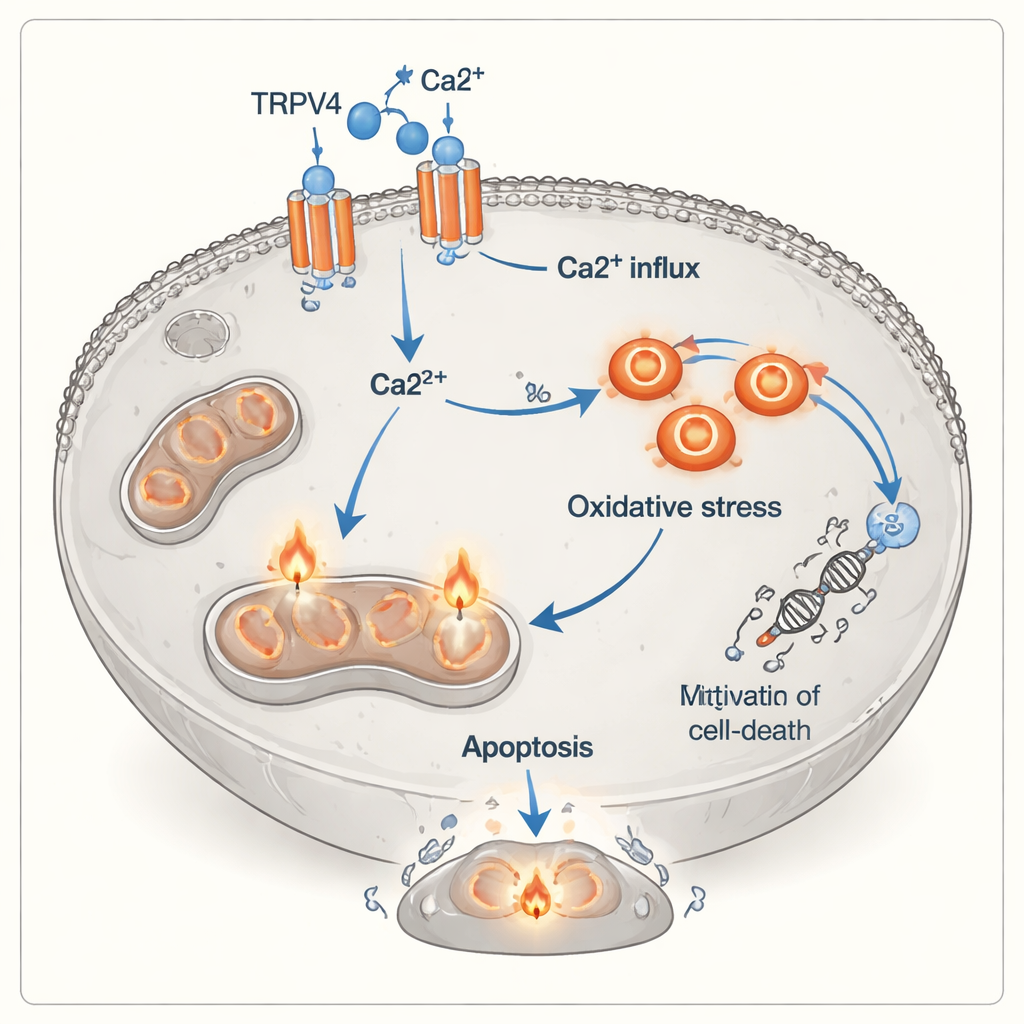
لفهم كيف يحدث هذا التحول من النمو إلى الموت، نظر الفريق في TRPV4، وهو قناة بروتينية في غشاء الخلية تسمح بتدفق الكالسيوم إلى الداخل. باستخدام تحليل البروتينات، وجدوا أن مستويات TRPV4 ارتفعت sharply عندما تعرَّضت خلايا A549 للكالسيوم المضاف، سواء كانت الخلايا التائية موجودة أم لا، وكانت أعلى مستوياتها عندما اجتمعا الكالسيوم والخلايا التائية المنشَّطة. في الوقت نفسه، أظهرت الخلايا السرطانية علامات واضحة على الإجهاد التأكسدي: انحاز التوازن بعيداً عن مضادات الأكسدة الواقية (انخفاض السعة المضادة للأكسدة الكلية) ونحو المؤكسدات الضارة (ارتفاع حالة المؤكسد الكلية). أكدت تقنية قياس التدفق الخلوية (flow cytometry)، التي تصنع ملصقات فلورية للخلايا، أن الخلايا التائية المنشَّطة تسبّب زيادة في كل من مراحل الاستماتة المبكرة والمتأخرة، خاصة عند وفرة الكالسيوم. تشير هذه الملاحظات معاً إلى سلسلة من الأحداث حيث تسمح قنوات TRPV4 بدخول المزيد من الكالسيوم، ما يولد بعد ذلك ضغطاً كيميائياً داخل الخلية ويدفعها نحو الموت.
طبقة جديدة لكيفية قتل خلايا المناعة للأورام
تقليدياً، تدمر الخلايا التائية القاتلة أهدافها عن طريق إطلاق بروتينات سامة أو عن طريق تفعيل مستقبلات الموت على سطح الخلية السرطانية. تقترح هذه الدراسة وجود طريق آخر، أكثر غير مباشرة: يبدو أن إشارات من الخلايا التائية المنشَّطة — بما في ذلك الجزيئات الالتهابية والاتصال الوثيق بين الخلايا — تجعل خلايا سرطان الرئة أكثر اعتماداً على TRPV4 وأكثر عرضة لتحمّل فائض الكالسيوم والضرر التأكسدي. في هذا السياق، تعمل TRPV4 كمفتاح حساس يحوّل الكالسيوم الذي يعزز النمو إلى إشارة قاتلة. وعلى الرغم من أن التجارب أُجريت في أطباق وباستخدام سطر خلوي سرطاني واحد، فإنها تبرز جسرًا محتملاً هاماً بين الهجوم المناعي وقنوات الأيون وآليات الإجهاد الداخلية في خلايا الورم.
ما الذي قد يعنيه هذا للعلاجات المستقبلية
لغير المتخصصين، الخلاصة هي أن نجاح العلاج المناعي قد يعتمد ليس فقط على جعل الخلايا التائية أقوى، بل أيضاً على جعل خلايا السرطان أسهل في القتل. من خلال استهداف TRPV4 أو قنوات الكالسيوم المرتبطة بها، قد يتمكن الأطباء في يوم من الأيام من تعزيز قدرة الخلايا التائية على القضاء على أورام الرئة أو ضبط العلاجات بدقة لتجنب إتلاف الأنسجة السليمة. لا يزال العمل في مرحلة مبكرة، ويؤكد المؤلفون الحاجة إلى تجارب إضافية في الحيوانات ونماذج أكثر تعقيداً. ومع ذلك، فإن اكتشاف محور TRPV4–الكالسيوم–الإجهاد التأكسدي يضيف هدفاً واعداً جديداً إلى صندوق أدوات تحسين العلاجات المناعية ضد سرطان الرئة.
الاستشهاد: Alavi, F., Kazemi-Lomedasht, F., Eftekhari, Z. et al. Activated T cells induce apoptosis in A549 lung adenocarcinoma cells via TRPV4-mediated calcium influx. Sci Rep 16, 7155 (2026). https://doi.org/10.1038/s41598-026-38589-2
الكلمات المفتاحية: العلاج المناعي لسرطان الرئة, الخلايا التائية, إشارة الكالسيوم, قناة TRPV4, الإجهاد التأكسدي