Clear Sky Science · ar
تحسين عوامل الارتباط بجليكتين‑3 عبر تخليق مركبات متعددة في الوضع الفعلي والقياس الكتلي الحَضري
لماذا هذا مهم لأدوية المستقبل
تعتمد العديد من الأدوية الحديثة على الالتصاق ببروتينات داخل أجسامنا، لكن إيجاد جزيء صغير يلتصق بقوة وبانتقائية بموقع محدد عملية بطيئة ومكلفة وغالباً ما تكون محبطة. تُقدّم هذه الدراسة طريقة أسرع لضبط مثل هذه الجزيئات مباشرة بوجود بروتين الهدف، ومن ثم تحديد الفائزين بتقنية وزن حسّاسة للغاية. يستعرض المؤلفون منهجهم على الجليكتين‑3، وهو بروتين مرتبط بنمو السرطان، وينتجون مرشحاً واعداً ذا خصائص دوائية يلتصق بقوة مساوية لبعض أفضل المركبات المعروفة، لكن في جيب غير متوقع على سطح البروتين.

إعادة التفكير في كيفية البحث عن مرشحات أدویة أفضل
يشبه تحسين العقاقير التقليدي لعبة تخمين مكلفة. يغيّر الكيميائيون مركبًا بادئًا خطوة بخطوة، يختبرون كل نسخة، ويأملون في تحسين إحكام الارتباط ببروتين الهدف. لكن أسطح البروتين مرنة، وجزيئات الماء تشكل عائقا، وحدث الارتباط نفسه قد يعيد تشكيل البروتين، مما يجعل التنبؤات الحاسوبية غير موثوقة. حتى عند توفر بنية ذات دقة عالية، لا توجد ضمانة أن التعديل المقترح سيكون مفيدا. تحاول الطرق الحالية «الموجَّهة بالهدف» أن تسمح للبروتين باختيار شركائه من مجموعة لبنات بناء، لكن هذه الأساليب لا تزال تعتمد على تحليلات معقدة وإشارات غير مباشرة للاستدلال على أي مركب يرتبط فعلاً بشكل أفضل.
دع البروتين يختار، ثم وزن الفائزين
جمع الباحثون بين فكرتين في طريقة عمل مبسطة. أولاً، استخدموا تفاعلًا كيميائياً عكوسًا يربط لبًا سكريًا مشتركًا بعدد من القطع الجانبية المختلفة في أنبوب واحد، مشكلاً مزيجًا من الجزيئات ذات الصلة. من خلال ضبط النسب الابتدائية بعناية، تستقر المنتجات الناتجة في حالة توازن يخضع لقواعد التركيز البسيطة، ما يساعد على تعادل كمياتها رغم اختلاف التفاعلية الخام. ثانياً، عرّضوا هذا المزيج للجليكتين‑3 وفحصوه باستخدام القياس الطيفي الكتلي الحَضري، وهو شكل من القياس الكتلي يحافظ على أزواج البروتين–الجزيء سليمة في محلول لطيف يشبه الماء. وبما أن كل مرشح له كتلة مميزة، يمكن للجهاز أن يكشف مباشرة أي الجزيئات مرتبطة فعلاً بالبروتين، دون احتياج لوسوم أو علامات مرجعية.
من مزيجات مكتظة إلى رابط بارز
باستخدام هذا الإعداد، أنشأ الفريق عشرات الروابط للجليكتين‑3 عن طريق إلحاق مجموعات جانبية متنوعة بنواة سكرية مستوحاة من مثبط معروف، GB1107. قسموا 35 قطعة هيدرازيد مختلفة إلى مجموعات قابلة للإدارة، شكلوا كل التركيبات في الوضع الفعلي، ثم أضافوا الجليكتين‑3. أبرز القياس الطيفي الكتلي الحَضري المركبات التي كانت ترافق البروتين أكثر من غيرها، معرِّفا إياها كضربات أولية. اختبرت متابعة لِلاستقرار الحراري ـ التي تقيس كيف يُثَبِّت المركب البروتين عندما يُسخَّن ـ أخرجت الإيجابيات الكاذبة الناتجة عن خصائص قياس الطور الغازي. تبقى ثلاثة مرشحين رائدين، وأظهرت قياسات الارتباط الحرارية التفصيلية أن أحدهم المسمى GalAldBZ20 ارتبط بالجليكتين‑3 بقوة خاصة، في مدى دون الميكرومولار.
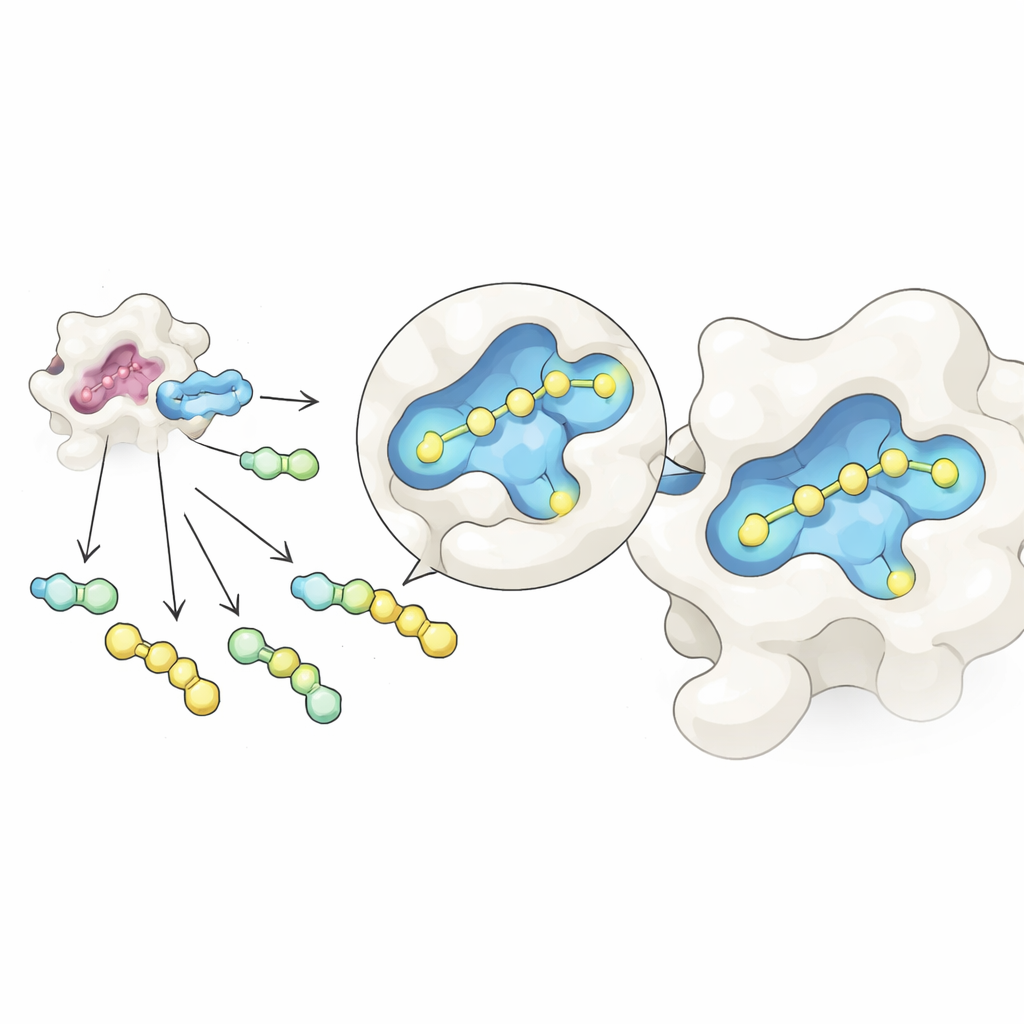
اكتشاف جيب مخفي وتقويته
جاءت المفاجأة التالية عندما نظر الفريق في كيفية تموضع GalAldBZ20 على سطح الجليكتين‑3. تستخدم معظم الروابط المعروفة «جيبًا ألفا» قرب موقع ربط السكر، لكن الطرق التركيبية والمحاكاة الحاسوبية أشارت إلى أن GalAldBZ20 يفضّل بدلاً من ذلك جيبًا مجاورًا «بيتا». دلّت البلورة بالأشعة السينية على هذا، وكشفت المغناطيسية النوية في المحلول عن حالات طي محلية متعددة قرب ذلك الجيب، ودعمت محاكيات الديناميكا الجزيئية نموذجاً حيث يحضن حلقة حاملة للنيترو الجزيء داخل الموقع بيتا. اعتماداً على هذا الاستدلال، أعاد الكيميائيون تصميم الرابط الكيميائي بين السكر والحلقة النيتروية لتشجيع اتصالات قطبية جديدة مع البروتين وتقليل المرونة.
تحويل شاشة ذكية إلى مرشح قوي
بناءً على هذه الرؤية، صنع الفريق مجموعة صغيرة من الجزيئات المتابعة الأكثر صلابة التي احتفظت بنفس السكر والحلقة النيتروية لكن غيرت الموصل بينهما. برزت نسخة واحدة، N‑galactoside (المركب 5): ارتبطت بالجليكتين‑3 أقوى بحوالي عشرة أضعاف من الضربة الأصلية، حتى وصلت قوة ارتباط قابلة للمقارنة مع GB1107، ومع ذلك فضّلت لا تزال الجيب بيتا. أظهرت بنية بلورية فائقة الدقة كثافة واضحة للحلقة النيتروية المحتضنة في ذلك الجيب، مدعومة بعدة روابط هيدروجينية وتماس كاتيون‑π مع أحماض أمينية رئيسية. عندما أُزيلت مجموعة النيترو أو استبدلت بمجموعة ميثيل بسيطة، ضعُف الارتباط بشكل ملحوظ، مما يبرز أهميتها. وبما أن الجليكتين‑1، بروتين ذو صلة، يفتقر إلى هذا الجيب بيتا، قد يوفر المركب الجديد في نهاية المطاف انتقائية أفضل، وهي ميزة مرغوبة في تصميم الأدوية.
ماذا يعني هذا لاكتشاف الأدوية في المستقبل
بعبارات مبسطة، تُظهر هذه الدراسة أنه يمكن خلط العديد من الجزيئات ذات الصلة معًا، وترك بروتين مرتبط بالمرض «ليختار» المفضلات، ثم وزن أزواج البروتين–الجزيء مباشرة لمعرفة أيها يلتصق أفضل. عند تطبيقها على الجليكتين‑3، وجدت هذه الاستراتيجية بشكل غير متوقع ثم قوّت الارتباط إلى جيب أقل استكشافًا، مُنتجة مركبًا ينافس بعض أفضل المثبطات الحالية وقد يخدم كقائد لأدوية مضادة للسرطان جديدة. وبشكل أوسع، يوفر ربط الكيمياء في الوضع الفعلي بالقياس الطيفي الكتلي الحَضري طريقًا مختصراً عاماً لتحسين مرشحات الأدوية ضد بروتينات ذات مواقع ربط متعددة، مما قد يوفر الوقت والمواد والجهد في المراحل المبكرة من اكتشاف الأدوية.
الاستشهاد: Hoshi, K., Konuma, T., Taguchi, R. et al. Optimization of galectin-3 binding agents by in situ multiple compound synthesis and native mass spectrometry. Sci Rep 16, 8453 (2026). https://doi.org/10.1038/s41598-026-38570-z
الكلمات المفتاحية: مثبطات الجليكتين‑3, القياس الطيفي الكتلي الحَضري, اكتشاف الأدوية القائم على الشظايا, التخليق الموجَّه بواسطة الهدف, مرشحات أدوية السرطان