Clear Sky Science · ar
مقارنة ودمج زيفينابانت مع تثبيط ATR وPARP لتعزيز تأثير الإشعاع على خلايا سرطان الرأس والعنق سلبية فيروس الورم الحليمي
لماذا يهم تعزيز الإشعاع
العلاج الإشعاعي هو علاج أساسي لأورام الفم والبلعوم، لكن العديد من الأورام تقاومه، مما يدفع الأطباء إلى استخدام جرعات عالية قد تضر الأنسجة السليمة. تطرح هذه الدراسة سؤالاً عملياً ذا تبعات كبيرة للمرضى: من بين عدة أدوية سرطانية حديثة صُممت لجعل خلايا الورم أكثر عرضة للضرر، أيها ينجح فعلاً مع الإشعاع ضد سرطانات الرأس والعنق السلبية لفيروس الورم الحليمي المزروعة مختبرياً؟
العلاج الحالي وحدوده
يُعالج الأشخاص المصابون بسرطان الخلايا الحرشفية في الرأس والعنق موضعياً متقدّم غالباً بمزيج من الإشعاع ودواء الكيماوي سيسبلاتين، أو بالجراحة تليها جلسات إشعاعية. وعلى الرغم من أن هذا النهج قد يسيطر على السرطان، إلا أنه يترك غالباً آثاراً جانبية طويلة الأمد خطيرة مثل صعوبة البلع، وجفاف الفم، ومشاكل سمعية، وتلف الكلى. كثير من المرضى المسنين أو الضعفاء طبياً لا يتحملون سيسبلاتين على الإطلاق. وقد أثار ذلك اهتماماً كبيراً بـ "محسّنات الحساسية للإشعاع" — أدوية تجعل خلايا الورم أسهل قتلاً بالإشعاع بحيث يكون العلاج أكثر فعالية أو، ربما، أقل عنفاً.
دواء واعد تعثّر
أحد هذه الأدوية، زيفينابانت، حُمِّل في البداية على أنه اختراق علاجي. فهو يحاكي بروتيناً طبيعياً يُدعى SMAC ويمنع جزيئات تساعد خلايا السرطان على تجنّب الموت المبرمج. في أعمال سابقة، أدى إضافة زيفينابانت إلى العلاج الكيميائي الإشعاعي القياسي إلى تحسن في النتائج في تجربة سريرية مرحلة 2 لسرطان الرأس والعنق، مما أثار آمالاً بأن يصبح معيار علاج جديداً. لكن تجربة أكبر بكثير في المرحلة 3، اسمها TrilynX، أُوقفت مبكراً عندما أظهرت بيانات مرحلية ليس فقط غياب فائدة بل تراكماً في معدلات الوفيات ومزيداً من الآثار الجانبية في مجموعة زيفينابانت. هذا الفشل غير المتوقع خلق حاجة ملحة لإعادة تقييم مدى مساهمة زيفينابانت فعلاً مع الإشعاع، ولمقارنته باستراتيجيات أحدث أخرى.
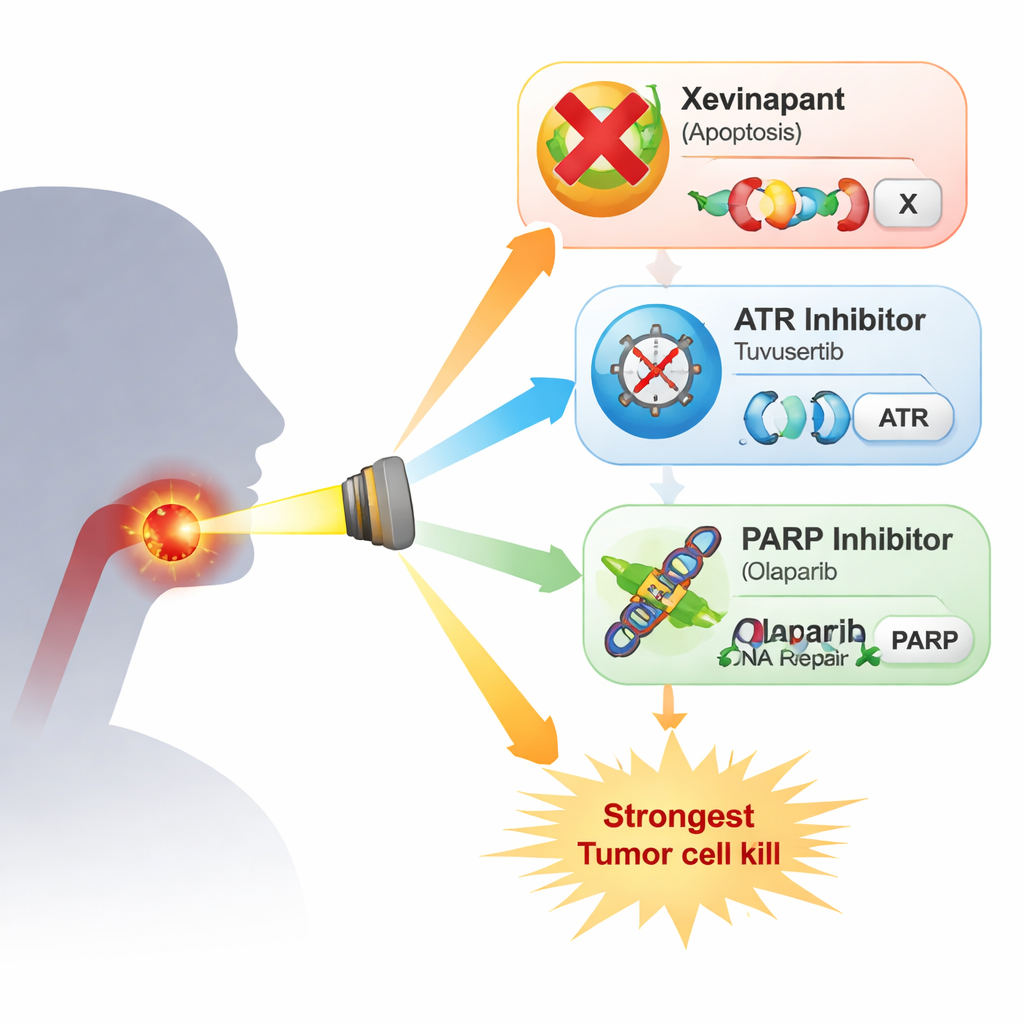
مواجهة ثلاث استراتيجيات وجهاً لوجه
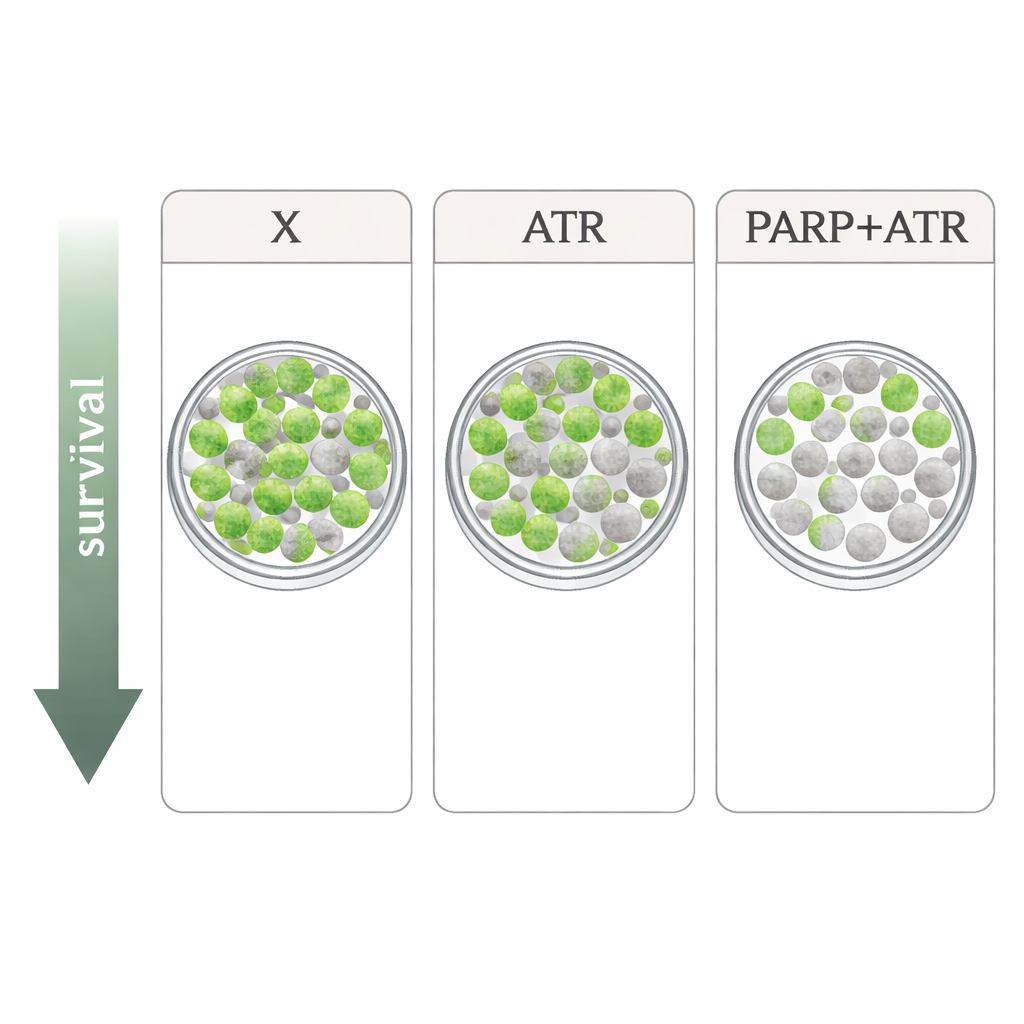
درس الباحثون أربع خطوط خلوية من سرطانات الرأس والعنق سلبية فيروس الورم الحليمي ومقاومة للإشعاع. قارنوا زيفينابانت مع عقارين يستهدفان استجابة الخلية لضرر الحمض النووي: مثبط ATR توفوسيرتيب ومثبط PARP أولاباريب، كلاهما استُخدم بجرعات مماثلة لتلك الممكن تحقيقها في المرضى. يلعب ATR وPARP أدواراً رئيسية في إيقاف دورة الخلية وإصلاح الحمض النووي بعد أضرار مثل تلك التي تسببها الأشعة السينية. في اختبارات النمو البسيطة، أبطأ كل دواء بمفرده تكاثر الخلايا بشكل طفيف فقط، وكانت الأنماط مختلفة بين خطوط الخلايا. عندما جُمِّعَت الأدوية مع الإشعاع في أشد الاختبارات صرامة — عدّ الخلايا الوحيدة القادرة على النمو لتشكيل مستعمرات — تبلورت الصورة: أعطى زيفينابانت تأثيراً إضافياً طفيفاً أو معدوماً في عدة خطوط، بينما جعل كل من توفوسيرتيب وأولاباريب الإشعاع أكثر فتكاً بشكل متسق. وكان الأثر الأقوى من الجمع بين تثبيط ATR وPARP، الذي أفضى إلى انخفاضات عميقة في بقاء المستعمرات في ثلاث من أصل أربع خطوط خلوية.
إشارات موت الخلايا ليست القصة كاملة
بما أن زيفينابانت مصمم لتحفيز موت الخلايا، قاس الفريق أيضاً عدد الخلايا التي تدخل في موت مبرمج أو تتحلل بعد العلاج، مع وبدون الإشعاع. زادت هذه مؤشرات الموت بشكل ملحوظ في بعض الظروف — خصوصاً في خط خلوي واحد اسمه HSC4 وعند الجمع بين الأدوية — لكنها لم تتوافق بشكل موثوق مع مدى كبح الإشعاع للبقاء طويل الأمد. بعبارة أخرى، كانت قراءات الموت قصيرة الأمد مؤشرات ضعيفة للحساسية الحقيقية للإشعاع. وهذا التفاوت يبرز درسا رئيسياً لتطوير الأدوية: الاختبارات التي تتبع الخلايا فترة كافية لمعرفة ما إذا كانت قادرة على إعادة النمو — مثل اختبارات تكوين المستعمرات — هي الوحيدة القادرة على الحكم بشكل صحيح ما إذا كان محسن الحساسية للإشعاع فعالاً.
ماذا يعني هذا للعلاجات المستقبلية
من هذه التجارب المخبرية، زيفينابانت لديه بعض القدرة على تعزيز الإشعاع في خلايا سرطان الرأس والعنق سلبية فيروس الورم الحليمي، لكن تأثيره كان أضعف وأقل اتساقاً من النهج التي تتدخل مباشرة في معالجة ضرر الحمض النووي عبر ATR وPARP. أتاح اقتران مثبطات ATR وPARP التأثير الأقوى، ما يوحي بأن مجموعات مدروسة الجرعات من هذه الأدوية مع العلاج الإشعاعي قد توفر مساراً أكثر وعداً من مواصلة السعي وراء زيفينابانت، على الأقل لهذا النوع من السرطان. لن يكون نقل هذه النتائج إلى العيادات أمراً مباشراً، لأن مثل هذه الأدوية قد تؤثر أيضاً على الأنسجة السريعة الانقسام السليمة وقد استلزم ذلك بالفعل خفض الجرعات في التجارب المبكرة. ومع ذلك، تشير الدراسة للأطباء والباحثين إلى أن استراتيجيات استهداف إصلاح الحمض النووي تبدو مرشحة أكثر إقناعاً لجعل العلاج الإشعاعي أكثر فعالية وربما أكثر أماناً للمرضى الذين لا يستطيعون تلقي العلاج الكيميائي القياسي.
الاستشهاد: Roehrle, J., Perugachi-Heinsohn, A., Gatzemeier, F. et al. Comparing and combining xevinapant with ATR and PARP inhibition for the radiosensitization of HPV-negative HNSCC cells. Sci Rep 16, 5882 (2026). https://doi.org/10.1038/s41598-026-38550-3
الكلمات المفتاحية: سرطان الرأس والرقبة, العلاج الإشعاعي, مثبطات إصلاح الحمض النووي, زيفينابانت, تعزيز الحساسية للإشعاع