Clear Sky Science · ar
مثبطات HDAC8 المستهدفة باستخدام مركبات [1,2,4]triazolo[4,3-a] quinoline غير الهيدروكسامات
أمل جديد لسرطان الأطفال
الورم العصبي الوليدي نوع عدواني من سرطانات الأطفال ينشأ من خلايا العصب وغالبًا ما يكون من الصعب علاجه بعد انتشاره. تستكشف هذه الدراسة طريقة جديدة لإبطاء أو قتل خلايا الورم العصبي الوليدي عن طريق إيقاف مفتاح خلوي رئيسي يسمى HDAC8. من خلال بناء عائلة جديدة من الجزيئات الشبيهة بالأدوية التي تعمل بانتقائية عالية على هذا المفتاح، يسعى الباحثون إلى ابتكار علاجات أكثر فعالية ضد الأورام وألطف على بقية الجسم.
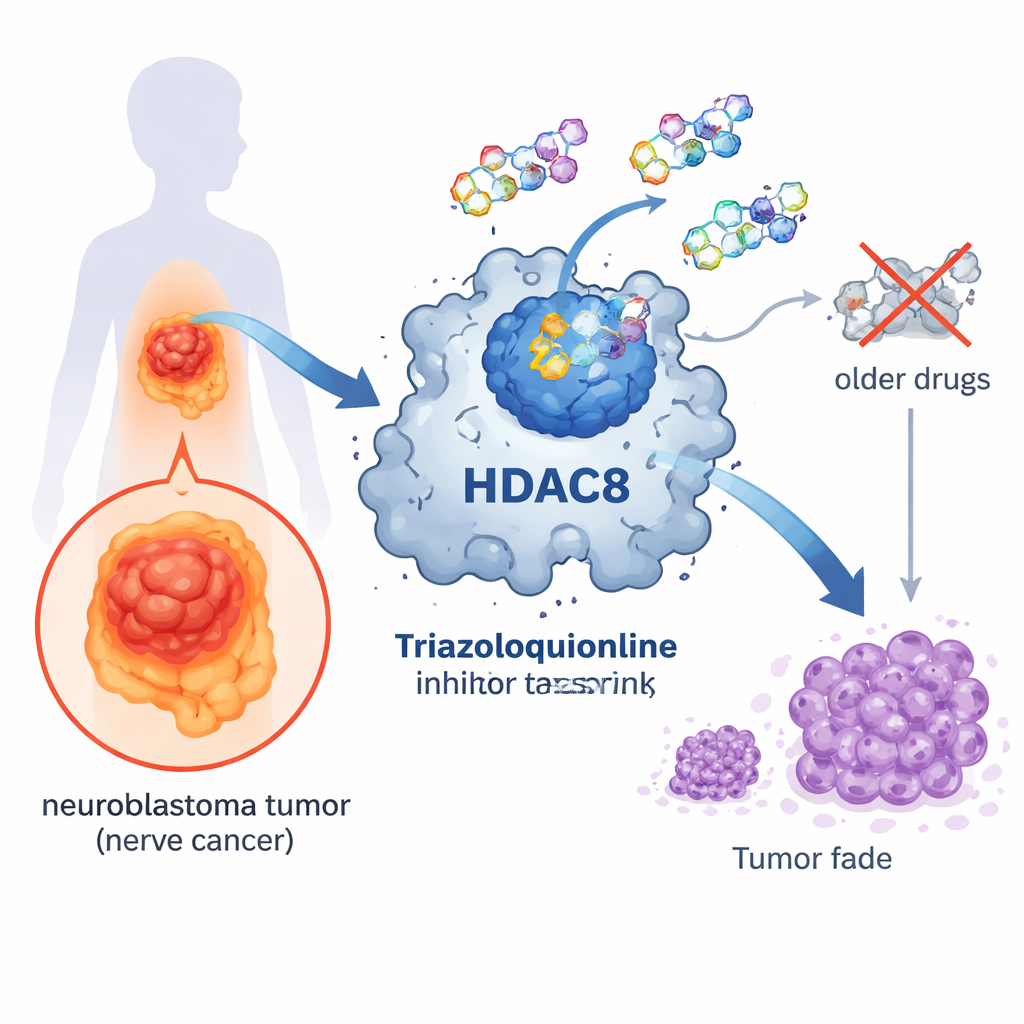
مفتاح جزيئي في قلب السرطان
داخل خلايانا، تُشغّل وتُطفأ الجينات باستمرار. أحد أنظمة التحكم المهمة يعتمد على علامات كيميائية صغيرة تُسمى مجموعات الأستيل التي تلتصق بالبروتينات المرتبطة بالحمض النووي. إنزيمات تُدعى ديأسيتلاز الهيستون (HDACs) تزيل هذه العلامات، مما يؤدي إلى تشديد تغليف الحمض النووي وعادةً إلى خفض نشاط الجينات. يُعد HDAC8 أحد أعضاء هذه العائلة من الإنزيمات وقد رُبط بعدة سرطانات، بما في ذلك الورم العصبي الوليدي. عندما يكون HDAC8 مفرط النشاط، يمكن لخلايا السرطان أن تنمو وتبقى على قيد الحياة وتنتشر بسهولة أكبر، مما يجعله هدفًا جاذبًا للأدوية الجديدة.
قيود أدوية HDAC القديمة
هناك عدة أدوية تعيق HDAC تمت الموافقة عليها بالفعل لبعض سرطانات الدم، لكنها تميل إلى استهداف عدة أنواع من HDAC في آن واحد. تستخدم معظم هذه الأدوية مجموعة هيدروكسامات لالتحام بأيون المعدن في الموقع النشط للإنزيم. ورغم فعاليتها، فإن هذه المجموعة ترتبط بالمعادن بقوة كبيرة مما قد يؤدي إلى آثار جانبية ويحد من قدرة الدواء على التمييز بدقة بين أنواع HDAC المختلفة. ونتيجة لذلك قد يعاني المرضى من سمية وتتعرض الخلايا الطبيعية للضرر إلى جانب خلايا السرطان. لذلك بحث الباحثون عن تصاميم كيميائية بديلة تحافظ على الفوائد المضادة للسرطان مع تقليل الأضرار غير المرغوبة.
تصميم فئة جديدة من المثبطات المستهدفة
في هذا العمل، صمم الفريق وركب 21 مركبًا جديدًا مبنيًا حول جسور تريازولوكوينولين، متصلة من خلال رابط مرن بمنطقة «ألفا-أمين أميد» قادرة على ربط ذرة الزنك في الموقع النشط لـ HDAC8. باستخدام التصميم الموجه بالحاسوب، اختاروا هذا البناء ليناسب قناة ضيقة لإفراز الأسيتيت فريدة في HDAC8، وهي ميزة هيكلية تساهم في تحقيق انتقائية عالية. أظهرت دراسات الإرساء التفصيلية ومحاكاة الديناميكيات الجزيئية أن عدة جزيئات جديدة — لا سيما 9m و9r — تُكون تفاعلات مستقرة وطويلة الأمد داخل جيب HDAC8 وتترابط بقوة مساوية أو أكبر من مثبط مرجعي معروف. والأهم من ذلك، أكدت الاختبارات البيوكيميائية أن أفضل المركبات تمنع HDAC8 بقوة بينما تترك أعضاء عائلة HDAC الأخرى إلى حد كبير دون تأثير.
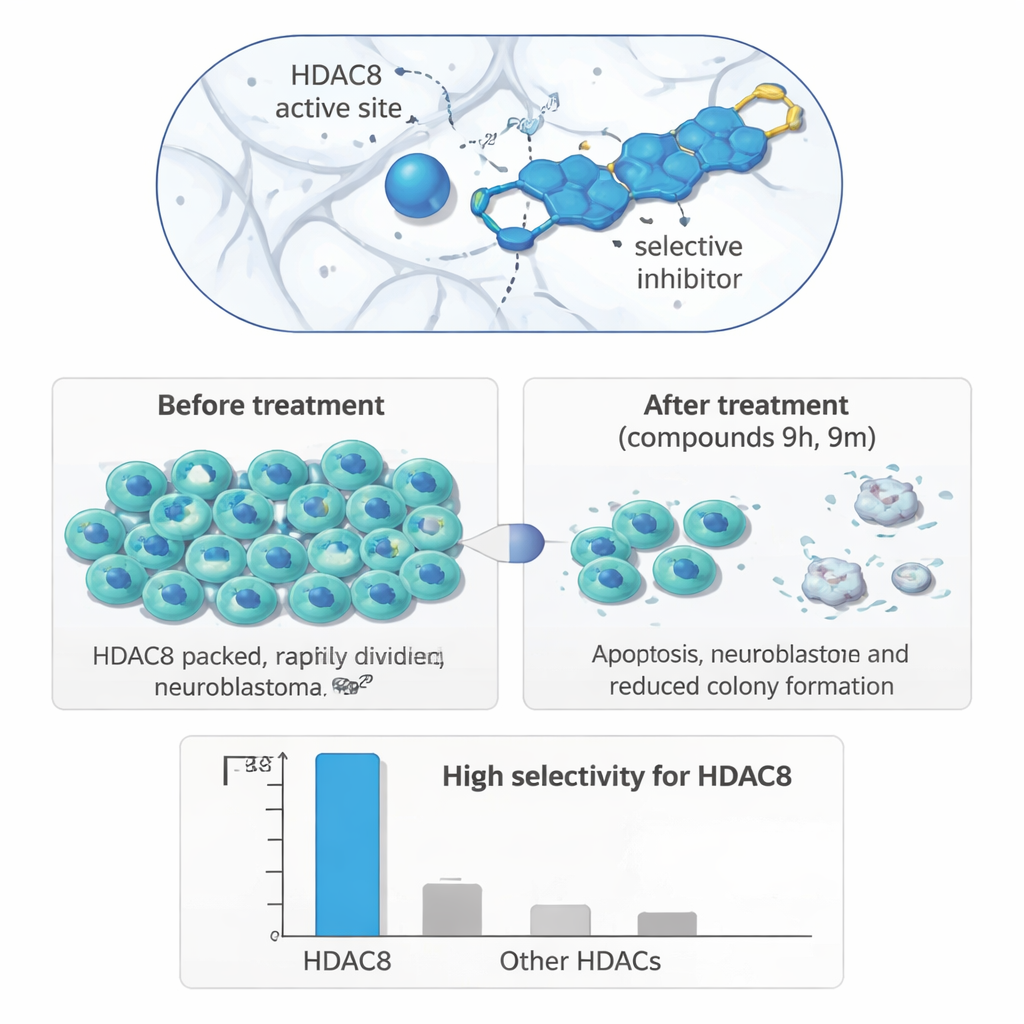
من أنبوب الاختبار إلى خلايا الورم
لفحص ما إذا كان هذا الاستهداف الدقيق للإنزيم يترجم إلى تأثيرات بيولوجية مفيدة، اختبر الباحثون مركباتهم على مجموعة من خطوط الخلايا البشرية. في خلايا الورم العصبي الوليدي (IMR‑32)، برزت جزيئتان، 9h و9m، بوضوح: فقد قلّصتا نمو الخلايا عند تراكيز ميكرومولارية وفعلتا ذلك بقوة أكبر في الورم العصبي الوليدي مقارنةً بخلايا سرطان الثدي أو القولون، أو خلايا الكلية غير السرطانية. أظهرت تجارب تكوين المستعمرات طويلة الأمد أن الخلايا المعالجة فقدت جزءًا كبيرًا من قدرتها على إعادة النمو بعد التعرض للدواء. وفي تجربة شفاء الجروح، التي تتتبع مدى سرعة تحرك الخلايا لسد خدش في طبقة خلوية، أبطأت المركباتان حركة خلايا الورم العصبي الوليدي، مما يوحي بتقليل الإمكانية النقيلية.
تحري كيفية قتل المركبات لخلايا السرطان
أظهرت تجارب التحليل الخلوي بتقنية تدفق الخلايا أن 9h و9m يحفزان موت الخلايا المبرمج (الاستماتة) في خلايا الورم العصبي الوليدي ويتسببان في تراكم الخلايا في طور من دورة الخلية مرتبط بتلف الحمض النووي أو الموت (Sub‑G1). وللتأكد من أن هذه التأثيرات تنشأ فعلًا من حجب HDAC8، قاس الفريق حالة استيلان بروتين يُدعى SMC3، وهو هدف معروف لـ HDAC8 ويشارك في الحفاظ على اقتران الكروموسومات الشقيقة أثناء انقسام الخلية. عندما يُثبط HDAC8، يتراكم SMC3 المستؤل. بعد المعالجة بـ 9h أو 9m، ارتفعت مستويات SMC3 المستؤل بشكل حاد، بينما ظل إجمالي بروتين SMC3 دون تغيير — دليل قوي على أن هذه المركبات تؤثر مباشرة على HDAC8 في الخلايا الحية وتعطل وظيفته الطبيعية في التحكم بالكروموسومات.
ماذا قد يعني هذا للعلاجات المستقبلية
معًا، ترسم الكيمياء والنمذجة الحاسوبية واختبارات الإنزيمات والتجارب الخلوية صورة متسقة: فالمركبات التريازولوكوينولين الجديدة هي مثبطات قوية وذات انتقائية عالية لـ HDAC8 يمكنها الحد من نمو وانتشار خلايا الورم العصبي الوليدي مع الحفاظ على باقي إنزيمات HDAC. وبما أنها تتجنب مجموعة الهيدروكسامات التقليدية، فقد توفر مسارًا أكثر أمانًا لاستهداف HDAC8 علاجيًا. رغم أن الكثير من العمل لا يزال مطلوبًا — خاصة دراسات على الحيوان وتجارب سريرية مستقبلية — فإن هذا البحث يضع أساسًا صلبًا لتطوير أدوية أكثر دقة ضد الورم العصبي الوليدي لدى الأطفال وربما أمراض أخرى مدفوعة بـ HDAC8.
الاستشهاد: Bandaru, N.V.M.R., Fathima, A., Sengar, S. et al. Targeted HDAC8 inhibition with non-hydroxamate [1,2,4]triazolo[4,3-a] quinoline compounds. Sci Rep 16, 7472 (2026). https://doi.org/10.1038/s41598-026-38490-y
الكلمات المفتاحية: مثبطات HDAC8, الورم العصبي الوليدي, العلاج فوق الجيني, تريازولوكوينولين, أدوية السرطان المستهدفة