Clear Sky Science · ar
نموذج تعلّم آلي قابل للتفسير يستخدم بيانات سريرية روتينية للتنبؤ بالانتكاس المبكر في سرطان الكبد الخلوي
لماذا هذا مهم للمرضى والعائلات
بالنسبة للأشخاص الذين يخضعون لعملية جراحية لاستئصال سرطان الكبد، فإن أحد أكثر الأسئلة إلحاحًا هو: «هل سيعود السرطان قريبًا؟» اليوم، يمكن للأطباء تقديم تقديرات تقريبية فقط، غالبًا استنادًا إلى أنظمة تصنيف واسعة تعامل العديد من المرضى وكأنهم متشابهون. تقدّم هذه الدراسة نهجًا جديدًا للاستفادة من المعلومات التي تجمعها المستشفيات بالفعل — اختبارات دم روتينية ونتائج فحوصات التصوير — إلى جانب ذكاء اصطناعي قابل للتفسير لتقديم صورة أوضح وأكثر تخصيصًا لكل مريض حول مخاطر رجوع السرطان على المدى القصير.
سرطان شائع مع معدل عودة عنيد
يُعدُّ سرطان الكبد الخلوي أكثر أنواع سرطانات الكبد الأولية شيوعًا وهو سبب رئيسي لوفيات السرطان على مستوى العالم. حتى عندما يزيل الجراحون الأورام الظاهرة بالكامل، يعود المرض لدى أكثر من 70% من المرضى خلال خمس سنوات. الانتكاس المبكر — خلال حوالي سنتين بعد الجراحة — مثير للقلق بشكل خاص، لأنه عادةً ما يعكس خلايا سرطانية عدوانية قد انتشرت بالفعل داخل الكبد، ويؤثر بقوة على البقاء على قيد الحياة. أنظمة التصنيف السريرية الحالية، مثل TNM أو نظام برشلونة لتصنيف سرطان الكبد (BCLC)، تستطيع ترتيب المرضى إلى فئات عامة إلى حد ما لكنها غالبًا ما تفشل في تحديد من هم فعلاً الأكثر عرضة لعودة مبكرة للسرطان.
تحويل نتائج الفحوصات اليومية إلى درجة مخاطرة
استند الباحثون إلى سجلات 1,120 مريضًا خضعوا لجراحة كانت تبدو علاجية في مستشفيين رئيسيين في الصين بين 2014 و2024. ركزوا فقط على المعلومات المتاحة قبل العملية: العمر والجنس، وميزات التصوير مثل حجم أكبر ورم وما إذا كانت الأورام متعددة، ومجموعة واسعة من الاختبارات المخبرية القياسية التي أُجريت في الأيام التي سبقت الجراحة. من بين هذه المعطيات، انتقوا تسعة مؤشرات رئيسية مرتبطة بفرصة الانتكاس. بدل الاعتماد على صيغة رياضية واحدة، دمجوا ثلاث مقاربات مختلفة للتعلّم الآلي واحتسبوا متوسط نواتجها ليكوّنوا درجة مخاطرة واحدة بين 0 و1. ثم وُضِع المرضى في فئات منخفضة ومتوسطة وعالية المخاطرة استنادًا إلى هذه الدرجة. 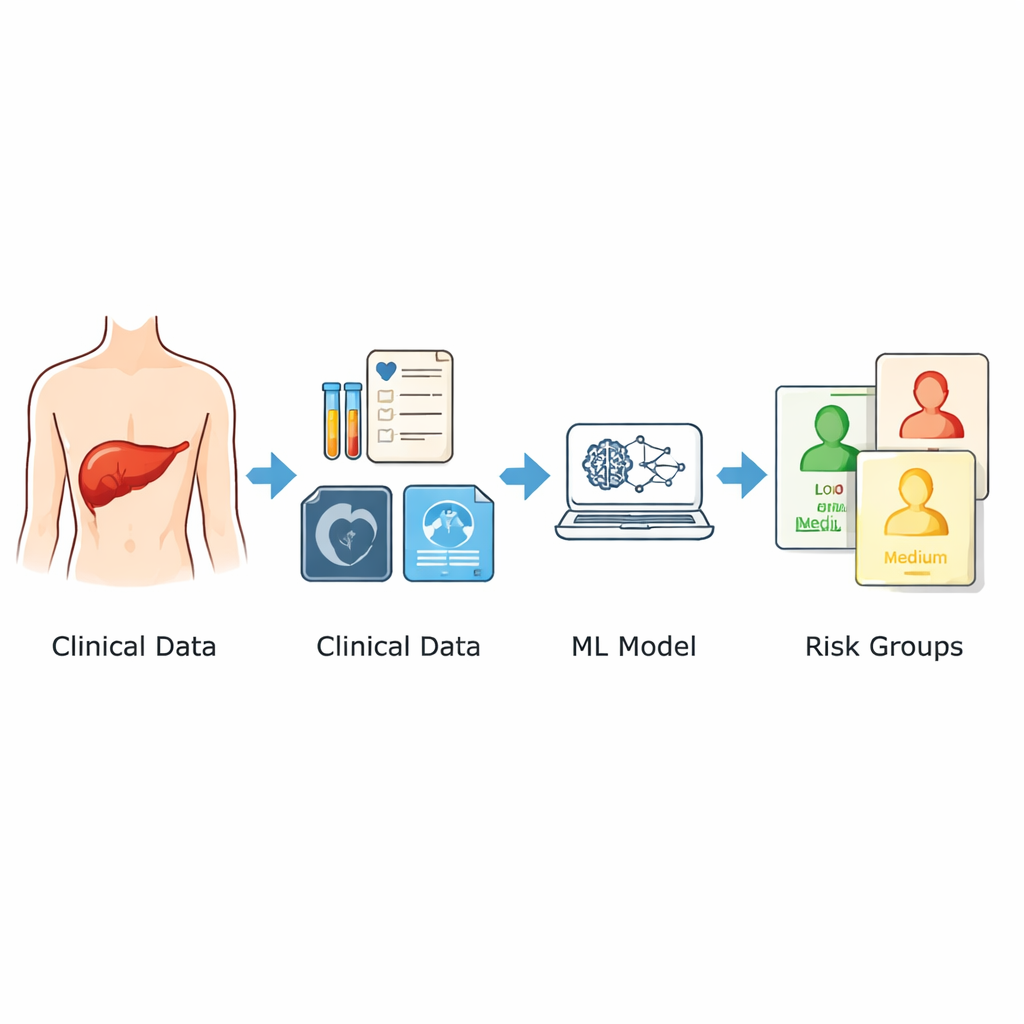
تفوق على أنظمة التصنيف القياسية
لاختبار أداء النموذج، قيّمه الفريق أولًا على مجموعة احتُجزت جانبًا من نفس المستشفى الأصلي ثم على مجموعة مستقلة من المستشفى الثاني. في كلا الحالتين، كان النموذج الجديد أفضل بوضوح من أنظمة التصنيف التقليدية في تمييز من سيظل خاليًا من السرطان ومن سيعاود له خلال 24 شهرًا. في مجموعة الاختبار الداخلية، كانت دقة النموذج على مدى الزمن، المقاسة بإحصائية قياسية تُسمى المساحة تحت المنحنى، نحو 0.76، مقارنة بحوالي 0.55 إلى 0.64 لطرق التصنيف الشائعة. كان لدى الأشخاص في فئة المخاطرة العالية أسوأ معدل للبقاء خاليًا من الانتكاس، وقد خُفضت مخاطر العودة لدى فئة المخاطرة المتوسطة بنحو 60%، وكانت فئة المخاطرة المنخفضة لديها مخاطر أقل بنحو 90% مقارنة بالفئة العالية. ظلت هذه الفروق القوية صحيحة أيضًا في المستشفى الخارجي ومتسقة عبر معظم الفئات الفرعية، مثل المرضى الأصغر والأكبر سنًا، والرجال والنساء، ومن لديهم أورام كبيرة أو صغيرة.
فتح الصندوق الأسود للذكاء الاصطناعي
من الانتقادات المتكررة لتطبيق التعلّم الآلي في الطب أنه يتصرف كصندوق أسود: قد يتنبأ جيدًا لكن حتى المتخصصين لا يستطيعون رؤية السبب. لمعالجة ذلك، طبق المؤلفون طريقة تُسمَّى توضيحات Shapley الإضافية (SHAP)، التي تُفكك كل تنبؤ إلى مساهمات كل عامل مدخل. أظهرت التحليلات أن حجم الورم كان العامل الأقوى الوحيد الذي يدفع نحو مخاطر أعلى عبر الخوارزميات الثلاث جميعها، تلاه خصائص مثل عدد الأورام ومؤشرات دموية لوظيفة الكبد والالتهاب. ومن المثير للاهتمام أن مستوى الكلوريد في الدم كان يميل إلى دفع الخطر في الاتجاه المعاكس، إذ عمل كعامل وقائي في هذه المجموعة من البيانات. بالنسبة للمرضى الأفراد، يمكن للنموذج أن يولّد رسومًا بيانية بسيطة على شكل أشرطة تُظهر، على سبيل المثال، كيف يدفع قُطر الورم الكبير والمؤشرات الدموية غير المواتية درجة المخاطرة إلى الأعلى، بينما تسحب علامة وظائف الكبد الأفضل الدرجة إلى الأسفل. 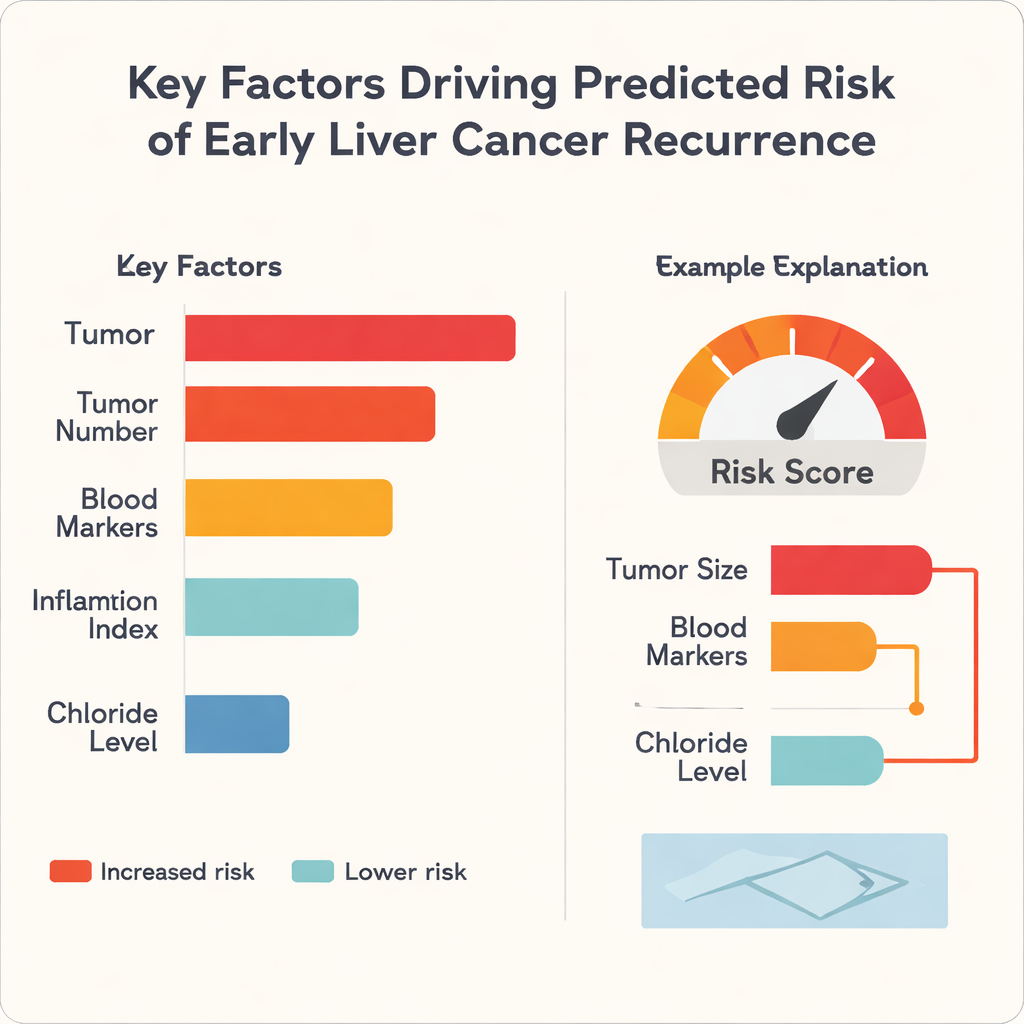
ماذا قد يعني هذا في العيادة
لأن النموذج يعمل على بيانات تجمعها المستشفيات بالفعل ولا يتطلب فحوصًا خاصة أو اختبارات جينية مكلفة، فقد يمكن نشره في العديد من بيئات الرعاية المختلفة، بما في ذلك تلك ذات الموارد المحدودة. قبل الجراحة، يمكن للأطباء استخدامه لتحديد الأشخاص الذين يحتاجون إلى جداول متابعة أكثر كثافة أو الذين قد يستفيدون من علاجات إضافية بعد الجراحة، مع توفير اختبارات وقلق غير ضروريين للمرضى ذوي المخاطر الحقيقية المنخفضة. ويشير المؤلفون إلى أن دراستهم استعادية ومأخوذة من مجموعة سكانية محددة، لذا ما تزال هناك حاجة إلى تجارب مستقبلية في بيئات أكثر تنوعًا. ومع ذلك، توضح دراستهم كيف يمكن للذكاء الاصطناعي الشفاف والقابل للتفسير أن يحوّل أرقام المختبرات ونتائج الفحوص المعروفة إلى توقعات مخصّصة ذات معنى تدعم اتخاذ القرار المشترك بين المرضى وفرق الرعاية الخاصة بهم.
الاستشهاد: Guo, DF., Wen, Q., Zhang, X. et al. An interpretable machine learning model using routine clinical data for early recurrence prediction in hepatocellular carcinoma. Sci Rep 16, 7520 (2026). https://doi.org/10.1038/s41598-026-38484-w
الكلمات المفتاحية: انتكاس سرطان الكبد, نموذج تعلّم آلي, تنبؤ المخاطر السريرية, الذكاء الاصطناعي القابل للتفسير, سرطان الكبد الخلوي