Clear Sky Science · ar
مُثبِّط G9a المزدوج ومُضاد مستقبل الهيستامين H3 A-366 يحسن السلوكيات المتكررة والاجتماعية ويخفّف الالتهاب العصبي في فئران BTBR T + tf/J
لماذا تهم هذه الدراسة الفأرية في موضوع التوحد
تواجه العائلات التي تعيش مع اضطراب طيف التوحد (ASD) غالبًا خليطًا من العلاجات التي تُخفّف بعض الأعراض فقط في كل مرة. تستكشف هذه الدراسة مركبًا تجريبيًا جديدًا يُسمى A-366، صُمم ليؤثر في نظامين حيويين مختلفين في الوقت نفسه. في نموذج فأري واسع الاستخدام للسلوكيات المشابهة للتوحد، قلّل A-366 من الأفعال المتكررة، وحسّن التفاعل الاجتماعي، وهدّأ الالتهاب الدماغي، مما يشير إلى احتمال أن دواء واحدًا قد يعالج عدة سمات أساسية لـ ASD معًا في المستقبل.
حالة ذات أجزاء متحركة متعددة
لا يُعَدّ ASD مرضًا وحيد السبب أو الشكل. يشمل صعوبات في التواصل الاجتماعي، وسلوكيات متكررة، وغالبًا تحديات أخرى مثل القلق أو مشاكل الانتباه. وراء هذه العلامات الظاهرة توجد سلسلة من التغيرات في كيمياء الدماغ وتنظيم الجينات. تستهدف الأدوية الحالية، مثل مضاد الذهان أريبيبرازول، أساسًا أنظمة الرسول في الدماغ مثل الدوبامين والسيروتونين، وموافَقَةٌ عليها فقط لأعراض مصاحبة مثل السُرْعَة أو الانزعاج. وفي الوقت نفسه، كشفت الأبحاث أن طريقة تغليف الـ DNA والتعليمات الكيميائية عليه داخل خلايا الدماغ — أي فوق الجينات (الإبيجنتيك) — تتغير أيضًا في ASD، كما تتغير فعالية الاستجابات المناعية والالتهابية في الدماغ. تشير هذه الطبقات المتعددة إلى أن نهج "هدف واحد في كل مرة" قد يكون ضيقًا جدًا.
استهداف مفاتيح الجين ورسائل الدماغ معًا
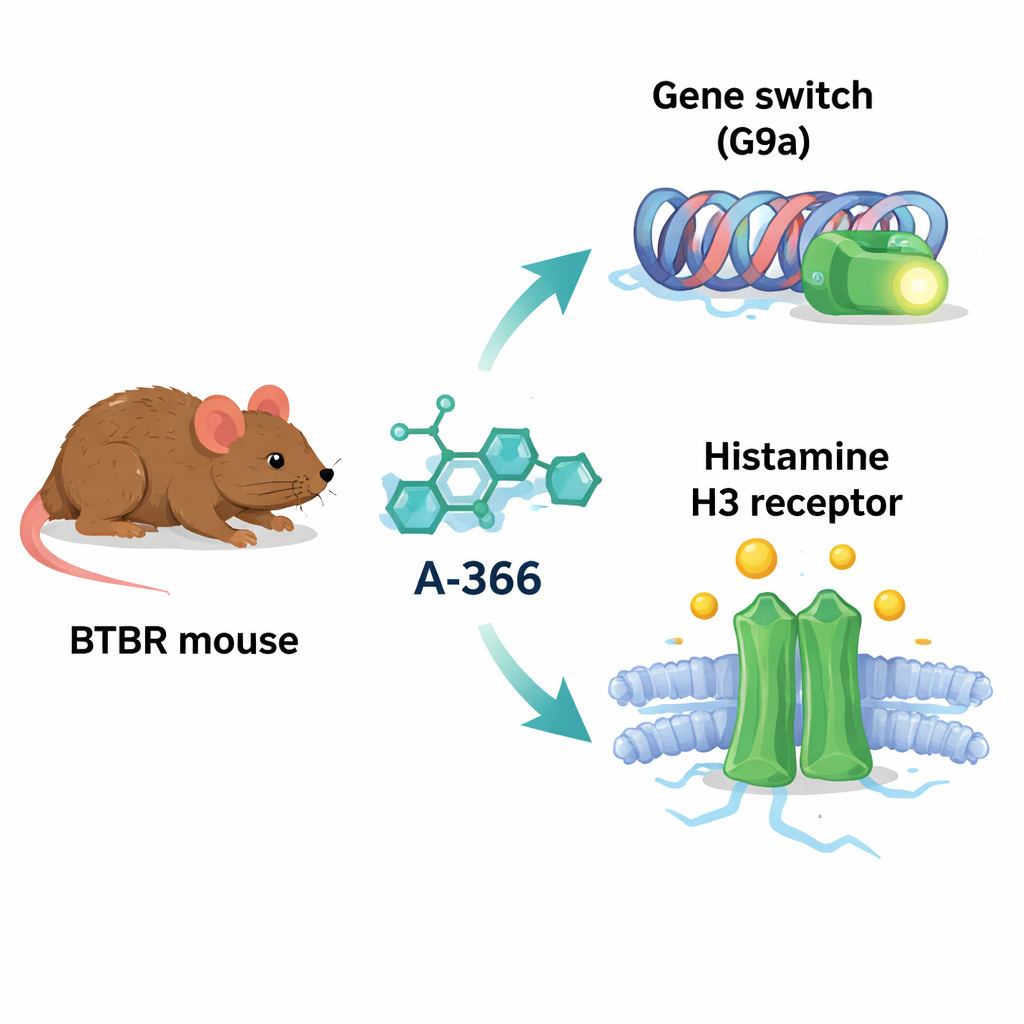
طُوِّر A-366 أصلاً ليُعطِّل بروتينًا يُسمى G9a، وهو إنزيم يضيف علامات كيميائية على بروتينات الهيستون ويميل إلى خفض نشاط الجينات. في عدة اضطرابات دماغية، ترتفع نشاطات G9a وعلاماته، ما قد يُسكت جينات مهمة للتعلّم والذاكرة والتوصيل السليم للدماغ. ومن المثير أن الشكل الكيميائي لـ A-366 يُشبه أيضًا أدوية تُعطِّل مستقبل الهيستامين H3، وهو مفتاح يتحكم في إفراز الهيستامين وناقلات عصبية أخرى وارتبط بالانتباه واليقظة والسلوك الاجتماعي. بسبب هذا التشابه، افترض الباحثون أن A-366 قد يعمل كـ "عامل مزدوج": فكّ كبح الجينات الضار عبر تثبيط G9a وفي الوقت نفسه تعزيز إشارات الهيستامين عن طريق حجب مستقبلات H3.
اختبار A-366 في فئران شبيهة بالتوحد
عمل الفريق مع فئران BTBR T+tf/J، سلالة تظهر طبيعيًا قلة الاجتماع الاجتماعي، وحلاقة وحفر متكررة قوية، وارتفاعًا في الالتهاب الدماغي — سمات تردّد جوانب رئيسية من ASD. تلقّى ذكور BTBR حقنًا يومية من A-366 لمدة ثلاثة أسابيع بثلاث جرعات مختلفة، وقورنت سلوكياتهم مع فئران C57 النموذجية ومع فئران BTBR عولجت إما بالبيتوليسانت (مُثبِّط قياسي لمستقبل H3) أو الأريبيبرازول. عبر مهمات متعددة، خفّض A-366 الحفر والتخريم والحلاقة الذاتية بشكل يعتمد على الجرعة وحسّن الأداء في اختبار متاهة Y لذاكرة العمل المكانية. في اختبار اجتماعي ذو ثلاث حجرات، لم يستعد A-366 فقط تفضيل الفئران لقضاء الوقت مع فأر آخر مقابل قفص فارغ، بل في أعلى جرعة رفع درجات السلوك الاجتماعي إلى مستوى الفئران النموذجية وتفوق في تأثيره على تأثيرات البيتوليسانت والأريبيبرازول.
تهدئة الالتهاب وتأكيد الأهداف
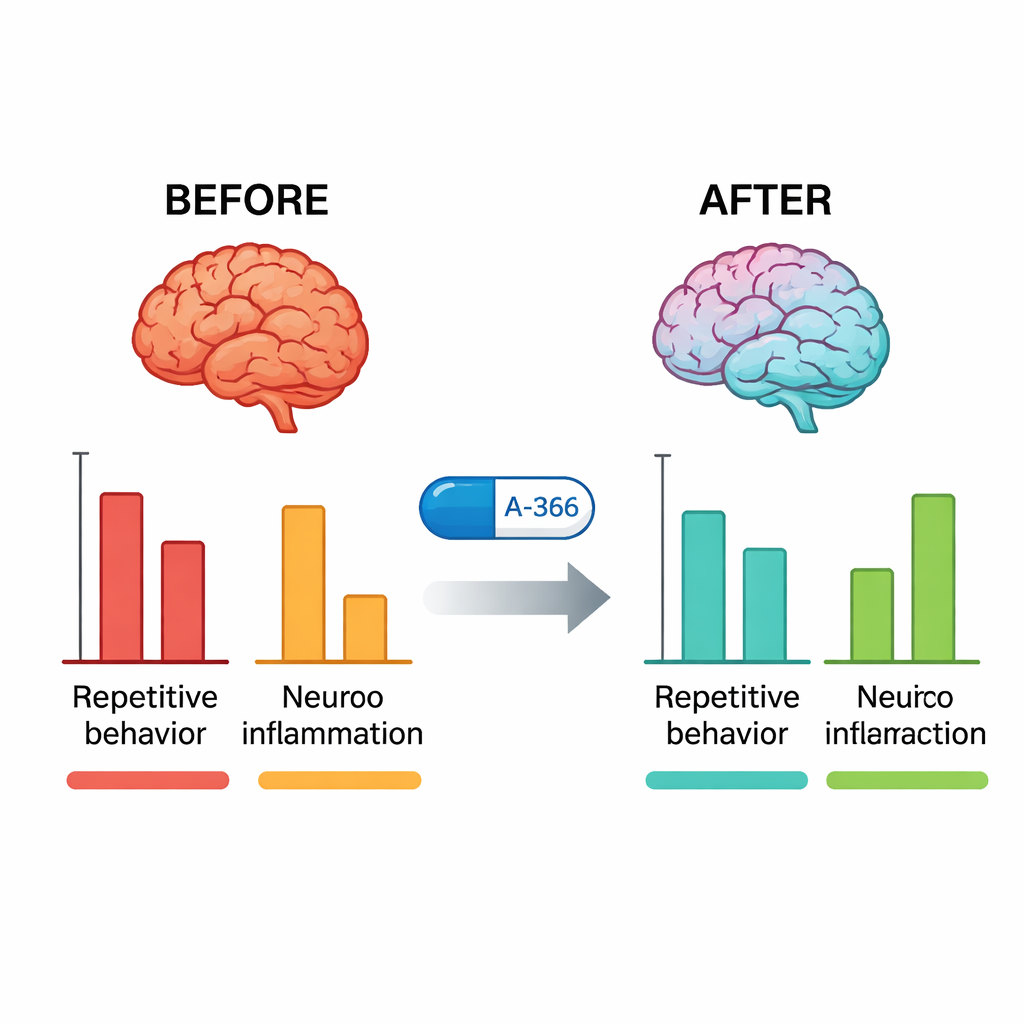
بعد اختبارات السلوك، فحص الباحثون أدمغة الفئران. في فئران BTBR غير المعالجة، كان نشاط G9a في الحُصين والمخيخ أعلى بكثير من الفئران النموذجية. خفّض العلاج بـ A-366 هذا النشاط بشكل حاد نحو الطبيعي، بينما لم يفعل البيتوليسانت وحده ذلك، مما يؤكد أن A-366 يَستهدف فعلاً آليته فوق الجينية. وفي الوقت نفسه، كانت جزيئات الالتهاب الأساسية — TNF-α وIL-6 وIL-1β — مرتفعة جدًا في فئران BTBR وانخفضت بشكل ملحوظ بواسطة A-366، أكثر مما فعل الأريبيبرازول. عندما أضاف العلماء دواءً ينشط مستقبلات H3 (RAMH) بالإضافة إلى A-366، انعكست الفوائد السلوكية والمضادة للالتهاب جزئيًا فقط، وظل انخفاض نشاط G9a قائمًا. يدعم هذا النمط آلية مركّبة: تخفيف فوق جيني مستقر عبر تثبيط G9a بالإضافة إلى مساهمة تتوسطها الهيستامين عبر حجب مستقبل H3.
ماذا قد يعني هذا لعلاجات المستقبل
لغير المتخصص، توحي هذه النتائج بأنه قد يكون ممكنًا تصميم أدوية تعمل على "البرمجيات" و"نظام الرسائل" في الدماغ معًا. في هذا النموذج الفأري للشبه بالتوحد، سهّل A-366 الأفعال المتكررة، وحسّن التفاعل الاجتماعي، وخفّض علامات الالتهاب الدماغي المزمن عبر فكّ كبتات جينية ضارة وضبط إشارات الهيستامين في الوقت نفسه. صُمم A-366 أصلاً لأمراض أخرى وسيحتاج إلى تحسين واختبارات أمان واسعة قبل أي استخدام بشري. مع ذلك، يقدّم نموذجًا لفئة جديدة من الأدوية متعددة الأهداف تستهدف البيولوجيا المعقدة لـ ASD، حيث إن معالجة مسار واحد فقط في كل مرة أمدّت حتى الآن بتخفيف محدود.
الاستشهاد: Hajar, M., Jayaprakash, P., Stark, H. et al. The dual G9a inhibitor and histamine H3 receptor antagonist A-366 improves repetitive and social behaviors and attenuates neuroinflammation in BTBR T + tf/J mice. Sci Rep 16, 7105 (2026). https://doi.org/10.1038/s41598-026-38481-z
الكلمات المفتاحية: اضطراب طيف التوحد, علاج فوق جيني, مستقبل الهيستامين H3, التهاب عصبي, نموذج فأري