Clear Sky Science · ar
يعيد aFGF الشباب إلى الخلايا الليفية المسنة الناجمة عن الجلوكوز العالي ويُحسّن شفاء جروح السكري عبر تنظيم مسار SIRT1/STAT3
لماذا تهم الجروح ذات الشفاء البطيء
بالنسبة لكثير من الأشخاص المصابين بالسكري، قد تتحول جرح صغير في القدم أو الساق إلى قرحة عنيدة تبقى لفترة طويلة، أحياناً تؤدي إلى عدوى أو حتى بتر. هذه القروح المزمنة ليست مشكلة سطحية فحسب: خلايا الجلد التي ينبغي أن تبني النسيج المتضرر غالباً ما تتقدم في العمر قبل أوانها وتتوقف عن العمل بشكل صحيح. تستعرض هذه الدراسة نهجاً واعداً لـ «إعادة شباب» بعض تلك الخلايا باستخدام إشارة إصلاح طبيعية، بهدف مساعدة جروح السكري على الانغلاق بشكل أسرع وأكثر اكتمالاً.
خلايا تشيخ مبكراً
تعتمد البشرة السليمة على الخلايا الليفية — وهي خلايا داعمة تعيش في الطبقات العميقة من الجلد — لتتكاثر، وتهاجر إلى الجرح، وتضع القالب اللازم للنسيج الجديد. في حالة السكري، يدفع ارتفاع السكر المزمن والجزيئات المتضررة بالسكر هذه الخلايا الليفية إلى حالة تُسمى الشيخوخة الخلوية أو السِنِنَة. الخلايا الليفية المسنة تفقد قدرتها على الانقسام، وتنتج كميات أقل من البروتينات البنائية اللازمة للإصلاح، وبدلاً من ذلك تطلق خليطاً من العوامل المحفزة للالتهاب التي تغذي حالة الالتهاب المستمرة. يبيّن المؤلفون أنه في الفئران المصابة بالسكري، يحتوي الجلد المحيط بالجرح على عدد أكبر من هذه الخلايا الليفية المسنة وأقل من بروتينات المصفوفة المفيدة، مما يتطابق مع بطء شديد في الشفاء.
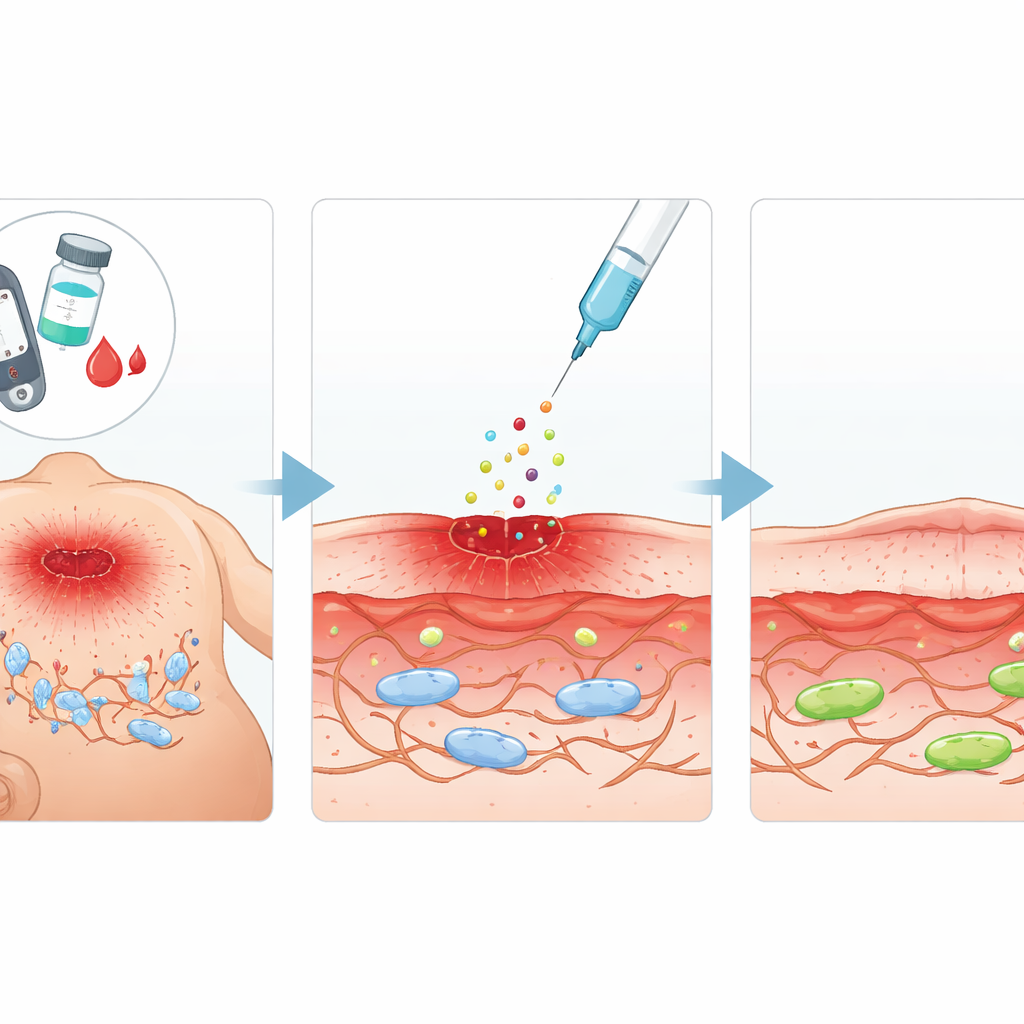
إشارة إصلاح ذات وعد
ركّز الفريق على عامل النمو الليفي الحمضي (aFGF)، وهو بروتين طبيعي معروف بتشجيعه لنمو الخلايا وإصلاح الأنسجة. تساءلوا عما إذا كان aFGF يمكنه ليس فقط تعزيز نشاط الخلايا الليفية، بل أيضاً عكس التغيرات الشبيهة بالشيخوخة الناجمة عن ارتفاع السكر. في فئران سكريّة، صنعوا جروحاً جلدية معيارية وحقنوا aFGF حول المنطقة المصابة كل بضعة أيام. مقارنةً بالحيوانات المصابة دون علاج، أظهرت الفئران المعالجة بـ aFGF تقلصاً أسرع لمساحة الجرح، وإعادة بناء أفضل للأنسجة تحتها، وانخفاضاً في مستويات العلامات الدالة على الشيخوخة الخلوية. في تجارب مخبرية موازية باستخدام سلالة خلايا ليفية من الفأر تعرضت لجلوكوز مرتفع جداً، أعاد aFGF قدرة الخلايا على الانقسام والهجرة — سلوكان ضروريان لإغلاق الجرح.
تهدئة الإجهاد التأكسدي داخل الخلايا
لا يقتصر أثر ارتفاع السكر في الدم على تغذية الخلايا بالوقود الزائد فحسب: بل يدفع أيضاً إلى الإفراط في إنتاج أنواع الأكسجين التفاعلية، وهي جزيئات غير مستقرة تتلف البروتينات والدهون والحمض النووي. هذا الإجهاد التأكسدي هو محفز رئيسي لدخول الخلايا الليفية في حالة السِنِنَة. قاس الباحثون عدة مؤشرات معيارية لهذا الإجهاد في نموذج الخلايا لديهم، بما في ذلك نواتج الضرر ونشاط إنزيمات مضادات الأكسدة الخلوية. تحت ظروف الجلوكوز العالي، أظهرت الخلايا الليفية مزيداً من التلف ودفاعات مضادة للأكسدة أضعف. عند إضافة aFGF، تحوّلت الموازنة: انخفضت المؤشرات الضارة، وزاد نشاط الإنزيمات الواقية. وهذا يوحي بأن aFGF يساعد على استعادة بيئة داخلية أكثر صحة، ما يقلل احتمال انزلاق الخلايا الليفية إلى حالة مسنة دائمة.
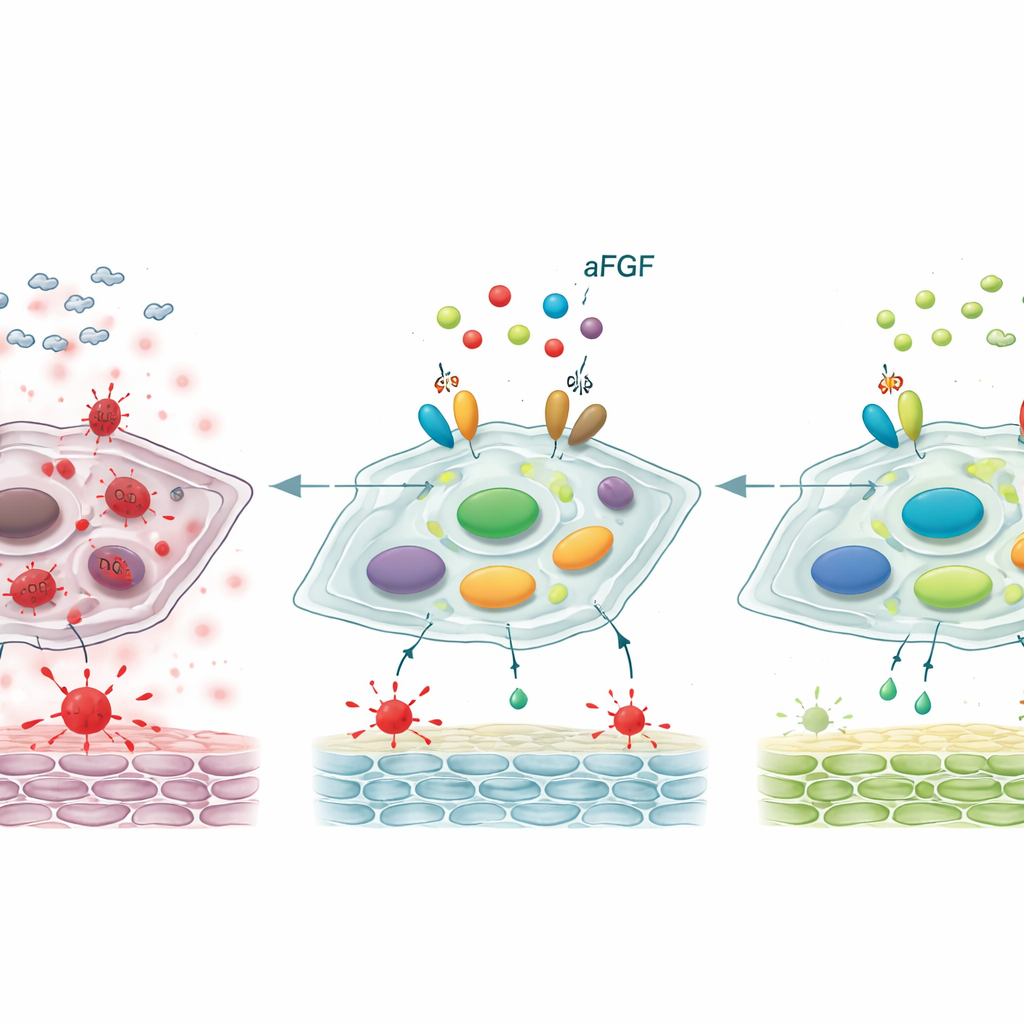
إعادة ضبط مفتاح تحكّم أساسي
بتعمق أكثر، فحص العلماء محور تحكم جزيئي يشمل بروتينين، SIRT1 وSTAT3، اللذين يؤثران معاً على ما إذا كانت الخلايا الليفية تظل شابة أو تدخل السِنَنَة. في جروح السكري والخلايا المعالجة بالجلوكوز العالي، كانت مستويات SIRT1، الحارس المرتبط بمقاومة الإجهاد، منخفضة، بينما ازداد الشكل المنشط من STAT3 — وهو محرك للسلوك الالتهابي والشيخوخي. قلب العلاج بـ aFGF هذا النمط: ارتفع SIRT1، وانخفض STAT3 المنشط. عندما عطل الفريق SIRT1 بمثبط محدد، فقد aFGF إلى حد كبير قدرته على تقليل الإجهاد التأكسدي، وكبح علامات الشيخوخة، وتسريع إغلاق الجروح في الفئران. يشير هذا إلى أن التأثيرات المفيدة لـ aFGF تعتمد بقوة على إعادة تنشيط SIRT1، الذي بدوره يكبح STAT3 والبرنامج الضار للشيخوخة الذي يتحكم به.
ماذا يمكن أن يعني ذلك للمرضى
بشكل مجمل، تشير النتائج إلى أن aFGF يفعل أكثر من مجرد دفع الخلايا إلى النمو. يبدو أنه ينقذ الخلايا الليفية المثقلة في جروح السكري من دائرة شيخوخة مدمرة، مقللاً الإجهاد التأكسدي ومعيداً ضبط مفتاح جزيئي أساسي بحيث تستطيع هذه الخلايا مجدداً المساعدة في إعادة بناء النسيج. مع أن العمل أُجري في فئران وخلايا مُزرَعَة، والجروح السكرية الحقيقية أعقد من النماذج المستخدمة هنا، فإن النتائج تضع aFGF كمرشح واعد لعلاجات مستقبلية. إذا تأكدت فوائد مماثلة في البشر، فقد تساعد معالجة مستهدفة بحذر بـ aFGF يوماً ما على شفاء القرائح السكرية المزمنة بشكل أسرع، مما يقلل الألم ومخاطر العدوى وفرص حدوث مضاعفات خطيرة.
الاستشهاد: Wang, X., Lu, M., Jia, S. et al. aFGF rescues high glucose-induced senescent fibroblasts and improves diabetic wound healing by regulating SIRT1/STAT3 pathway. Sci Rep 16, 7856 (2026). https://doi.org/10.1038/s41598-026-38480-0
الكلمات المفتاحية: التئام جروح السكري, شيخوخة الخلايا الليفية, الإجهاد التأكسدي, علاج بعوامل النمو, مسار SIRT1 STAT3