Clear Sky Science · ar
المسح المتكامل عبر مجموعات بيانات متعددة للتنبؤ بالتنبؤ وتحديد أهداف جينية للعلاج المناعي لدى مرضى سرطان الكبد الحجري
لماذا يهم هذا الأشخاص المصابين بسرطان الكبد
سرطان الكبد الحجري، الشكل الأكثر شيوعًا لسرطان الكبد الأولي، يتسبب بوفاة مئات الآلاف من الأشخاص سنويًا. كثير من المرضى الذين هم في نفس مرحلة المرض يستجيبون بشكل مختلف للعلاج، لا سيما للعلاجات المناعية الحديثة التي تهدف إلى إطلاق جهاز المناعة لدى الجسم. تطرح هذه الدراسة سؤالًا بسيطًا لكنه حاسم: هل يمكننا قراءة نشاط الجينات داخل الورم مثل بصمة لإصلاح من سيصاب بسوء، ومن سيستجيب للأدوية المناعية، وأي الجينات قد تكون أفضل أهداف علاجية جديدة؟
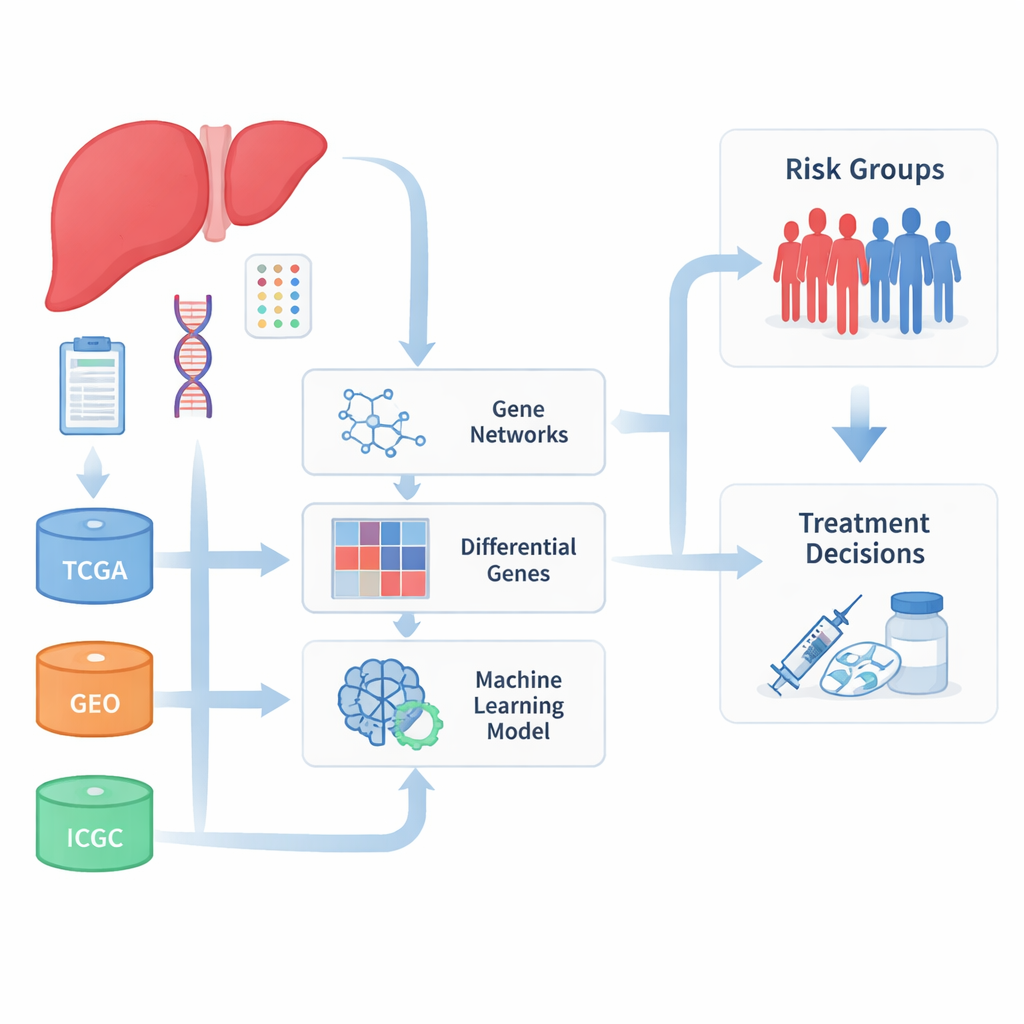
جمع مجموعات بيانات متعددة معًا
بدأ الباحثون بجمع مجموعات كبيرة من عينات سرطان الكبد من عدة قواعد بيانات دولية تحفظ بيانات نشاط الجينات ونتائج المتابعة السريرية. من خلال دمج بيانات من مشروع جينوم السرطان (The Cancer Genome Atlas)، والمشروع الدولي لجينوم السرطان (International Cancer Genome Consortium)، والعديد من دراسات مستودع تعبير الجينات (Gene Expression Omnibus)، جمعوا مجموعة مرضى أكبر وأكثر تنوعًا مما يمكن لأي مستشفى أو مشروع منفرد أن يوفره. ونظرًا لأن هذه المجموعات أُنتجت في مختبرات وأساليب مختلفة، قضى الفريق في البداية جهدًا كبيرًا لتصحيح الفروقات التقنية حتى تقودهم الإشارات البيولوجية الحقيقية وليس الضوضاء المخبرية.
اكتشاف أنماط جينية مرتبطة بالنتيجة
مع وجود البيانات المنقحة، بحث الفريق عن مجموعات من الجينات التي تميل إلى التشغيل والإيقاف معًا والتي كانت أيضًا مرتبطة بمدى تحسّن المرضى. باستخدام نهج شبيه بالشبكات، جمعوا آلاف الجينات في وحدات ثم ركزوا على الوحدات المرتبطة بقوة بسلوك الورم وبقاء المرضى. كما قارنوا الأنسجة الورمية بالأنسجة غير الورمية لاكتشاف الجينات التي كانت أكثر أو أقل نشاطًا بوضوح في السرطان. أدى التقاطع بين هذين المنظورين إلى مجموعة مكوَّنة من 93 جينًا كانت معدَّلة في سرطان الكبد ومرتبطة ارتباطًا وثيقًا بميزات المرض الرئيسية، كثير منها يشارك في كيفية تعامل الكبد مع الأدوية والمواد السامة.
بناء مقياس مخاطر بعشر جينات
لتحويل هذه القوائم الجينية إلى شيء قد يستخدمه الأطباء مستقبلًا، لجأ المؤلفون إلى التعلم الآلي. اختبروا أكثر من مئة مزيج من خوارزميات اختيار السمات وتنبؤ البقاء، وقيموها بناءً على مدى دقتها في تقسيم المرضى إلى مجموعات ذات نتائج أفضل وأسوأ عبر مجموعات تحقق مستقلة متعددة. من هذا البحث الواسع، استخلصوا بصمة مدمجة مكونة من عشر جينات شكّلت معًا مقياسًا للمخاطر. المرضى ذوو الدرجات العالية كان لديهم باستمرار فترة بقاء إجمالية وأخرى خالية من المرض وأخرى خالية من التقدم أقصر، سواء في المجموعات الرئيسية أو في مجموعات التحقق الخارجية. من بين هذه الجينات، برزت TYMS كمؤشر قوي لتوقع سيء، بينما ارتبطت APOL3 وFBXO2 بنتائج أكثر ملاءمة.
دلالات من البيئة المناعية المحيطة بالورم
لم تكتفِ الدراسة بالتنبؤ بل حاولت أن تشرح لماذا تهم هذه الجينات. باستخدام عدة أدوات حوسبية، قدّر الفريق أنواع الخلايا المناعية الموجودة في كل ورم ومدى ارتباط مقياس العشر جينات بتلك الخريطة المناعية. تميل الأورام عالية المخاطر إلى إظهار نمط مناعي وتغيرات جينية مرتبطة بمزيد من الطفرات وعلامات هروب مناعي، بما في ذلك روابط بجزيئات نقاط التفتيش المعروفة مثل PD-1 وCTLA-4. كما فحصوا ملفات الطفرات الفعلية ووجدوا أن الأورام عالية المخاطر تحتوي على تَغيُّرات متكررة أكثر في محفزات السرطان الكلاسيكية مثل TP53. أخيرًا، أكدت اختبارات الدم لدى المرضى والمتطوعين الأصحاء أن مستويات TYMS مرتفعة وFBXO2 منخفضة لدى المصابين بسرطان الكبد، مما يدعم فكرة أن هذه الجينات نشطة بيولوجيًا في المرض وليست مجرد نتائج إحصائية.
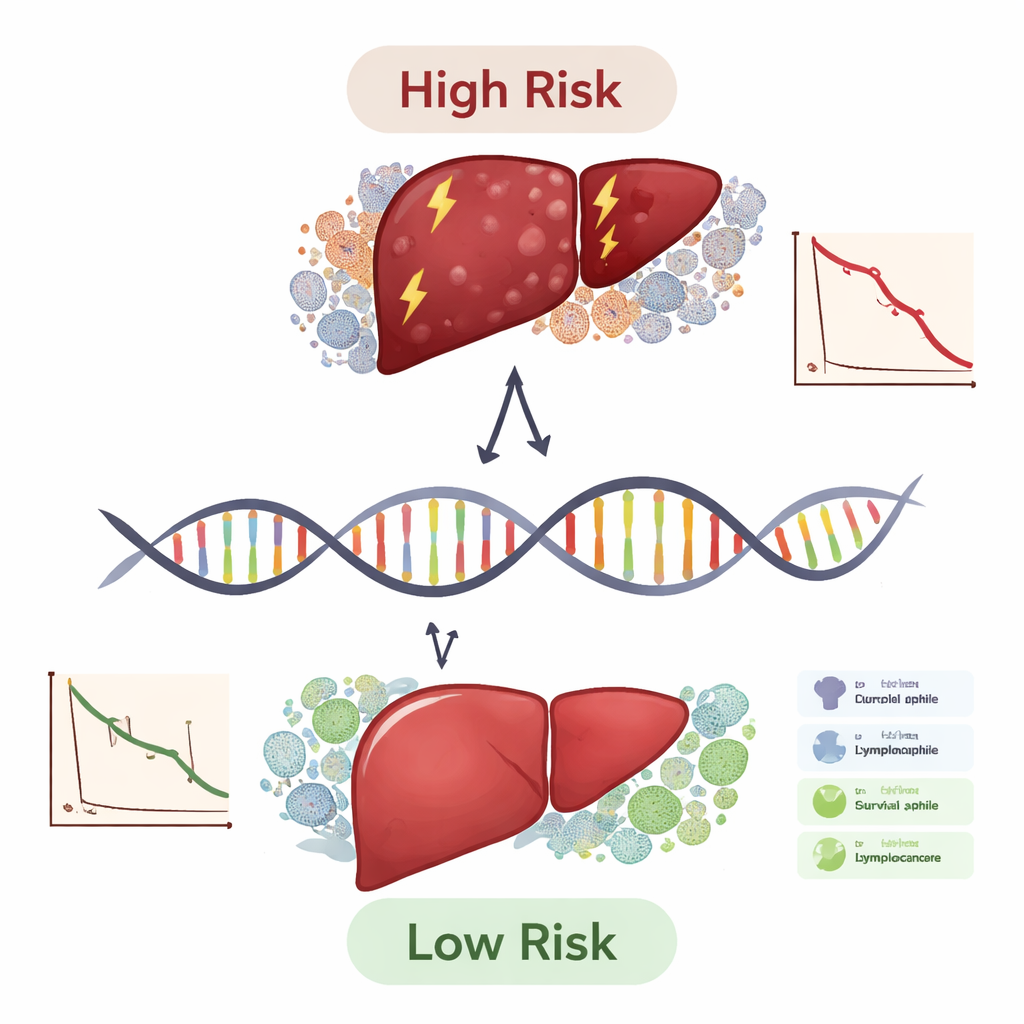
ماذا يعني هذا للمرضى والأطباء
من الناحية العملية، يقدم هذا العمل مخططًا لاستخدام لوحة صغيرة من الجينات لتصنيف مرضى سرطان الكبد إلى مجموعات مخاطرة وللتلميح إلى من قد يستفيد أكثر من العلاجات المعتمدة على المناعة. مقياس العشر جينات ليس اختبارًا جاهزًا للاستخدام السريري بعد، لكنه تفوق على أنظمة المرحلة التقليدية لوحدها وظل مفيدًا عبر مجموعات فرعية مختلفة من المرضى. تمامًا كما توجه لوحات الكوليسترول الوقاية من أمراض القلب، قد يساعد مثل هذه اللوحة الجينية في يوم من الأيام أطباء الأورام على اختيار علاجات أكثر عدوانية للمرضى عاليي المخاطر، وتجنب آثار جانبية غير لازمة لدى المرضى منخفضي المخاطر، وتوجيه مطوري الأدوية نحو أهداف جديدة مثل TYMS وAPOL3 وFBXO2. هناك حاجة إلى دراسات مستقبلية أكبر وتجارب مخبرية، لكن هذا التحليل المتكامل يشكل خطوة مهمة نحو رعاية أكثر تخصيصًا ومعتمدة على البيولوجيا لسرطان الكبد.
الاستشهاد: Zhou, L., Zhang, W., Liu, Z. et al. Integrated multi-dataset screening to predict prognosis and identify immunotherapy gene targets in hepatocellular carcinoma patients. Sci Rep 16, 7014 (2026). https://doi.org/10.1038/s41598-026-38424-8
الكلمات المفتاحية: سرطان الكبد الحجري, بصمة جينية, العلاج المناعي, التنبؤ بالمآل, البيئة المصاحبة للورم