Clear Sky Science · ar
إشارة CNOT2 / c-Myc / STAT3 متورطة بشكل حاسم في الاستماتة المحفزة بتثبيط التحلل السكري بواسطة بنزيل إيزوثيوسيانات في سرطان الكبد
مكوِّن محارب للسرطان على طبقك
بنزيل إيزوثيوسيانات، أو BITC اختصارًا، هو مركب طبيعي يوجد في خضراوات مألوفة مثل البروكلي والملفوف والكرنب. على الرغم من أن الأطباء كانوا يعلمون منذ زمن أن الأشخاص الذين يتناولون المزيد من هذه الأطعمة يميلون إلى معدلات أقل من السرطان، فإن كيفية إبطاء مركبات نباتية محددة للخلايا السرطانية أو قتلها لا تزال قيد الدراسة. تبحث هذه الدراسة في كيفية تأثير BITC على خلايا سرطان الكبد في المختبر وتكشف عن صلة مفاجئة بين طريقة استهلاك الخلايا السرطانية للسكر وكيف يتم دفعها نحو تدميرها الذاتي.
لماذا يحتاج سرطان الكبد إلى خيارات أفضل
سرطان الكبد هو أحد أكثر السرطانات فتكًا في العالم، والسرطان الكبدي الخلوي هو شكله الأكثر شيوعًا. حتى مع الجراحة والعلاج الكيميائي والأدوية المستهدفة، يعود العديد من الأورام أو تتوقف عن الاستجابة للعلاج. أحد الأسباب هو أن الخلايا السرطانية تعيد توصيل طرق استخدام الطاقة: بدلاً من الاعتماد بشكل رئيسي على الأكسجين في الميتوكوندريا، تحرق كميات كبيرة من السكر بسرعة في عملية غالبًا ما تسمى «تأثير واره burg». هذا الاستخدام المشوه للسكر يساعد الخلايا السرطانية على النمو بسرعة أكبر والمقاومة ضد الموت. إيجاد طرق آمنة لقطع هذا الإمداد الطاقي، خصوصًا باستخدام جزيئات مشتقة من الطعام، هو استراتيجية جذابة.
اختبار مركب نباتي على خلايا سرطان الكبد
قام الباحثون بمعاملة سطرين من خلايا سرطان الكبد البشري، SK-Hep1 وHuh7، بجرعات متزايدة من BITC. مع ازدياد الجرعة، نجت خلايا أقل، ما أظهر أن BITC سام لخلايا سرطان الكبد تحت هذه الظروف. عندما نظروا عن كثب إلى ما يحدث داخل الخلايا، رأوا علامات كلاسيكية للموت المبرمج للخلايا، أو الاستماتة. البروتينات الرئيسية التي توجد عادة في شكل «غير نشط» قبل أن تُقص أثناء الاستماتة، مثل PARP وكاسبيز-3، انخفضت في أشكالها السليمة أو «المهيئة». اختبارات cytometry الانسيابية أظهرت أيضًا مزيدًا من الخلايا في كسور تحت طور G1 من دورة الخلية ومزيدًا من الخلايا الموجبة لـ Annexin V، وكلاهما دلالة على أن الخلايا السرطانية كانت تخضع للاستمناء النشط بدلاً من أن تكون متضررة ببساطة.
إغلاق شغف السرطان بالسكر
ثم استكشف الفريق ما إذا كان BITC يؤثر على تأثير واره burg. قاسوا البروتينات التي تساعد الخلايا السرطانية على التهام السكر وتحويله إلى طاقة ولاكتات — وتحديدًا HK2 وPKM2 وLDH. خفض علاج BITC مستويات الثلاثة في كلا سطري خلايا سرطان الكبد وتقليل كمية اللاكتات التي أطلقتها الخلايا وكمية الجلوكوز التي استهلكته من الوسط الغذائي. بمعنى آخر، جعل BITC خلايا سرطان الكبد أقل قدرة على تشغيل آلتها عالية السرعة لحرق السكر. عندما أضاف العلماء البيروفات، وهو منتج لاحق لتفكيك السكر يمكن أن يغذي أيض الخلية، تم عكس العديد من آثار BITC: استعادت الخلايا مستويات أعلى من PARP وكاسبيز-3 وإنزيمات اللاهضم السكري. هذه الإنعاشات اقترحت أن التدخل في معالجة السكر هو جزء أساسي من كيفية دفع BITC الخلايا نحو الموت.
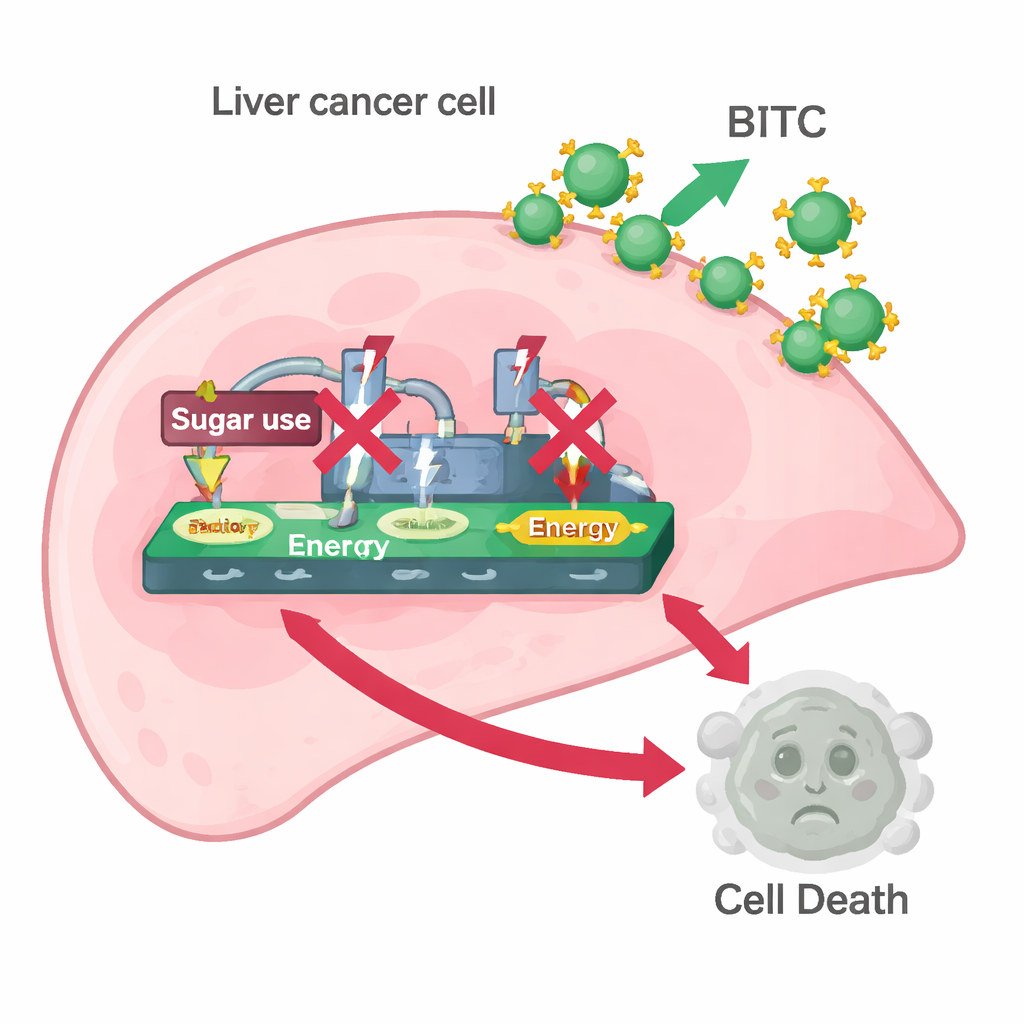
فك مفاتيح التحكم داخل الخلية
لفهم طبقات التحكم الأعمق، ركز الباحثون على ثلاثي الإشارة: CNOT2 وc-Myc وSTAT3. هذه البروتينات تساعد في دفع النمو والبقاء وإعادة توصيل الأيض في العديد من الأورام. أظهرت بيانات من مرضى سرطان الكبد أن CNOT2 يميل لأن يكون أعلى لدى الأشخاص ذوي النتائج الأسوأ. في المختبر، خفض علاج BITC الشكل النشط المفروز من STAT3 ومنشطه الأعلى JAK1، والبروتين المحفز للنمو c-Myc، وCNOT2 نفسه. استخدام أدوات جينية لتقليل مستويات CNOT2 أو STAT3 جعل تأثير القتل لـ BITC أقوى، حيث خفض أكثر من ذلك PARP وكاسبيز-3. كشفت تجارب ربط البروتينات أن BITC أيضًا اضطراب الشراكات الفيزيائية بين CNOT2 وSTAT3 وبين CNOT2 وc-Myc. عندما زاد الباحثون من CNOT2 أو c-Myc صناعيًا، فقد BITC جزءًا كبيرًا من قدرته على إيقاف إنزيمات التحلل السكري وتحفيز الاستماتة، مما يبرز أن محور الإشارة هذا يعمل كمفتاح رئيسي يربط بين استقلاب السكر والبقاء.
ماذا قد يعني هذا للعلاجات المستقبلية
معًا، ترسم النتائج صورة متماسكة: يهاجم BITC خلايا سرطان الكبد عن طريق قطع خط الوقود القائم على السكر المفضل لديهم وتقليب مفاتيح موت الخلايا التي تعتمد على محور CNOT2/c-Myc/STAT3. من خلال حجب كل من إشارات النمو واستخدام السكر، يدفع BITC الخلايا السرطانية إلى ما بعد نقطة الانقلاب الأيضية نحو الاستماتة. هذه النتائج مستمدة من تجارب زراعة الخلايا، وليس من المرضى، ودُرِست فقط نوعان من خلايا سرطان الكبد، لذا هناك حاجة إلى المزيد من العمل في النماذج الحيوانية والبشرية. ومع ذلك، تعزز هذه الدراسة فكرة أن مركبات معينة من الخضراوات اليومية يمكن تحسينها أو دمجها مع علاجات أخرى لتجويع أورام الكبد بشكل أكثر دقة مع تشجيعها على التدمير الذاتي.
الاستشهاد: Koh, W., Park, SY., Kim, B. et al. CNOT2 /c-Myc/STAT3 signaling is critically involved in glycolysis mediated apoptosis of benzyl isothiocyanate in hepatocellular carcinoma. Sci Rep 16, 7000 (2026). https://doi.org/10.1038/s41598-026-38416-8
الكلمات المفتاحية: سرطان الكبد, بنزيل إيزوثيوسيانات, تمثيل غذائي للسرطان, الاستماتة, خضراوات الصليبيات