Clear Sky Science · ar
نموذج تنبؤي قائم على التعلم الآلي لجينات الصلابة وتكوين الأوعية للتنبؤ بالتنبؤ والتسلل المناعي لدى مرضى سرطان الكبد
لماذا يهم هذا البحث مرضى سرطان الكبد
سرطان الخلايا الكبدية، هو الشكل الأكثر شيوعًا لسرطان الكبد، وغالبًا ما يعود أو ينتشر حتى بعد العلاج. يستكشف هذا البحث أسباب ذلك وكيف يمكن للأطباء التنبؤ بشكل أفضل أي المرضى هم الأكثر عرضة للخطر. من خلال دمج مجموعات بيانات جينية كبيرة مع تقنيات التعلم الآلي الحديثة، بنى الباحثون أداة تربط بين صفتين قويتين في السرطان — «الصلابة» (خلايا تتصرف مثل بذور عنيدة) وتكوّن أوعية دموية جديدة — وفرص بقاء المرضى واستجابتهم المحتملة للعلاجات المناعية.
خلايا «البذور» السرطانية والأوعية الجديدة
تحتوي العديد من الأورام على مجموعة صغيرة من الخلايا التي تتصرف كبذور. هذه الخلايا الجذعية السرطانية قادرة على تجديد نفسها، ومقاومة العلاج، وإعادة إيقاظ الورم بعد الجراحة أو العلاج الكيميائي. في الوقت نفسه، تحتاج الأورام لبناء أوعية دموية جديدة لجلب الأكسجين والمواد المغذية كي تنمو وتنتشر. تظهر الأعمال الحديثة أن هذين العمليين مرتبطان: الخلايا الشبيهة بالجلدة تطلق إشارات تشجع نمو الأوعية، في حين أن البيئة الغنية بالأوعية تساعد تلك الخلايا «البذرية» على البقاء. فهم هذه الشراكة واستهدافها معًا مهم بشكل خاص في سرطان الكبد، الذي يتميز بوفرة الأوعية وارتفاع معدلات الانتكاس.
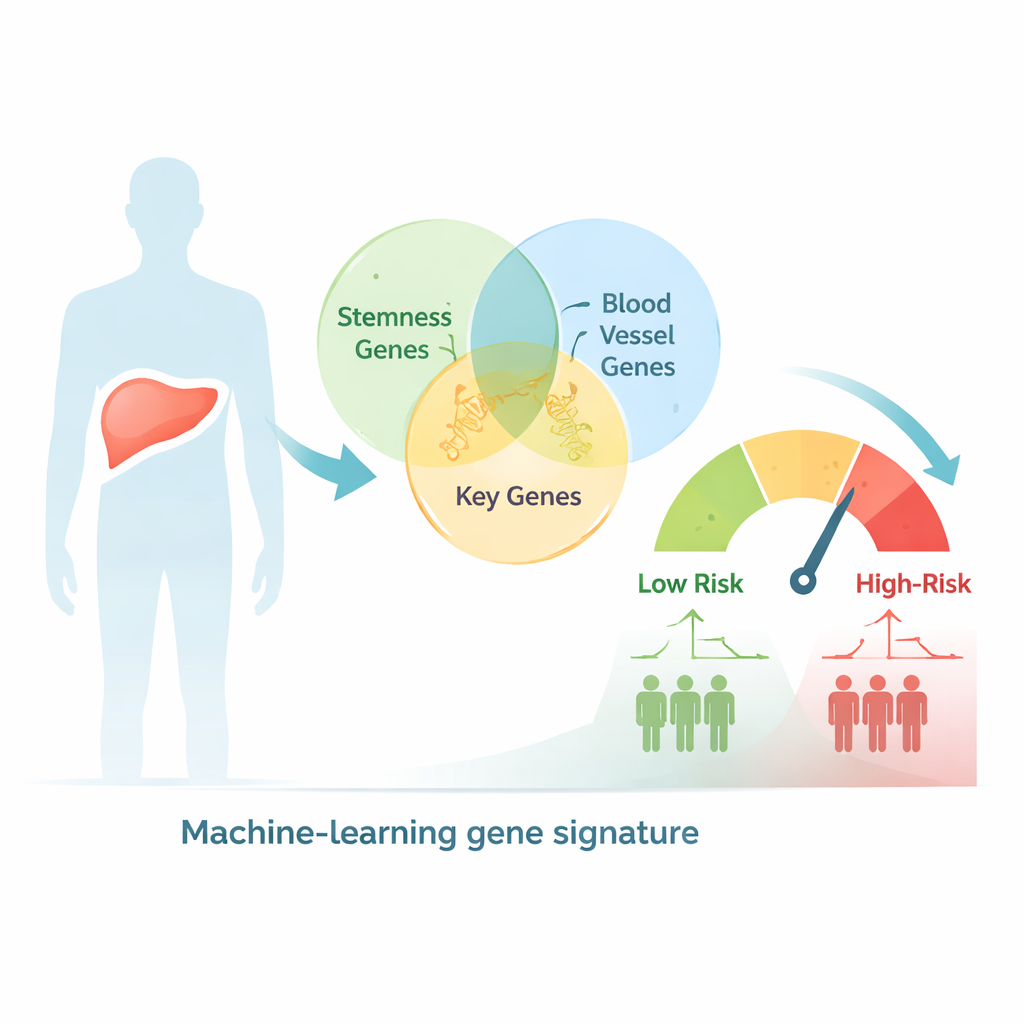
استخدام البيانات الكبيرة لفرز المرضى حسب الخطر
بدأ الباحثون بالبحث في قاعدة بيانات جينية بشرية كبيرة عن جينات مرتبطة بالسلوك الشبيه بالصلابة وبتكوّن الأوعية، فتوصلوا إلى أكثر من 2600 مرشح متداخل. ثم فحصوا عينات سرطان الكبد من مئات المرضى الذين سُجلت نشاطات جينات أورامهم ونتائجهم السريرية في قواعد بيانات عامة للسرطان. باستخدام اختبارات إحصائية وأساليب تجميع العنقود، صنفوا المرضى إلى نوعين جينيين أظهرا فروقًا واضحة في المرحلة، وحجم الورم، والبقاء على قيد الحياة، ما يشير إلى أن الإشارات المشتركة المرتبطة بالصلابة والأوعية تعكس بيولوجيا مهمة في هذا المرض.
بناء مقياس خطر مكوّن من تسعة جينات
من هذه المجموعة الكبيرة من الجينات، استخدم الفريق نهجًا قائمًا على التعلم الآلي للحد إلى تسع جينات رئيسية فقط التي تنبأت بشكل أفضل بمقدار طول عمر المرضى. استُخدمت هذه التسع جينات لحساب درجة مخاطرة لكل شخص. كان لدى المرضى الذين أظهرت أورامهم درجة عالية وقت بقاء إجمالي أقصر بشكل ملحوظ، سواء في مجموعة البيانات الأصلية أو في مجموعة مستقلة من مرضى سرطان الكبد استخدمت للتحقق. كانت دقة النموذج منافسة أو أفضل من العديد من الأدوات الموجودة، وعند دمج الدرجة مع معلومات سريرية بسيطة مثل مرحلة الورم في رسم تخطيطي يسمى نموجرام، تحسن التنبؤ بالبقاء عند 1 و3 و5 سنوات بشكل أكبر.
روابط مع الجهاز المناعي واستجابة العلاج
سأل الفريق أيضًا ماذا تكشف درجة التسع جينات عن بيئة الورم المناعية. كانت الأورام منخفضة المخاطرة تميل لأن تكون أكثر «التهابًا»، مع مستويات أعلى من خلايا مناعية متعددة وإشارات أقوى لمسارات الهجوم. في المقابل، أظهرت الأورام عالية المخاطرة أنماطًا متسقة مع التملص المناعي ومعدلات طفرة أعلى في جينات مهمة مثل TP53. باستخدام أدوات حاسوبية معتمدة تقدر كيف قد تستجيب الأورام لأدوية المناعة الحديثة، اقترح البحث أن المرضى منخفضي المخاطرة قد يستجيبون بشكل أفضل لمانعات نقاط التفتيش المناعية مقارنة بالمرضى عالِي المخاطرة. وبينما تحتاج هذه التنبؤات إلى اختبار في بيئات علاجية حقيقية، فإنها تشير إلى وسيلة عملية لتحديد المرضى الذين قد يستفيدون أكثر من هذه الأدوية.
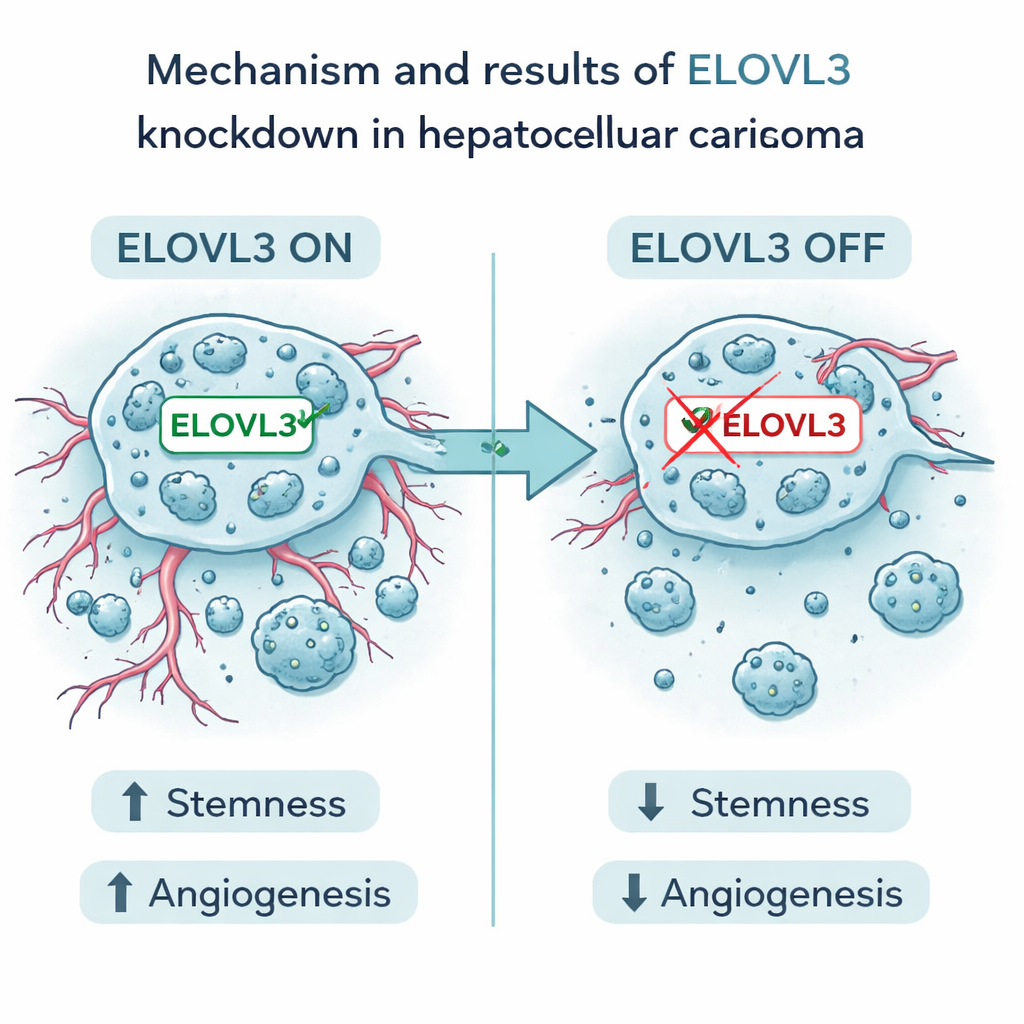
تركيز على هدف واعد واحد
من بين التسع جينات، برزت جينة واحدة تُدعى ELOVL3. ارتبطت المستويات العالية لهذه الجينة بسوء البقاء. في تجارب مخبرية، خفض الباحثون تعبير ELOVL3 في خلايا سرطان الكبد البشرية. جعل ذلك الخلايا أقل قدرة على تشكيل تجمعات شبيهة بالصلابة وخفض مستويات علامات الصلابة المعروفة جيدًا. كما قلل إنتاج وإطلاق عاملين رئيسيين محفزين لتكوين الأوعية، VEGFA وFGF2. نما السرطان وتوغّل وتحرك أقل، وفي نماذج فأرية، كانت الأورام التي حدث فيها تقليل ELOVL3 أصغر وأظهرت ميزات أقل عدوانية. تدعم هذه النتائج فكرة أن ELOVL3 يساهم في تغذية سلوك الخلايا «البذرية» في سرطان الكبد وقدرتها على بناء أوعية داعمة.
ما الذي قد يعنيه هذا للرعاية المستقبلية
بعبارات بسيطة، يقدم هذا العمل رسالتين رئيسيتين. أولًا، يمكن لمقياس بسيط مكوّن من تسع جينات المستخلص من عينات الورم أن يصنف مرضى سرطان الكبد إلى مجموعات عالية ومنخفضة المخاطرة ويعطي تلميحًا عن كيفية استجابتهم للعلاجات المناعية. ثانيًا، تبدو إحدى الجينات في هذا المقياس، ELOVL3، وكأنها تقع عند مفترق طرق بين قدرة السرطان على التجدد وقدرته على تكوين أوعية جديدة، مما يجعلها هدفًا دوائيًا واعدًا للمستقبل. على الرغم من أن النموذج والهدف يحتاجان إلى تأكيد في تجارب سريرية مستقبلية، فإنهما يفتحان الباب لرعاية أكثر تخصيصًا لسرطان الكبد ولإستراتيجيات تركيبية تمنع كلًا من «الخلايا البذرية» للسرطان ومصدر تغذيتها الوعائي.
الاستشهاد: Cheng, F., Shi, Y., Gao, X. et al. Machine learning-based prognostic model of stemness and angiogenesis-related genes for predicting prognosis and immune infiltration in patients with HCC. Sci Rep 16, 7271 (2026). https://doi.org/10.1038/s41598-026-38379-w
الكلمات المفتاحية: سرطان الخلايا الكبدية, خلايا جذعية سرطانية, تكوّن الأوعية الدموية, توقيع جيني تنبؤي, ELOVL3