Clear Sky Science · ar
تثبيط PERK يخفف موت الخلايا متعدد البرامج عبر تفعيل Nrf2/HO-1 في اعتلال الشبكية السكري مع بروتيوميك متكامل والتحقق الوظيفي في خلايا بطانة الشبكية البشرية
لماذا حماية البصر لدى مرضى السكري مهمة
بالنسبة لملايين الأشخاص الذين يعيشون مع مرض السكري، فإن أحد أكثر المضاعفات مخافة هو الفقدان التدريجي للبصر المعروف باعتلال الشبكية السكري. يحدث هذا الضرر لأنسجة استقبال الضوء في الجزء الخلفي من العين غالبًا بصمت، قبل ظهور الأعراض بوقت طويل. البحث الذي تقف وراء هذه المقالة يتقصّى ما الذي يقتل فعلاً خلايا الأوعية الدموية الصغيرة التي تحافظ على صحة الشبكية—ويجرب طريقة جديدة لحمايتها. من خلال فهم وتهدئة "استجابات الإجهاد" الخلوية التي يسببها ارتفاع سكر الدم، يأمل الباحثون في إبطاء أو حتى منع العمى لدى المصابين بالسكري.
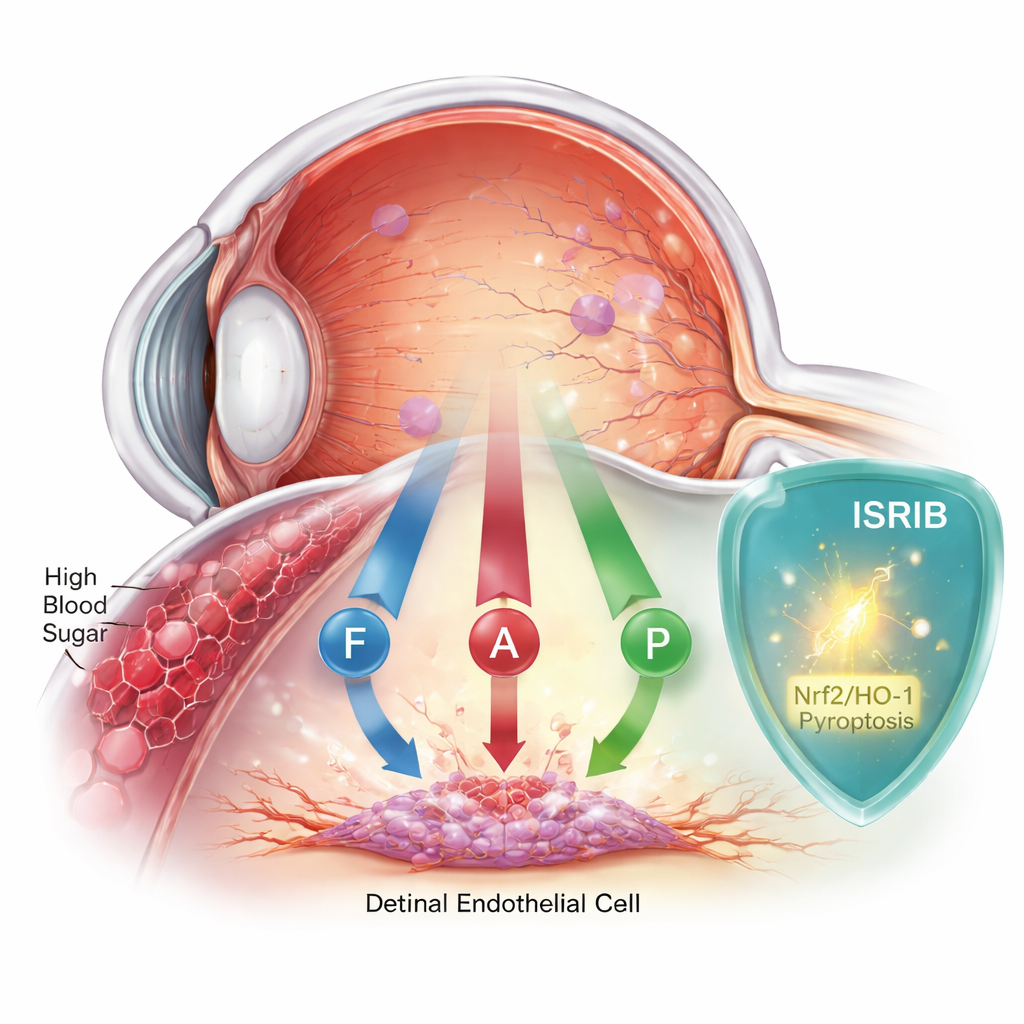
عندما يجهد سكر الدم العين بهدوء
يبدأ اعتلال الشبكية السكري عندما يضر ارتفاع سكر الدم البطانة الرقيقة لأوعية الشبكية الدموية. تشكل هذه الخلايا حاجزًا يبقي الشبكية مغذّاة ومحمية. لسنوات، ظنّ العلماء أن شكلًا واحدًا من موت الخلايا، يُدعى الاستماتة (apoptosis)، هو المسؤول في المقام الأول. لكن الأدلة المتزايدة تشير إلى أن القصة أكثر تعقيدًا. ركز هذا الفريق على خلايا بطانة الأوعية الدموية الشبكية البشرية المزروعة في المختبر وعرضها لمستويات سكر مماثلة لتلك الموجودة في السكري غير المسيطر عليه جيدًا، ثم راقب كيف استجابت الخلايا خلال يومين.
ثلاث طرق يمكن أن تموت بها الخلايا في آن واحد
باستخدام تقنية قوية لقياس البروتينات تُسمى البروتيوميكس، وجد الباحثون أن المستويات العالية من السكر عطّلت مئات البروتينات، خاصة تلك المشاركة في استجابات الإجهاد والتمثيل الغذائي والتعامل مع الحديد. أظهرت الاختبارات اللاحقة أن الخلايا لم تكن تموت بطريقة واحدة فحسب، بل ثلاث طرق: الموت المبرمج الكلاسيكي (الاستماتة)، وشكل ملتهب مرتبط بالنار (البيروبتوزيس)، وشكل أحدث مدفوع بالحديد يسمى الفيروبتوزيس. ارتفعت علامات الضرر التأكسدي، وفرط الحديد، ونضوب مضادات الأكسدة، بينما انخفضت الإنزيمات الواقية. معًا، رسمت هذه التغيرات صورة لخلايا غارقة في الإجهاد والالتهاب وتراكم جزيئات تفاعلية سامة.
مفتاح ضغط الإجهاد في قلب المشكلة
ثم ركز الفريق على جهاز استشعار إجهاد رئيسي داخل الخلايا يُدعى PERK، والذي يوجد على غشاء الشبكة الإندوبلازمية، البنية التي تساعد على طي ومعالجة البروتينات. تحت ظروف السكر المرتفع، أصبح PERK مفرط النشاط، يعمل مثل إنذار طوارئ عالق يصرخ باستمرار. بدا أن هذا يغذي جميع برامج الموت الثلاثة. في الوقت نفسه، ضعفت آلية دفاع طبيعية عادةً ما تساعد الخلايا على التعامل مع الضرر التأكسدي—مسار Nrf2/HO-1 المضاد للأكسدة. ببساطة، كانت إشارات الخطر مرتفعة بينما كانت مطافئ الحريق الداخلية خاملة.
خفض الإجهاد، وزيادة الحماية
لاختبار ما إذا كان بإمكانهم كسر هذه الدائرة المدمرة، عالج الباحثون الخلايا المعرضة للسكر المرتفع بمركب صغير يُدعى ISRIB، والذي يخفف فعليًا إشارة إجهاد PERK. كانت النتائج لافتة. حسّن ISRIB بقاء الخلايا، وخفّض علامات الضرر المدفوع بالحديد والإجهاد التأكسدي، وقلّل المؤشرات الكيميائية لكل من الاستماتة والبيروبتوزيس. في الوقت نفسه، عزز مسار الدفاع Nrf2/HO-1، مما ساعد الخلايا على استعادة قدرتها المضادة للأكسدة. دواء منفصل يوقف الفيروبتوزيس بشكل محدد ساعد أيضًا، لكن ISRIB برز لأنه هدّأ جميع مسارات الموت الثلاثة دفعة واحدة بدلاً من واحد فقط.
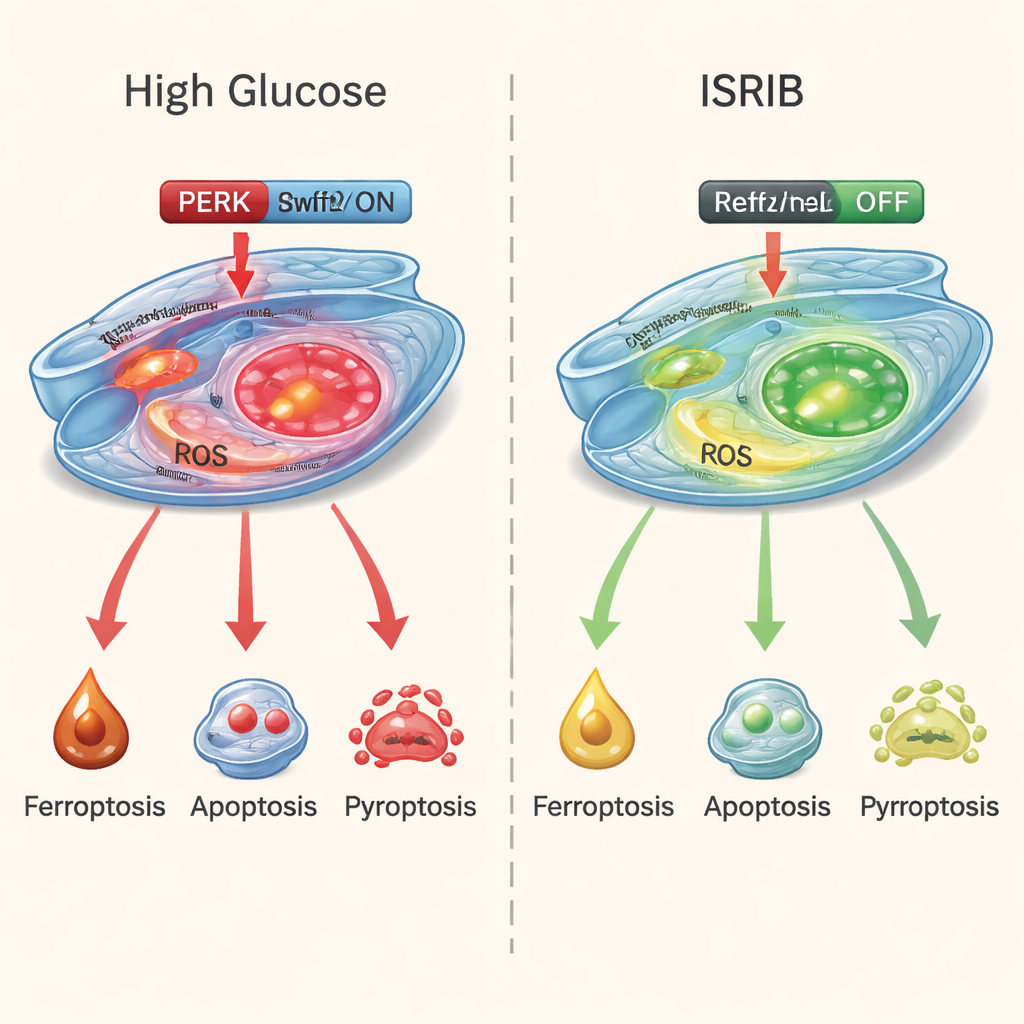
ماذا قد يعني هذا للأشخاص المصابين بالسكري
تشير هذه الدراسة إلى أن الضرر المبكر في اعتلال الشبكية السكري لا تسببه "جهة شريرة" واحدة، بل تقاطع لعدة برامج موت تعزز بعضها البعض يقودها الإجهاد الخلوي المزمن. من خلال خفض مفتاح إجهاد PERK وإعادة تنشيط أنظمة الحماية الذاتية للخلايا، قد توفر أدوية مثل ISRIB طريقًا أكثر توحيدًا للحفاظ على بقاء أوعية الشبكية الدموية. وبينما أجريت هذه التجارب في خلايا وليس بعد في المرضى، فإنها تشير إلى علاجات مستقبلية تستهدف استجابات الإجهاد داخل العين—مما قد يضيف طبقة جديدة من الحماية إلى جانب ضبط سكر الدم والحقن العينية الحالية للمساعدة في الحفاظ على البصر لدى المصابين بالسكري.
الاستشهاد: Xie, L., Zhang, X., Tian, M. et al. PERK inhibition attenuates multi-program cell death through Nrf2/HO-1 activation in diabetic retinopathy with integrated proteomics and functional validation in HRECs. Sci Rep 16, 7225 (2026). https://doi.org/10.1038/s41598-026-38213-3
الكلمات المفتاحية: اعتلال الشبكية السكري, موت خلايا الشبكية, الإجهاد التأكسدي, مسار PERK, Nrf2 HO-1