Clear Sky Science · ar
تحديد والتحقق من توقيع جيني جديد مرتبط بالفيروبتوزيس والمرتبط بالتنكس الشبكي الموروث في فئران Rd10
لماذا تهمنا خلايا العين المحتضرة جميعًا
التهاب الشبكية الصباغي هو مجموعة من أمراض العين الوراثية التي تسرق البصر تدريجيًا، غالبًا ما تبدأ بعمى الليل وتنتهي بفقدان الرؤية التام. لا يوجد علاج شافٍ، والعلاجات الجينية الحالية تفيد جزءًا صغيرًا فقط من المرضى. تبحث هذه الدراسة من منظور مختلف: شكل خاص من موت الخلايا يُسمى الفيروبتوزيس، المدفوع بالحديد والأضرار التأكسدية، للكشف عن أهداف جينية جديدة قد تحمي يومًا ما خلايا مستقبلات الضوء في الشبكية — بغض النظر عن الطفرة التي وُلِد بها الشخص.
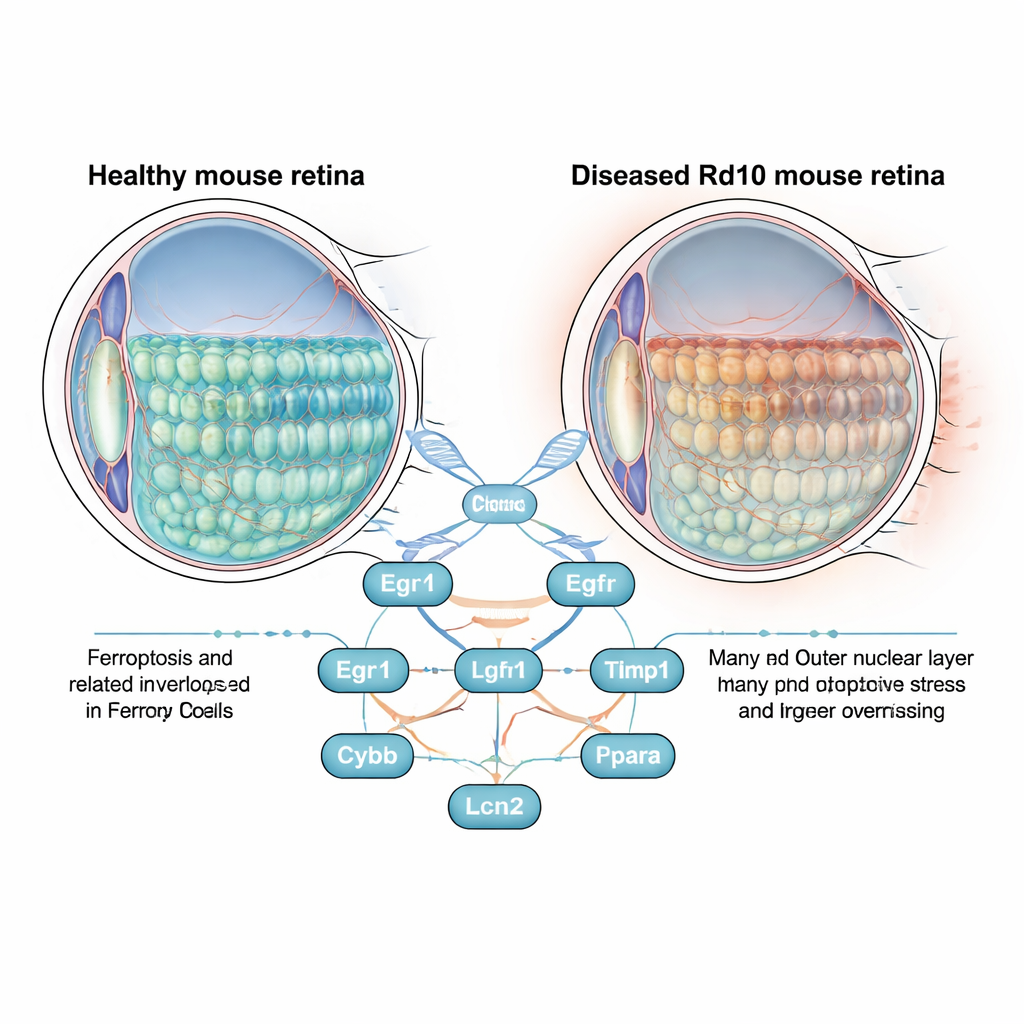
نظرة أوضح على مرض يسبب العمى
الشبكية هي طبقة رقيقة من الأنسجة في خلف العين تحتوي على خلايا قضيبية ومخروطية تستقبل الضوء وتحوله إلى إشارات كهربائية. في التهاب الشبكية الصباغي تموت هذه الخلايا تدريجيًا، محرومة الناس أولًا من الرؤية في الظلام والرؤية الجانبية ثم الرؤية المركزية لاحقًا. يدرس العلماء غالبًا هذه العملية في فئران Rd10 التي تحمل طفرة تحاكي المرض البشري عن كثب. بدلاً من التركيز فقط على الجين المعيب، طرح المؤلفون سؤالًا أوسع: مع تدهور الشبكية، أي الجينات المرتبطة بالفيروبتوزيس تُفعَّل أو تُكبح، وهل قد تكون هذه الجينات هي سبب فقدان الخلايا؟
العثور على الجينات الرئيسية في بحر من البيانات
استخرج الفريق مجموعات بيانات كبيرة عامة لتعبير الجينات من شبكيات سليمة وفئران Rd10، مما يعادل أخذ «لقطة» شاملة للجينات التي كانت أكثر أو أقل نشاطًا. وجدوا أكثر من 2000 جين تغيرت، ثم قارنوا هذه القائمة مع مجموعة مُنقّحة من الجينات المرتبطة بالفيروبتوزيس. ضيق هذا المسار إلى 37 مرشحًا مرتبطًا بموت الخلايا المؤكسد والمدفوع بالحديد. أظهرت التحليلات الحاسوبية أن هذه الجينات تتجمع في عمليات مثل الاستجابة للإجهاد التأكسدي، تنظيم موت الخلايا العصبية، ومسارات أيض الدهون — سمات مميزة للفيروبتوزيس واستجابات الضغط المعروفة في الأعصاب المتدهورة.
ثمانية جينات تبرز بين الباقي
لتحديد اللاعبين الأكثر تأثيرًا، بنى الباحثون شبكة تداخل البروتينات وطبقوا عدة خوارزميات ترتيب. برزت ثمانية جينات "محورية": Egr1، Cd44، Egfr، Tlr4، Timp1، Cybb، Lcn2، وPpara. كانت سبعة منها أكثر نشاطًا في الشبكيات المريضة، بينما كان Ppara أقل نشاطًا. أكدت المجموعة هذه الأنماط في مجموعة بيانات مستقلة ثم فحصت بشكل أدق مواقع ظهور الجينات الأعلى في العين. باستخدام صبغات فلورية وتسلسل RNA خلية بخلية، أظهروا أن Egr1 يزداد بقوة في الخلايا القضيبية والمخروطية، بينما يرتفع Cd44 بشكل لافت في خلايا مولر الداعمة التي تمتد عبر الشبكية. هذا يشير إلى أن الخلايا المستقبلة للضوء المتوترة وخلايا الدعم قد تتعاون — وربما تضر — عبر مسارات مرتبطة بالفيروبتوزيس.
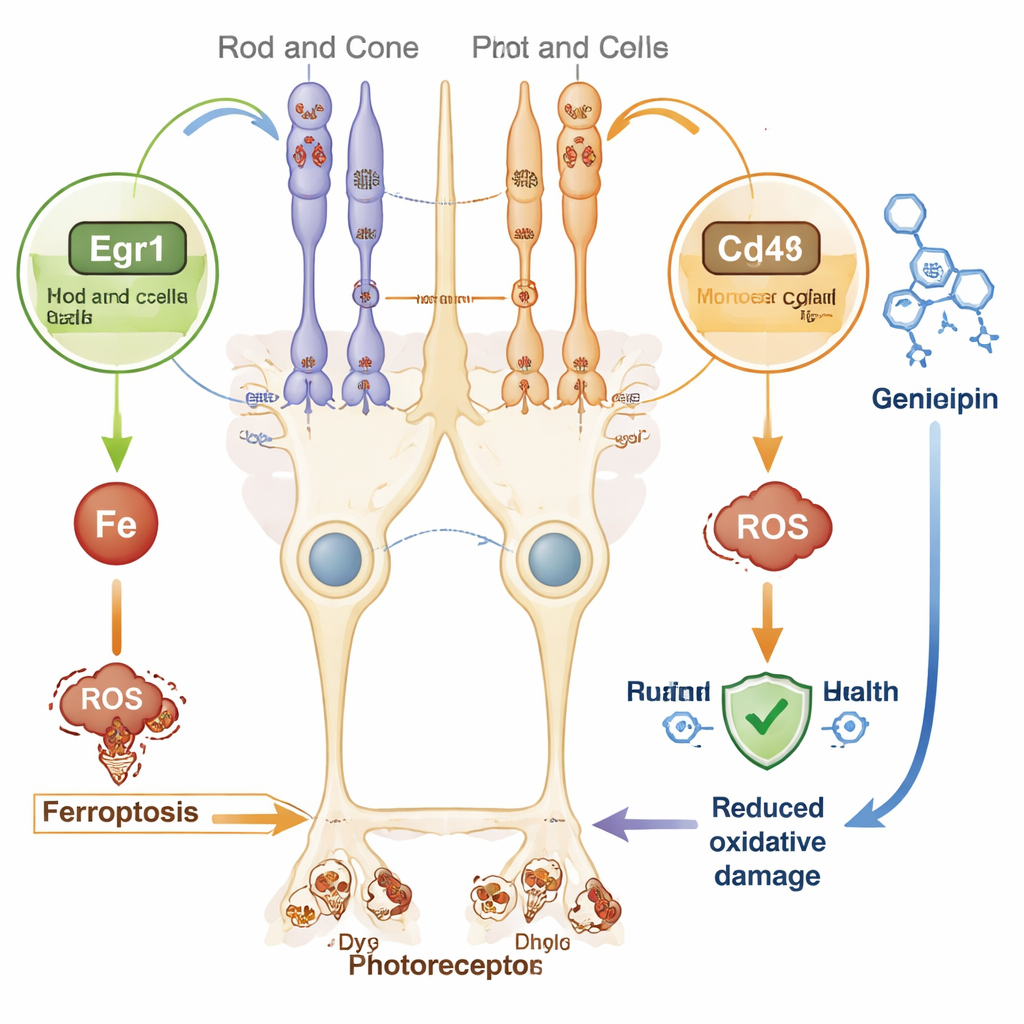
ما يعنيه هذا للعلاجات المستقبلية
نظرًا لأن العلاج الجيني المصمم لكل جين مُعيب معقد ومكلف، تبدو الاستراتيجيات واسعة المدى جذابة. يلمّح التوقيع الجيني المكتشف حديثًا إلى عدة مسارات من هذا النوع. على سبيل المثال، Egr1 هو مفتاح سريع الاستجابة يتفاعل مع الإجهاد التأكسدي ويمكن أن يعزز الفيروبتوزيس في أعضاء أخرى. أما Cd44، وهو جزيء سطحي في خلايا مولر، فقد أظهر في أنسجة مختلفة أنه يفاقم حمولة الحديد وموت الخلايا. في الوقت نفسه، قد يجعل انخفاض Ppara، المنظم لأيض الدهون واستهلاك الطاقة، خلايا الشبكية أكثر عرضة للضرر. من خلال استهداف هذه المسارات المشتركة للاستجابة للضغط، قد يكون من الممكن إبطاء تنكس الشبكية عبر أشكال وراثية عديدة من التهاب الشبكية الصباغي.
أدوية قد تساعد في حماية البصر
باستخدام قاعدة بيانات تفاعلات دواء–جين، بحث المؤلفون عن مركبات يمكن أن تؤثر على Egr1 أو Cd44. ظهرت عدة جزيئات موجودة بالفعل، بما في ذلك المركب الطبيعي جينيبين الذي أظهر تأثيرات حماية في نماذج مرض باركنسون، تنكس الأعصاب، واعتلال الشبكية السكري عبر تقليل الإجهاد التأكسدي والالتهاب. وعلى الرغم من أن أيًا من هذه الأدوية المرشحة لم يُختبر بعد في نموذج الفأر هذا لالتهاب الشبكية الصباغي، فإنها توفر نقاط انطلاق واعدة للدراسات المخبرية والحيوانية المستقبلية التي تهدف إلى حماية مستقبلات الضوء من الفيروبتوزيس.
الرسالة الأساسية لغير المتخصصين
تُظهر هذه الدراسة أن موت الخلايا المؤكسد المدفوع بالحديد مرتبط ارتباطًا وثيقًا بتغيرات نشاط الجينات التي تُرى في نموذج كلاسيكي للعمى الوراثي. من خلال تمييز ثمانية جينات رئيسية، وخاصة Egr1 المستجيب للإجهاد في مستقبلات الضوء وCd44 في خلايا مولر، ترسم الدراسة أرضية جديدة لعلاجات محتملة لا تعتمد على إصلاح جين واحد مُطفَل. إذا أكدت التجارب المستقبلية أن تهدئة الفيروبتوزيس عبر هذه الأهداف يمكن أن يحافظ على خلايا الشبكية حية، فقد يفتح ذلك الباب لعلاجات تفيد مجموعة واسعة من المرضى المعرضين لفقدان البصر التقدمي.
الاستشهاد: Qiu, X., Fu, XW., Lei, XL. et al. Identification and validation of a novel ferroptosis-related gene signature associated with inherited retinal degeneration in Rd10 mice. Sci Rep 16, 6992 (2026). https://doi.org/10.1038/s41598-026-38193-4
الكلمات المفتاحية: التهاب الشبكية الصباغي, الفيروبتوزيس, الخلايا المستقبلة للضوء, تنكس الشبكية, Egr1 Cd44