Clear Sky Science · ar
البلازما الغنية بالصفائح الدموية تعزز تعافي الخلايا من سمية النيكوتين عبر تعديل الالتهام الذاتي
لماذا يهم هذا لثتك
إذا كنت تدخن أو تستخدم منتجات تحتوي على النيكوتين، فإن لثتك تقاتل معركة غير مرئية كل يوم. النيكوتين لا يقتصر تأثيره على تلطيخ الأسنان أو رائحة الفم الكريهة؛ بل يضعف بهدوء الخلايا نفسها التي تحافظ على صلابة اللثة وقدرتها على التعافي. طرحت هذه الدراسة سؤالاً متفائلاً: هل يمكن للبلازما الغنية بالصفائح الدموية — منتج مشتق من الدم يُستخدم بالفعل لتسريع الشفاء في الجراحة وطب الرياضة — أن يساعد خلايا اللثة على التعافي من أضرار النيكوتين والمقاومة بشكل أفضل للأمراض طويلة الأمد؟
كيف يضر التدخين الفم بهدوء
التهاب اللثة المزمن هو مرض يسبب تدهور الأنسجة والعظم الداعمين للأسنان ببطء. عادةً ما تحافظ خلايا اللثة والجهاز المناعي على توازن البكتيريا الضارة وتصلح التلف اليومي. يخل النيكوتين بهذا التوازن بعدة طرق. يجبر الأوعية الدموية على الانقباض، مما يقلل الأكسجين والمغذيات. يجهد خلايا اللثة فتضعف نموها، وتشيخ أسرع، وتموت بسهولة أكبر. كما يثير الالتهاب ويحفز الخلايا المصممة على امتصاص العظام مما يرخِ جنب الأسنان. ركز المؤلفون على الأرومات الليفية اللثوية — الخلايا الرئيسية التي تبني وتعيد تشكيل نسيج اللثة — لمعرفة كيف يدفعها النيكوتين تحديداً نحو المرض.
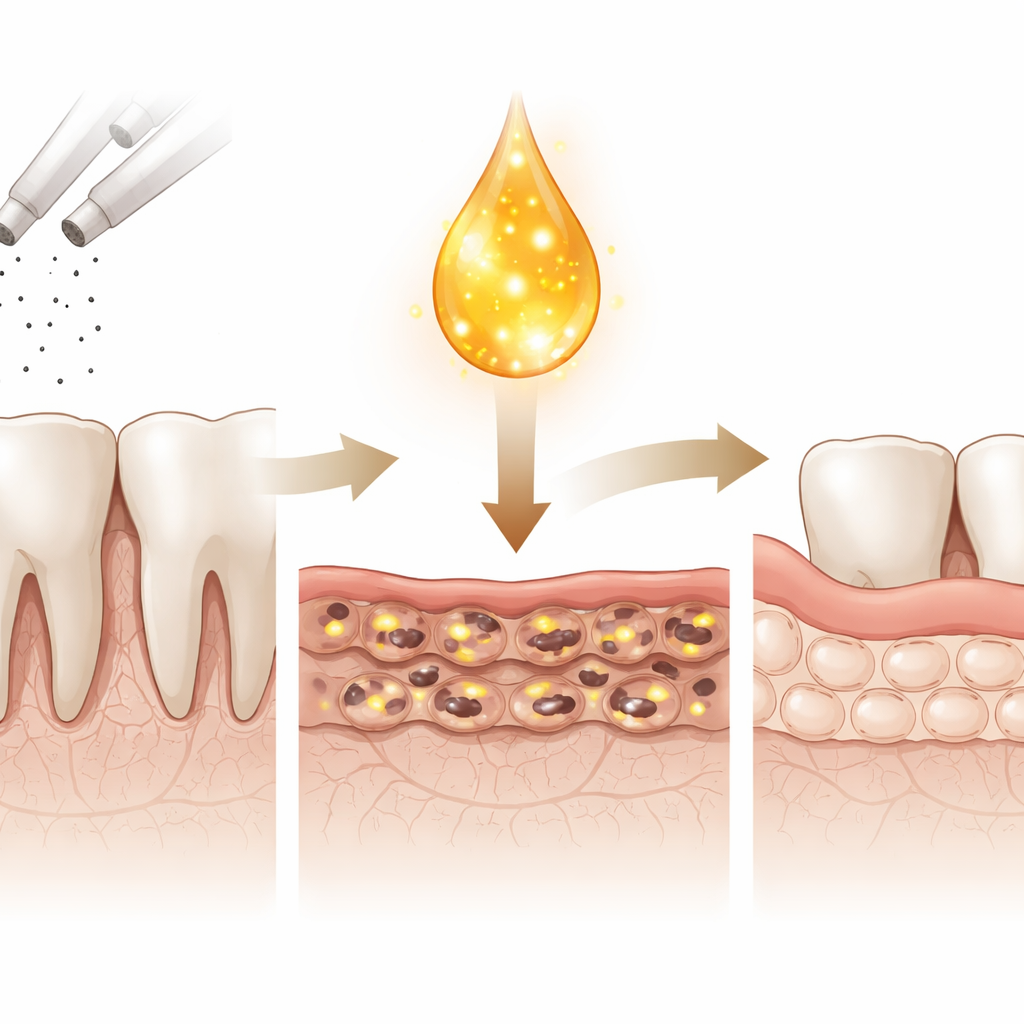
دفعة شفاء مأخوذة من الدم
تُحضَر البلازما الغنية بالصفائح الدموية (PRP) عن طريق طرد عينة صغيرة من الدم لزيادة تركيز الصفائح الدموية، وهي شظايا دقيقة محمَّلة بعوامل نمو وجزيئات إشارية. يستخدم أطباء الأسنان بالفعل PRP في بعض العمليات لتشجيع الشفاء الأسرع. في هذا العمل، عالج الباحثون الأرومات الليفية البشرية المزروعة مخبرياً بجرعات من النيكوتين تماثل المستويات الواقعية الموجودة في دم المدخنين. تسببت مستويات النيكوتين العالية في انتفاخ الخلايا بفقاعات مملوءة بالسوائل، وفقدان الطاقة، وتوقف الانقسام، وفي النهاية الموت. عندما تعرّضت نفس الخلايا المتضررة لكمية متواضعة من PRP، انعكست العديد من هذه التغيرات الضارة: استعادت مستويات الطاقة، نجا عدد أكبر من الخلايا، وأصبح صف الخلايا أكثر كثافة ومظهره أكثر صحة.
النيكوتين و"الأكل الذاتي" الخلوي وكيف يهدئه PRP
أحد تأثيرات النيكوتين الرئيسية هو تضخيم الالتهام الذاتي، وهو نوع من "التنظيف الذاتي" أو "الأكل الذاتي" داخل الخلايا. بجرعات صغيرة، يحافظ هذا المسار على صحة الخلايا عبر إعادة تدوير الأجزاء البالية؛ لكن عند فرط تنشيطه، يصبح علامة على الإجهاد وقد يدفع الخلايا نحو التلف والشيخوخة المبكرة. أظهر الفريق أن النيكوتين زاد من الأجزاء الحمضية والحويصلات المعالجة للنفايات داخل خلايا اللثة، إلى جانب ازدياد في أنواع الأكسجين التفاعلية — جزيئات عالية الطاقة تهاجم مكونات الخلية. خفض علاج PRP هذه الإشارات المرتبطة بالإجهاد، وقلل عدد الحويصلات المفرطة النشاط، وقلل الإجهاد التأكسدي. كما درس الباحثون دودات من نوع C. elegans، نموذج كلاسيكي لدراسة الشيخوخة. قصّر النيكوتين عمرها وحفز الالتهام الذاتي المفرط، لكن إضافة PRP خفّض هذا النشاط المفرط وساعد الديدان على العيش لفترة أطول تحت الضغط.
الإشارات التي تربط الشفاء والالتهاب وإعادة التدوير
لفهم كيف يعيد PRP تشكيل سلوك الخلايا، قاس العلماء عشرات البروتينات الإشارية التي تفرزها خلايا اللثة المعرضة للنيكوتين. بوجود PRP، ارتفعت عدة رسولات مشاركة في الالتهاب ونمو الأوعية الدموية وإعادة تشكيل الأنسجة بنمط منسق. العديد من هذه الجزيئات معروفة بتقاطعها مع المسارات التي تتحكم في الالتهام الذاتي، ما يوحي أن PRP لا يقتصر على تزويد الخلايا بعوامل نمو فحسب — بل يبدو أنه يعيد توازن استجابة الخلايا للإجهاد، يحدّ من الأكل الذاتي المفرط، ويعزز حالة أكثر توجهاً نحو الإصلاح تدعم هجرة الخلايا وإعادة بناء نسيج اللثة التالف.
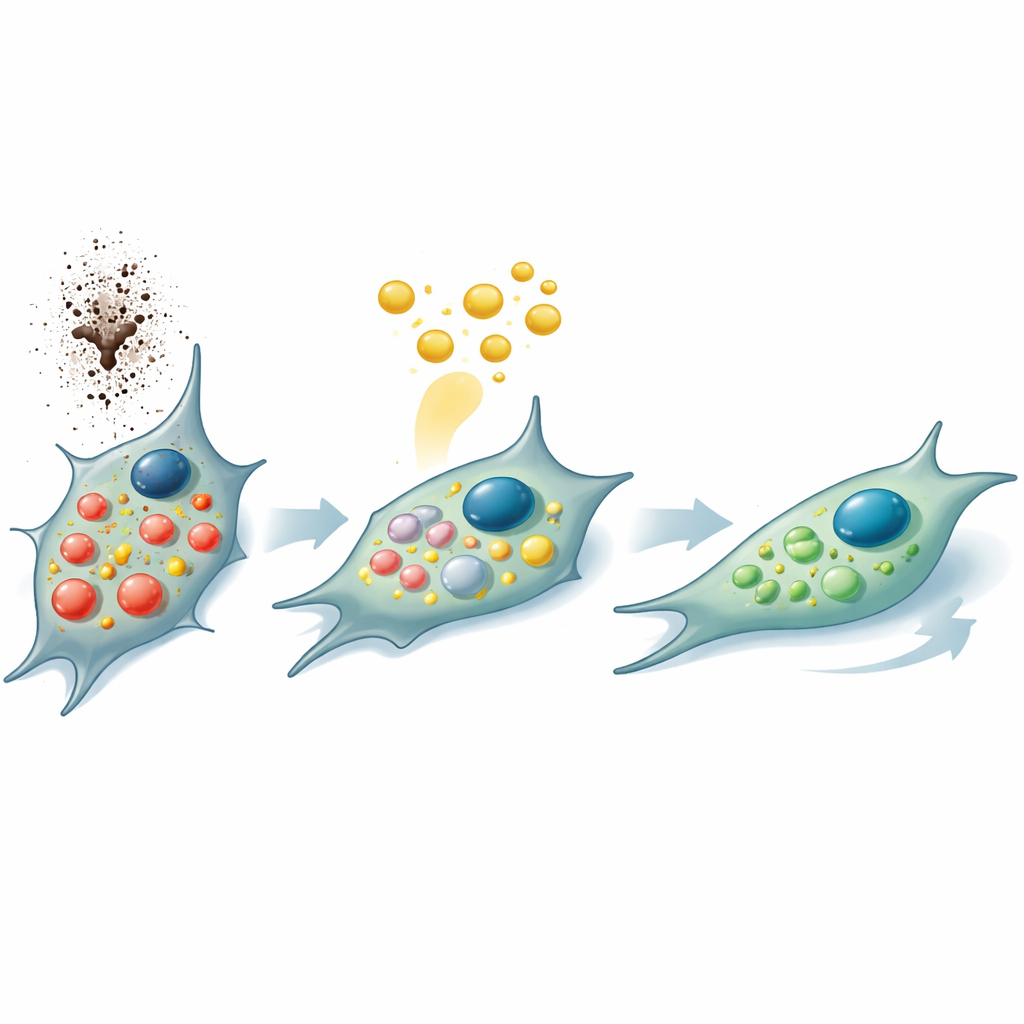
ما الذي قد يعنيه هذا لرعاية أسنان المدخنين
بصورة عامة، تشير الدراسة إلى أن PRP يمكن أن يحمي ويحيي خلايا اللثة التي تضررت بالنيكوتين، جزئياً عبر تهدئة الالتهام الذاتي المفرط والإجهاد التأكسدي وتشجيع حركة الخلايا وبقائها بصحة أفضل. بالنسبة لطب الأسنان، يفتح هذا الاحتمال بأن إضافة PRP إلى بعض علاجات اللثة قد يحسّن الشفاء لدى المرضى الذين ما زالوا يستخدمون النيكوتين. مع ذلك، أُجريت التجارب في ثقافات خلوية وعلى ديدان، وليست على أشخاص لديهم تاريخ طويل من التدخين. يؤكد المؤلفون أنه لا يمكن لأي علاج مستند إلى الدم أن يحل محل الإقلاع عن التبغ: يظل التوقف عن النيكوتين أقوى خطوة لحماية لثتك وصحتك العامة. ينبغي النظر إلى PRP كمساعد محتمل في الإصلاح، لا كذريعة لمواصلة التدخين.
الاستشهاد: Vérièpe-Salerno, J., Cancela, J.A., Vischer, S. et al. Platelet-rich plasma promotes cellular recovery from nicotine-induced toxicity via autophagy modulation. Sci Rep 16, 7979 (2026). https://doi.org/10.1038/s41598-026-38188-1
الكلمات المفتاحية: مرض اللثة, النيكوتين, البلازما الغنية بالصفائح الدموية, إجهاد خلوي, طب الأسنان التجددِي