Clear Sky Science · ar
IL-18 يعزز تليّف البنكرياس عبر إطلاق IL-4 من الخلايا النجميّة البنكرياسية ويحفّز استقطاب البلّعات النسيجية إلى النمط M2
لماذا يهم تندّب البنكرياس
التهاب البنكرياس المزمن هو التهاب طويل الأمد في البنكرياس يدمر هذا العضو الحيوي تدريجياً، وغالباً ما يسبب ألماً شديداً ومشكلات هضمية وزيادة خطر الإصابة بسرطان البنكرياس. من السمات الرئيسية للمرض هو التليّف — نسيج ندبي يحل محل خلايا البنكرياس السليمة. تطرح هذه الدراسة سؤالاً بسيطاً لكنه حاسم: ما الإشارات داخل البنكرياس التي تحوّل الالتهاب المستمر إلى تندّب دائم، وهل يمكن أن يؤدّي حجب هذه الإشارات إلى إبطاء أو إيقاف الضرر؟
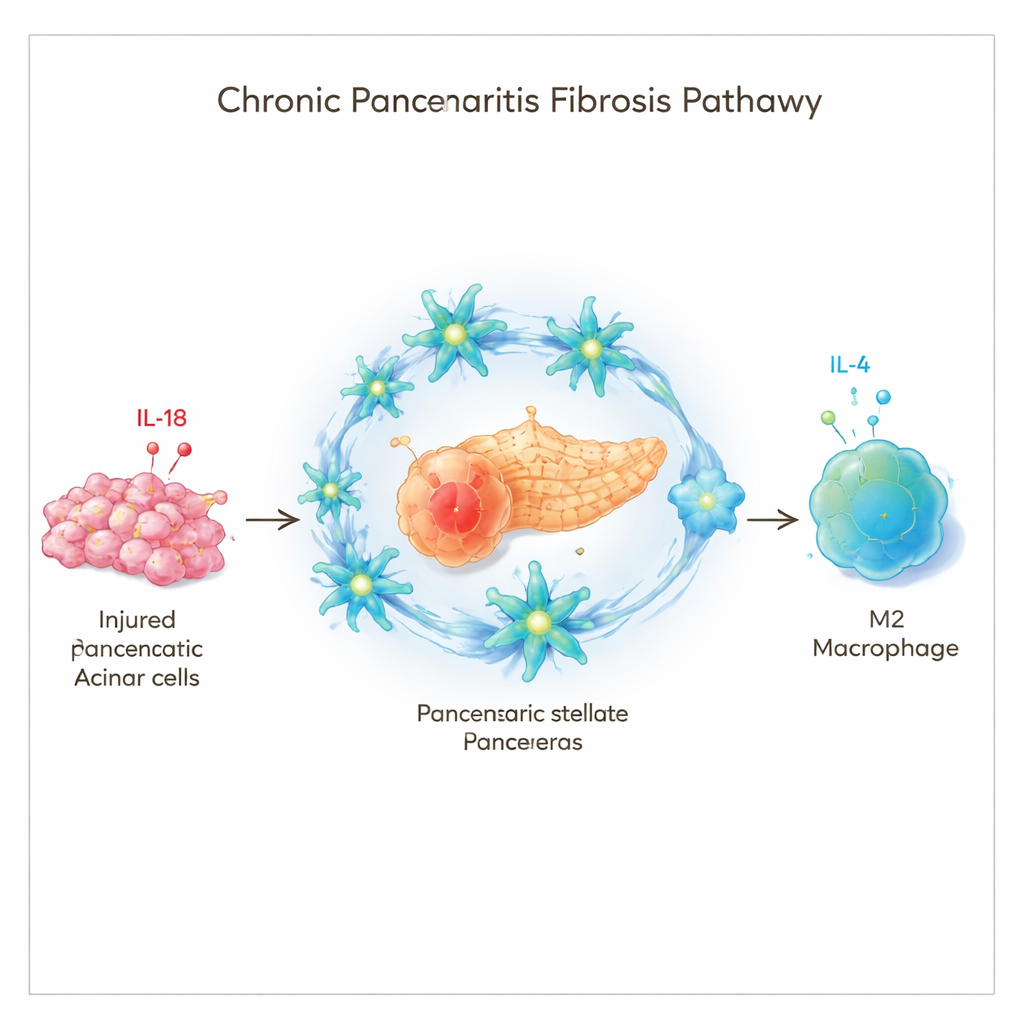
إشارة إنذار مُسبّبة للمشاكل
ركز الباحثون على جزيء يُدعى إنترلوكين‑18 (IL‑18)، وهو جزء من «نظام الإنذار» المناعي في الجسم. يُعرف عن IL‑18 أنه يرتفع أثناء الالتهاب وقد رُبط بالتليّف في القلب والكليتين والكبد. من خلال فحص عينات نسيجية من أشخاص مصابين بالتهاب البنكرياس المزمن واستخدام نماذج فأرية للمرض، وجد الفريق أن مستويات IL‑18 كانت أعلى بكثير في البنكرياسات المريضة مقارنةً بالسليمة. والأهم من ذلك، كلما زاد IL‑18 في بنكرياس المريض، كان التليّف أكثر امتداداً. وتتبعوا مصدراً رئيساً لهذا IL‑18 إلى الخلايا الحُويصلية المصابة — خلايا الإفراز الإنزيمية الهضمية العادية في البنكرياس — التي تُطلق IL‑18 عندما تتضرر.
الخلايا الداعمة التي تتحول إلى صانعي ندوب
النسيج الندبي في التهاب البنكرياس المزمن يُنتَج في المقام الأول بواسطة الخلايا النجمية البنكرياسية، وهي نوع من خلايا الدعم التي تكون عادة خاملة لكنها قد تتحول إلى حالة فعّالة منتجة للندوب. أظهرت الدراسة أن هذه الخلايا النجمية تحمل مستقبل IL‑18، ما يعني أنها تستطيع استشعار هذه إشارة الإنذار مباشرة. في الفئران المُعدّلة لعدم وجود هذا المستقبل، أدت الإصابات المتكررة إلى تليّف بنكرياسي أقل بكثير، وانخفاض تنشيط الخلايا النجمية، ونمط مختلف لاقتحام الخلايا المناعية. وتشير هذه النتائج إلى أن IL‑18 ليس مجرد علامة مرافق للالتهاب؛ بل هو دافع يساعد على دفع الخلايا النجمية والأنسجة المحيطة نحو التليّف.
كيف تُدفع الخلايا المناعية نحو وضعية مهيّأة للتندّب
لاعب رئيسي آخر في التهاب البنكرياس المزمن هو البلّاعة النسيجية (الماكروفاج)، وهي خلية مناعية يمكن أن تتبنى «شخصيات» مختلفة. في حالة واحدة (تُسمّى غالباً M1) تكون البلّاعات مهاجمة؛ أما في حالة أخرى (M2) فتميل إلى إعادة تشكيل الأنسجة وقد تروّج للتليّف للأسف. وجد العلماء أن الفئران التي تفتقد مستقبل IL‑18 كان لديها عدد أقل من البلّاعات من نوع M2 في بنكرياسها. ومن الغريب أن IL‑18 بمفرده لم يحول البلّاعات مباشرة إلى نمط M2 في الأطباق المخبرية. بدلاً من ذلك، عمل IL‑18 على الخلايا النجمية، محفّزاً إياها على إفراز جزيء إشاري آخر، إنترلوكين‑4 (IL‑4). يُعرف IL‑4 جيداً بقدرته على توجيه البلّاعات إلى الحالة M2 المروجة للتليّف. عندما تعرّضت البلّاعات لسائل مأخوذ من خلايا نجمية عولجت بـ IL‑18، تحوّلت بقوة نحو نمط M2 — لكن هذا التأثير اختفى إلى حد كبير عند حجب IL‑4.
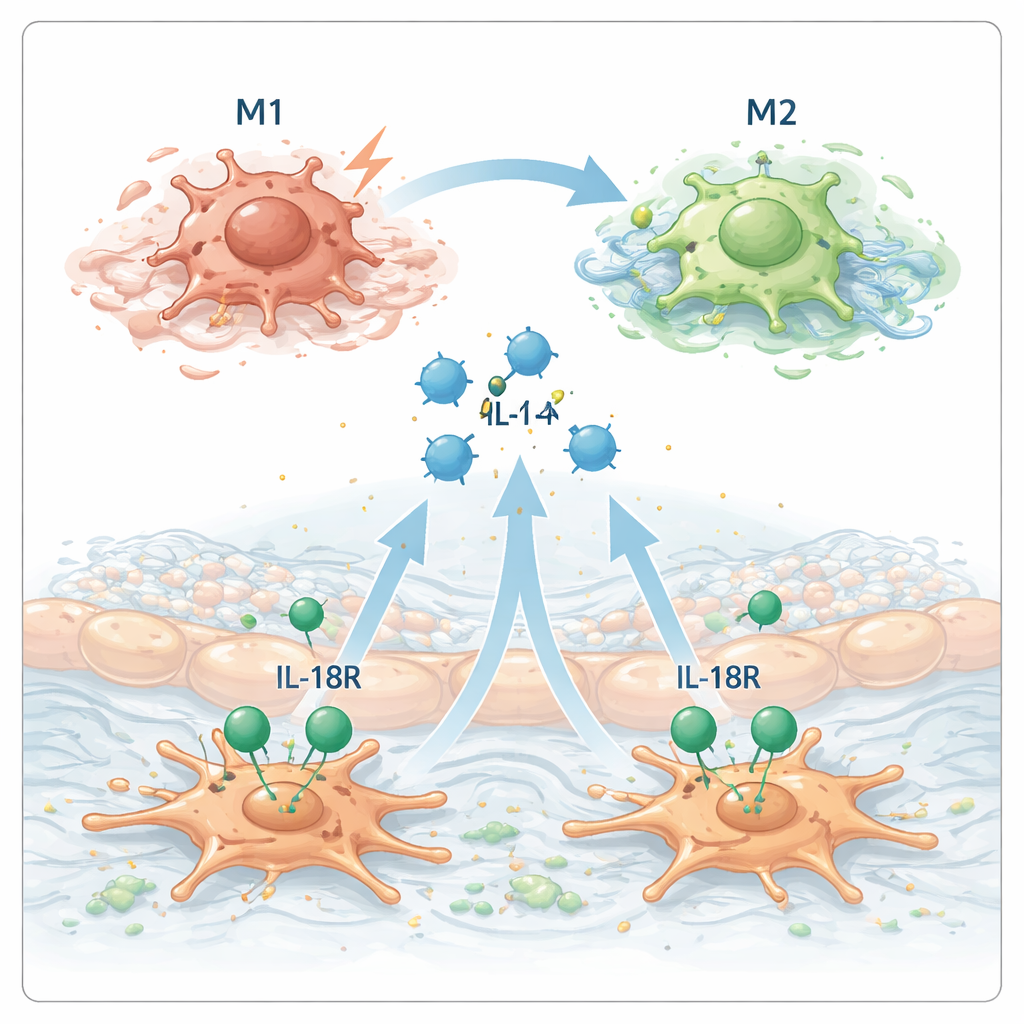
تفاعل سلسلة يفاقم التندّب
بتجميع هذه الأجزاء، يقترح الباحثون وجود تفاعل تسلسلي داخل البنكرياس المريض. أولاً، تتضرر الخلايا الحُويصلية وتفرز IL‑18. بعد ذلك، ينشّط IL‑18 الخلايا النجمية المجاورة عبر مستقبلها. استجابة لذلك، تفرز الخلايا النجمية IL‑4، الذي يوجّه البلّاعات لاعتماد الحالة M2 المروّجة للندوب. هذه البلّاعات M2 بدورها تحفّز الخلايا النجمية أكثر وتساهم في ترسيب الكولاجين ومكوّنات أخرى للنسيج الندبي، مما يعمّق التليّف. في تجارب الفئران، إضافة IL‑18 أثناء التهاب البنكرياس المزمن زاد من شدة المرض وغلّظ التليّف، لكن حجب IL‑4 قلّل هذه الآثار الضارّة.
ماذا يعني هذا لعلاجات المستقبل
بالنسبة لغير المتخصّصين، الرسالة الأساسية هي أن تليّف التهاب البنكرياس المزمن ليس عشوائياً؛ بل تديره محادثة محددة بين الخلايا البنكرياسية المصابة والخلايا النجمية والخلايا المناعية. يقع IL‑18 قرب قمة سلسلة هذه الاتصالات، ويعمل IL‑4 كوسيط رئيسي. من خلال التدخّل في IL‑18 أو مستقبله على الخلايا النجمية، أو في إشارات IL‑4 إلى البلّاعات، قد تتمكّن علاجات مستقبلية من تقليل أو إبطاء تراكم النسيج الندبي في التهاب البنكرياس المزمن، وبالتالي الحفاظ على وظيفة البنكرياس وتحسين جودة حياة المرضى.
الاستشهاد: Tu, G., Peng, C., Xie, S. et al. IL-18 promotes pancreatic fibrosis via release of IL-4 from pancreatic stellate cells and induces macrophage M2 polarization. Sci Rep 16, 7540 (2026). https://doi.org/10.1038/s41598-026-38168-5
الكلمات المفتاحية: التهاب البنكرياس المزمن, تليّف البنكرياس, IL-18, IL-4, استقطاب البلّعات النسيجية