Clear Sky Science · ar
تسلسل الحمض النووي الريبي يكشف تعبيرًا تفاضليًا للحمض النووي الريبي الحلقي في سرطان الرئة صغير الخلايا لدى البشر
لماذا قد تغيّر حلقات الحمض النووي الريبي الصغيرة رعاية سرطان الرئة
سرطان الرئة صغير الخلايا هو أحد أكثر أنواع السرطان فتكا، ينتشر بسرعة وغالبًا ما يقاوم العلاج الكيميائي. لا تزال لدى الأطباء اختبارات قليلة للكشف المبكر أو للتنبؤ بمن سيستجيب للعلاج. تبحث هذه الدراسة في فئة غير مألوفة من الجزيئات الجينية تُعرف بالحمض النووي الريبي الحلقي — حلقات صغيرة من الحمض النووي الريبي مستقرة بشكل مفاجئ داخل خلايانا — لمعرفة ما إذا كانت تسهم في دفع هذا السرطان العدواني وما إذا كان يمكن استخدامها كمؤشرات حيوية جديدة وأكثر موثوقية.
فهم أكثر أنواع سرطان الرئة عدوانية
يشكل سرطان الرئة صغير الخلايا نحو واحد من كل خمسة حالات سرطان رئة فقط، لكنه يسبب نسبة غير متناسبة من الوفيات لأنه ينمو بسرعة، وينتشر مبكرًا، وغالبًا ما يعود بعد العلاج الكيميائي. يُشخَّص معظم المرضى في مرحلة متقدمة، عندما لا تُعتبر الجراحة خيارًا وتكون عينات الأنسجة محدودة. بينما رسم الباحثون العديد من طفرات الـDNA في هذا النوع من السرطان، فهم يعرفون أقل بكثير عن كيفية تأثير الحمضيات النووية الريبية غير المشفرة — جزيئات لا تُنتج بروتينات لكنها تؤثر بشدة في سلوك الخلايا — على المرض. تُعدّ الحمضيات النووية الريبية الحلقيّة (circRNAs) مجموعة مثيرة للاهتمام، لأن بنيتها الدائرية المغلقة تجعلها أكثر مقاومة للتحلل مقارنةً بالحمضيات الريبية العادية، مما يثير الأمل بأنّها قد تُقاس بثبات في الأنسجة أو حتى في الدم.
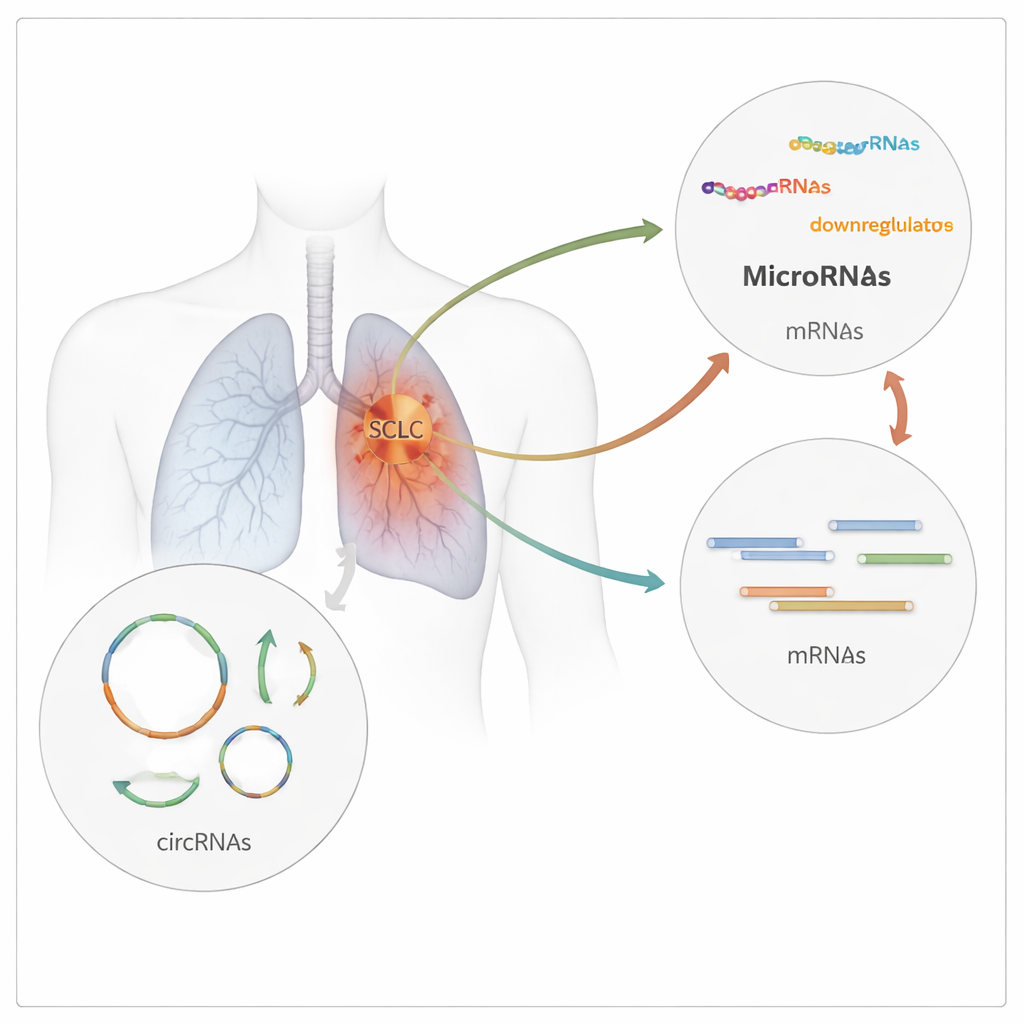
البحث عن حلقات الحمض الريبي في نسيج الورم
جمعت فريق البحث في الهند خزعات أورام من مرضى تم تشخيصهم حديثًا بسرطان الرئة صغير الخلايا وقارنوها بأنسجة رئوية طبيعية من أشخاص أجروا جراحة لسرطان الرئة غير صغير الخلايا في مراحل مبكرة. باستخدام تسلسل عالي الإنتاجية للحمض النووي الريبي، فحصوا أكثر من 26,000 وصلة يمكن أن تتشكل عندها الحمضيات الريبية الحلقيّة، ثم قاموا بتصفية وتحليل البيانات لتحديد أي circRNAs تختلف فعلاً بين العينات السرطانية وغير السرطانية. وجدوا 23 حمضًا نوويًا ريبيًا حلقيًا تغيرت نشاطاتها بشكل ملحوظ في سرطان الرئة صغير الخلايا: 13 منها كانت أكثر وفرة و10 أقل وفرة في الأورام مقارنةً بالنسيج الرئوي الطبيعي. نشأت هذه الجزيئات من 21 جينًا مختلفًا، مما يوحي بإعادة توصيل واسعة لتنظيم الحمض الريبي في هذا النوع من السرطان.
بناء شبكة ثلاثية الطبقات للتحكم بالحمض الريبي
غالبًا ما تعمل الحمضيات الريبية الحلقيّة كإسفنج جزيئي، تمتص المايكرو RNA — قصاصات قصيرة من الحمض الريبي التي تُثبّط عادةً تعبير جينات محددة. لرسم هذه الشبكة الرقابية، استخدم الباحثون قواعد بيانات عامة للتنبؤ أي المايكرو RNAs يمكن أن يرتبط بكل واحد من circRNAs الثلاثة والعشرين المعدلة، وأي الجينات من المرجح أن تتأثر بتلك المايكرو RNAs. كانت النتيجة شبكة ثلاثية الكثافة تربط 23 حمضًا نوويًا ريبيًا حلقيًا بـ241 مايكرو RNA ونحو 7,800 جين مشفر للبروتين. عند فحص وظائف هذه الجينات، تَمَركّزت العديد منها في التحكم بدورة الخلية، وتحلل البروتين، والاستجابات للضغط، ومسارات معروفة مرتبطة بالسرطان مثل p53 وMAPK وHippo والشيخوخة الخلوية. بعبارة أخرى، تبدو الحلقات الريبية المشوّهة في موضع تقاطع الدوائر الرئيسية للنمو والبقاء في خلايا سرطان الرئة صغير الخلايا.
حلقاَا حمض ريبي بارزان بوعود تشخيصية
من بين جميع circRNAs المتغيرة، برز اثنان. الأول، المسمى circLIFR، كان منخفضًا باستمرار في أنسجة SCLC وفي عدة خطوط خلوية لسرطان الرئة صغير الخلايا مقارنةً بخلايا الرئة الطبيعية. كانت المايكرو RNAs الشريكة له، بمن فيهم miR‑1234‑3p وmiR‑375‑3p، مرتفعة بشدة، وهو ما يتوافق مع الفكرة القائلة بأن فقدان إسفنجة الحمض الريبي يترك المزيد من المايكرو RNAs الحرة لتؤثر على الجينات المرتبطة بالسرطان. الحلقة الأخرى، circCAMSAP1، أظهرت النمط العكسي: كانت مرتفعة في الأورام، بينما كان أحد شركائها المبلغ عنهم من المايكرو RNA، miR‑145‑5p، منخفضًا sharply. المرضى الذين تفاقم سرطانهم رغم العلاج الكيميائي من الخط الأول ميالون إلى وجود مستويات أعلى من circCAMSAP1، مما يوحي بارتباط بمقاومة العلاج. عندما اختبر الفريق مدى قدرة هذه الجزيئات على تمييز نسيج SCLC عن الرئة الطبيعية، أدت circLIFR أداءً جيدًا بشكل خاص، بمقياس دقة (AUC) أعلى من 0.9، بينما أظهرت circCAMSAP1 والمايكرو RNAs المرتبطة بها قوة تشخيصية متوسطة لكنها لا تزال مفيدة.
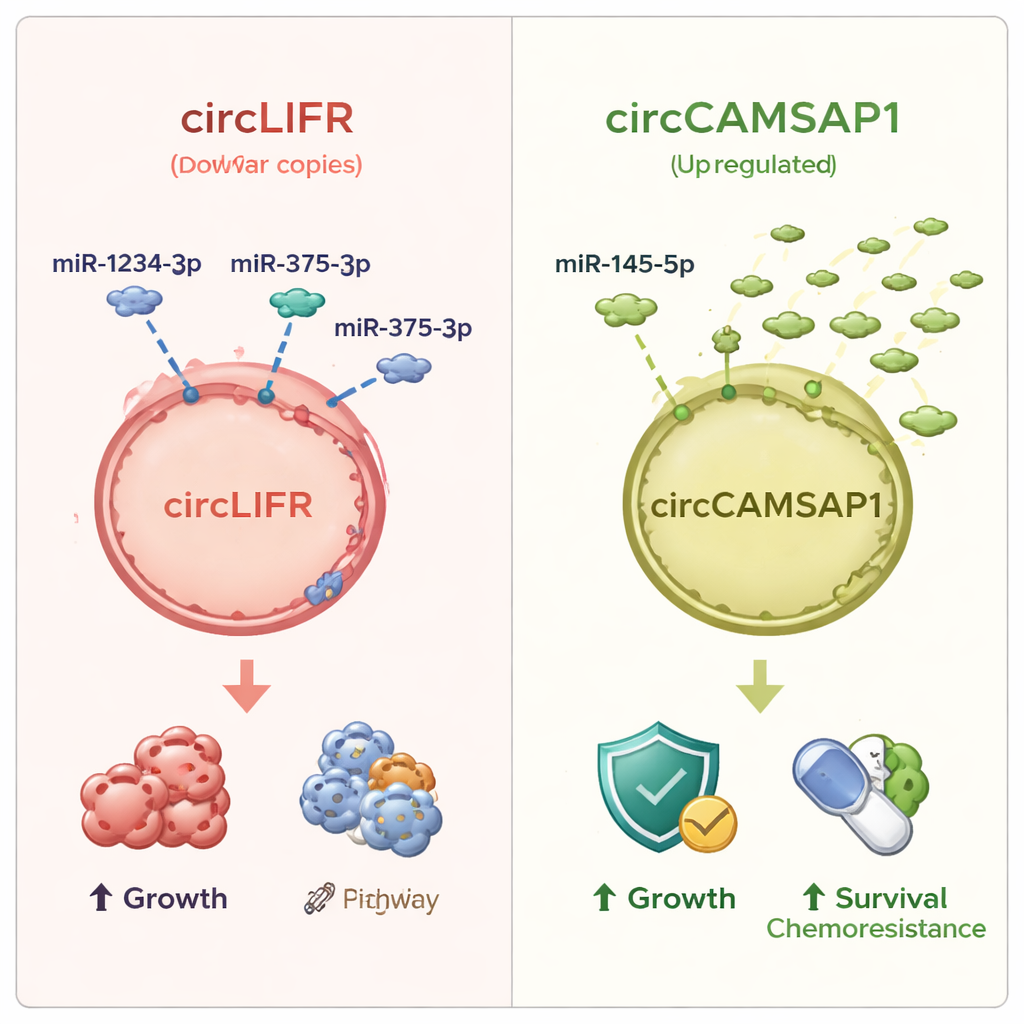
ماذا قد يعني هذا للمرضى
للقارئ العام، الخلاصة أن هذه الدراسة تكشف عن طبقة جديدة من التنظيم في سرطان الرئة صغير الخلايا — مبنية من حلقات حمض نووي ريبي صغيرة وشركائها — تساعد في تنظيم سرعة نمو الخلايا الورمية، وكيف تستجيب للضغط، وربما كيف تتحمل العلاج الكيميائي. يظهر حمضان نوويان ريبيان حلقيان محددان، circLIFR وcircCAMSAP1، كعلامتين واعدتين بشكل خاص: أحدهما يميل إلى الفقد في الأورام، والآخر يزداد، ومع المايكرو RNAs المرتبطة بهما يمكن أن يساعدا في التفريق بين النسيج السرطاني والطبيعي وقد يشيرا إلى كيفية استجابة مرض المريض للعلاج. بينما لا تزال هذه النتائج بحاجة إلى تجارب مخبرية لإثبات السبب والنتيجة ودراسات سريرية أكبر لاختبار الفائدة في العالم الحقيقي، فإنها تشير إلى اختبارات مستقبلية في الدم أو الأنسجة قائمة على الحمضيات الريبية الحلقيّة قد تحسّن تشخيص وإدارة أحد أكثر أشكال سرطان الرئة تحديًا.
الاستشهاد: Saxena, V., Abhilash, D., Budhraja, A. et al. RNA sequencing reveals differential expression of circular RNAs in human small cell lung cancer. Sci Rep 16, 7134 (2026). https://doi.org/10.1038/s41598-026-38145-y
الكلمات المفتاحية: سرطان الرئة صغير الخلايا, الحمض النووي الريبي الحلقي, المايكرو RNA, مؤشرات حيوية للسرطان, تسلسل الحمض النووي الريبي