Clear Sky Science · ar
أوبيnوتوزوماب يُحدث زعزعة استقرار الليزوزومات عبر تثبيط TRPML2 المعتمد على سفنغوميلين
لماذا تهمنا هذه القصة عن الأجسام المضادة
بالنسبة لكثير من الأشخاص المصابين بلمفومات الخلايا B، حولت أدوية الأجسام المضادة الحديثة تشخيصًا كان يُعد مميتًا بلا استثناء إلى مرضٍ يمكن معالجته. ومع ذلك، ليست كل الأجسام المضادة متساوية: بعضها يقتل الخلايا السرطانية بقوة وبشكل أكثر ثباتًا من غيرها. تستقصي هذه الورقة سبب تفوق دواء واحد من هذا النوع، أوبيnوتوزوماب، في قتل خلايا اللمفوما مباشرةً بالمقارنة مع سابقتها ريتوكسيماب، عبر التركيز على جهة غير متوقعة داخل الخلية — مراكز التدوير الخلوية نفسها المعروفة بالليزوزومات — وتوازن دقيق من الدهون وقنوات الأيون في أغشيتها.
من الهدف السطحي إلى الانتحار الداخلي
كل من ريتوكسيماب وأوبيnوتوزوماب يتعرفان على نفس الهدف على خلايا B، بروتين يُسمى CD20. لكن المؤلفين يبينون أن أوبيnوتوزوماب يُدخَل إلى داخل الخلية بسرعة وكفاءة أكبر بكثير. بعد ارتباطه بـ CD20 على سطح الخلية السرطانية، تُسحب مجمعات الجسم المضاد-المستقبل إلى الداخل عبر عملية ببتابية وتُسلم إلى حويصلات حمضية، بما في ذلك الليزوزومات. هناك يُحفز أوبيnوتوزوماب نفاذية غشاء الليزوزوم: يصبح غشاء الليزوزوم، الذي هو عادة قوي، مسربًا، مما يسمح لإنزيمات هضمية مثل الكاتيبسينات بالانسياب إلى داخل الخلية وإطلاق مسارات الموت الخلوي. وُجد أن التغيرات في توازن الملح والماء في هذه الحويصلات، التي تتسبب في انتفاخ الليزوزومات، تضخّم هذا التأثير القاتل بشكل كبير.
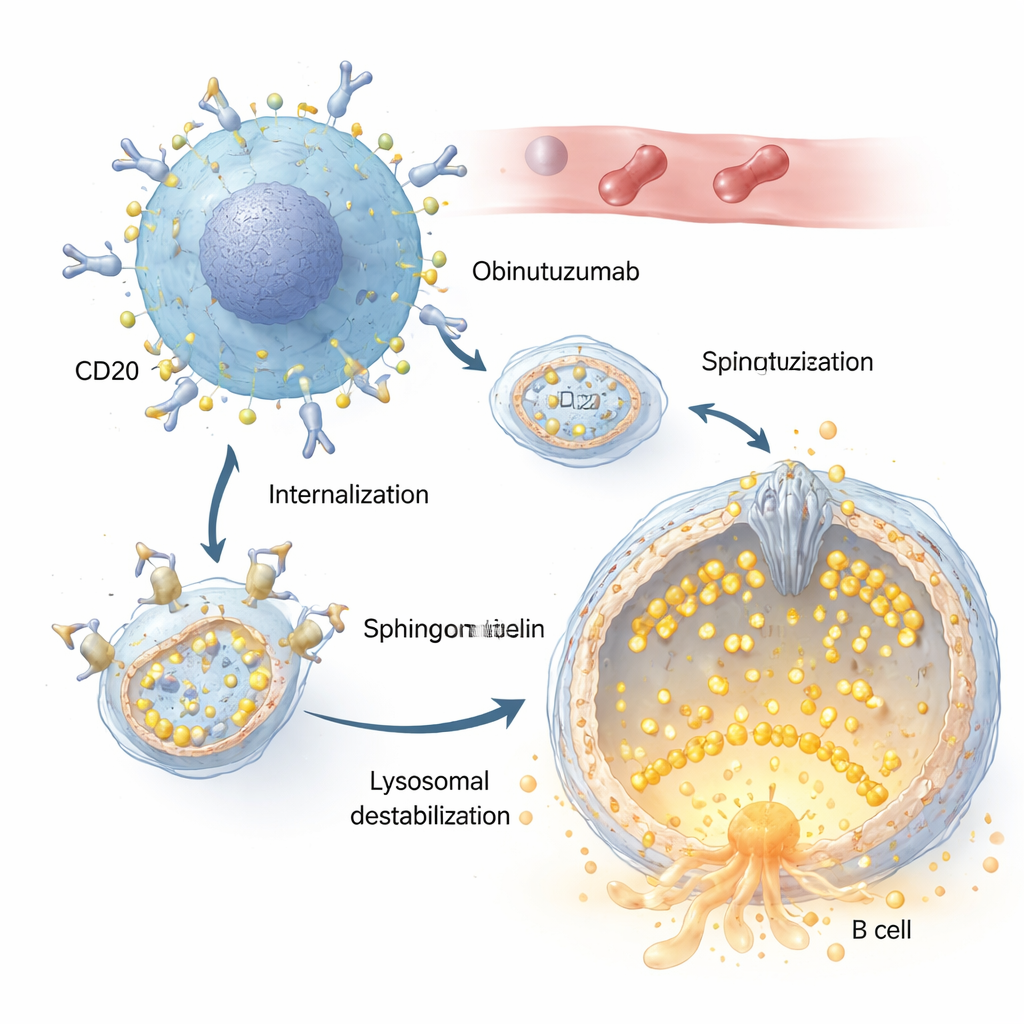
دور قناة حارس صغيرة
المحور المركزي في هذه القصة هو TRPML2، قناة كالسيوم مدمجة في غشاء الليزوزوم. في الظروف الطبيعية، يساعد TRPML2 الليزوزومات على مواجهة الإجهاد الميكانيكي والتناضحي عبر إطلاق الكالسيوم، مما يدعم إصلاح الأغشية، والنقل الخلوي، والتحكم في الحجم. باستخدام مزيج من صبغات الكالسيوم المضيئة ونُسخ معدلة من TRPML2 حساسة للكالسيوم، يظهر الباحثون أن أوبيnوتوزوماب يغلق هذه القناة بسرعة: خلال دقائق من المعالجة، يتوقف الدواء الذي عادة ما يفتح قنوات TRPML عن توليد طفرات الكالسيوم. الأساليب الجينية التي تقلل من مستويات TRPML2، أو المثبطات الجزيئية الصغيرة التي تحجب نشاط TRPML، تجعل خلايا اللمفوما أكثر عرضة لأوبيnوتوزوماب، مما يؤدي إلى تسرب لِيزوزومي أكبر ومعدلات أعلى من موت الخلايا المباشر.
كيف تميل دهون الغشاء الكفة
تسأل الدراسة بعد ذلك ماذا يربط امتصاص الجسم المضاد بإغلاق القناة. يتجه الانتباه إلى السفنغوميلين، وهو ليبيد (دهون) وفير في أغشية الخلايا ومعروف بتأثيره المعوق على قنوات TRPML. باستخدام مسبار فلوري يرتبط بالسفنغوميلين، يجد المؤلفون أن الحويصلات المحتوية على أوبيnوتوزوماب غنية بالسفنغوميلين بمجرد وصولها إلى الحويصلات الحمضية، أكثر بكثير من الحويصلات المحتوية على ريتوكسيماب. عندما تُعالج الخلايا بالسفنغوميليناز، وهو إنزيم يقص السفنغوميلين، يستعاد نشاط إطلاق الكالسيوم عبر TRPML2 حتى في وجود أوبيnوتوزوماب. في ظل هذه الظروف، تكون الليزوزومات أقل ميلاً للتسرب، ويموت عدد أقل من الخلايا، ما يشير بقوة إلى أن تراكم السفنغوميلين يعطل TRPML2 ويمهد الليزوزومات للانفجار.
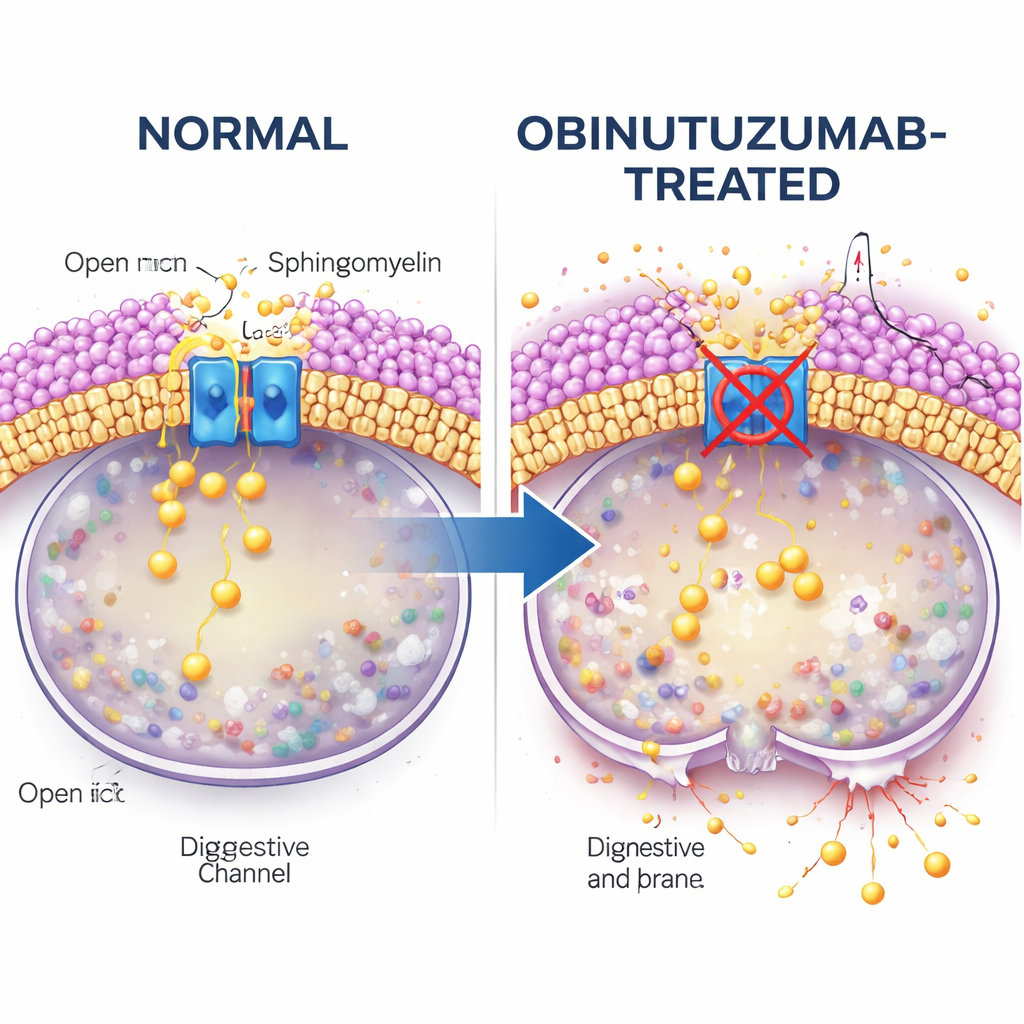
مسارات المرور ونقاط تفتيش الكوليسترول
مسار دخول أوبيnوتوزوماب إلى الخلية له أيضًا أهمية. تكشف الميكروسكوبي الإلكتروني ووسم الأجسام المضادة الحساس للـ pH أن أوبيnوتوزوماب يغادر سطح الخلية ويدخل الحويصلات داخل الخلوية أسرع من ريتوكسيماب. عندما يتدخل الباحثون في مسارات الامتصاص المحددة، يجدون أن حجب شكلٍ من البلعمة الخلوية المعتمد على الكوليسترول (بمركب يُدعى فيليبين) يمنع أوبيnوتوزوماب من إيقاف TRPML2، ويقلّل جزئيًا من تلف الليزوزومات وموت الخلايا. مثبطات البلعمة الأخرى لا تُظهر هذا التأثير الوقائي. يشير هذا إلى مسار متخصص غني بالكوليسترول والسفنغوميلين يُوصل أوبيnوتوزوماب إلى الليزوزومات بطريقة تُمهّد لتثبيط TRPML2 وزعزعة الأغشية لاحقًا.
ما يعنيه هذا لعلاج السرطان في المستقبل
بعبارات بسيطة، تُظهر هذه الدراسة أن أوبيnوتوزوماب يقتل لمفومات الخلايا B بكفاءة لأنّه يجبر الليزوزومات على الدخول في حالة هشة. عبر دفع مجمعات الجسم المضاد–CD20 إلى حويصلات غنية بالسفنغوميلين، يقوم الدواء بشكل غير مباشر بإيقاف قناة الكالسيوم الوقائية TRPML2. عندما يزول هذا الحاجز، تصير الليزوزومات أكثر عرضة للانفجار تحت الضغط، وتتدفق إنزيمات مُسببة للتآكل تفسد الخلية السرطانية من الداخل. فهم محور الدهون–قناة الأيون هذا لا يفسر فقط تفوّق أوبيnوتوزوماب على ريتوكسيماب؛ بل يقترح أيضًا استراتيجيات جديدة لتعزيز علاجات الأجسام المضادة — على سبيل المثال، اقترانها بعقاقير تغير مستويات السفنغوليبيدات أو تعزز نشاط TRPML2 لضبط كيفية ومتى تدمر ليزوزومات الخلايا الورمية نفسها.
الاستشهاد: Oh, J., Jin, N., Kwon, S. et al. Obinutuzumab induces lysosomal destabilization via sphingomyelin-dependent inhibition of TRPML2. Sci Rep 16, 7079 (2026). https://doi.org/10.1038/s41598-026-38087-5
الكلمات المفتاحية: أوبيnوتوزوماب, لمفومة الخلايا B, الليزوزوم, سفنغوميلين, TRPML2