Clear Sky Science · ar
هندسة كرايوجيلات مفعلة بالبوليثيلينإمين–المعادن لربط الكاتالاز بأداء متفوق واستمرارية طويلة الأمد
لماذا يهم تثبيت الإنزيمات في موضعها
بروكسيد الهيدروجين منتج كيميائي شائع في مجالات تتراوح من معالجة الأغذية إلى العلاجات الطبية، وتعتمد الخلايا الحية على الإنزيم كاتالاز لتحلّله إلى ماء وآكسجين غير ضارين. في الصناعة، يُستخدم الكاتالاز عادة في صورة مذابة حرة تفقد فعاليتها بسرعة، ولا يمكن استعادتها بسهولة، ويجب استبدالها بشكل متكرر. تستكشف هذه الدراسة طريقة «لإيقاف» الكاتالاز داخل مادة إسفنجية بحيث يبقى نشطًا لفترة أطول، ويمكن إعادة استخدامه مرات عديدة، ويعمل بكفاءة أكبر — وكل ذلك قد يخفض التكاليف ويجعل العمليات المعتمدة على الإنزيمات أنظف وأكثر استدامة.

بناء إسفنجة ذكية
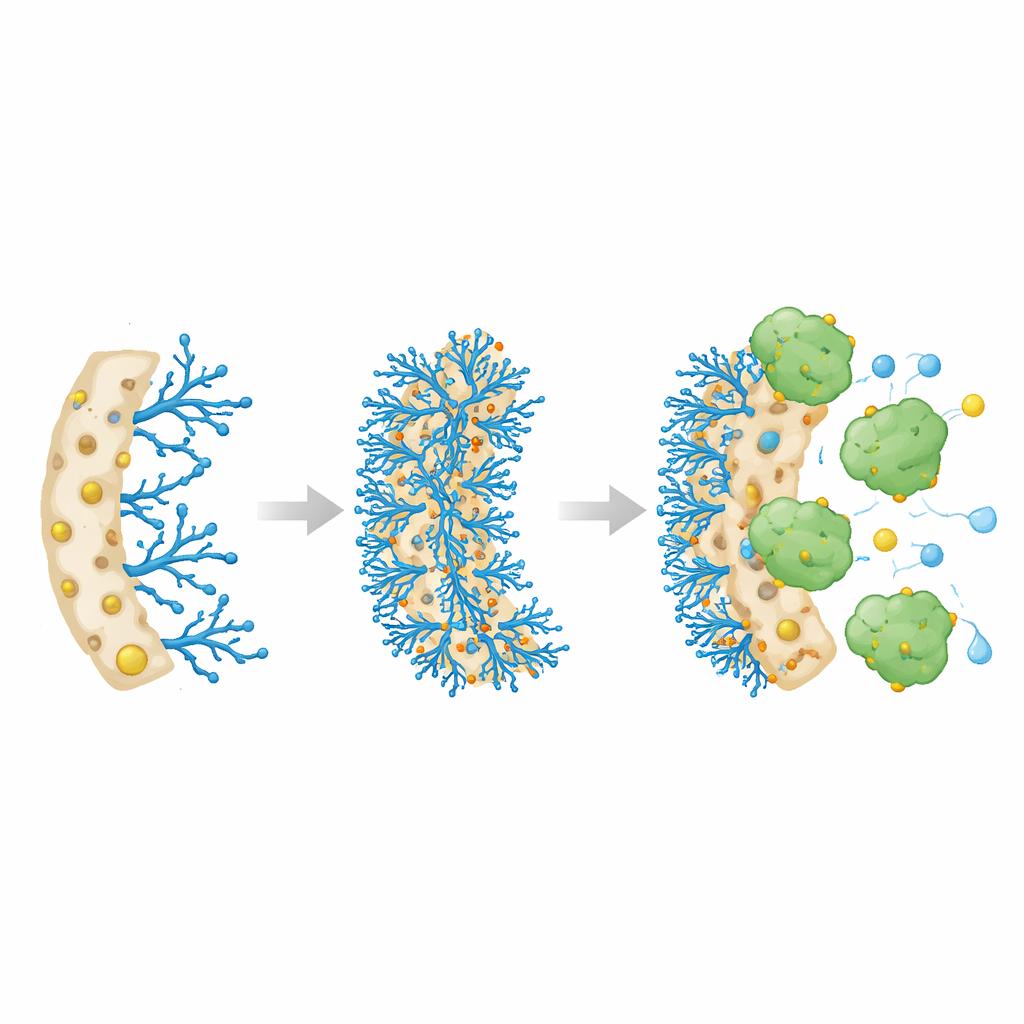
صمّم الباحثون إسفنجة بوليمرية خاصة تُسمى كرايوجيل، تتكوّن بتجميد وذوبان خليط سائل بحيث تنحت بلورات الجليد مسامات كبيرة ومتصلة. تتيح هذه المسامات تدفّق السوائل بحرية، مثل الماء عبر لوفة، بينما يظل الإطار الصلب قويًا ومرنًا. استخدم الفريق مادة أساسية اسمها Poly(HEMA-co-GMA)، ثم ربطوا كيميائيًا بجزئها جزيء متفرّع غني بمجموعات النيتروجين، وهو البوليثيلينإمين (PEI). أخيرًا، أرفقوا أيونات معدنية — نحاس أو نيكل أو كوبالت — إلى مواقع النيتروجين هذه. الفكرة كانت أن تعمل أيونات المعدن كنقاط ترسيخ تجذب الكاتالاز بقوة وتثبّته في مكانه دون أن تسدّ تدفّق السائل عبر الإسفنجة.
ضبط المادة لأفضل أداء
لفهم كيف غيّر كل خطوة من هذا التصميم خواص المادة، استخدم الفريق عدة تقنيات مخبرية لفحص بنيتها وكيميائها واستقرارها. أظهروا أن إضافة PEI ثم المعادن لم ينهار الشبكة المسامية، بل زاد في الواقع قدرة الإسفنجة على الاحتفاظ بالماء، وهو أمر مفيد للحفاظ على راحة الإنزيم ونشاطه. من بين المعادن الثلاثة، أعطى النحاس البيئة الأكثر ترطيبًا وتنظيمًا. كشفت صور المجهر أن المادة الأصلية كانت تبدو كحبيبات متراصة، بينما النسخ المعالجة بـPEI والمعدن فُتحت إلى شبكة أنظف وأكثر استمرارية من المسامات الكبيرة. وأكدت قياسات محتوى المعدن أن النحاس ارتبط بقوة وبكميات أكبر من النيكل أو الكوبالت، مما يشير إلى أنه سيوفر نقاط ترسيخ أكثر فعالية للكاتالاز.
تثبيت الكاتالاز في مكانه
عندما عُرّض الكاتالاز للإسفنجات الحاملة للمعادن المختلفة، جذبت الثلاثة الإنزيم بسرعة، لكن نسخة النحاس برزت بشكل خاص. حمّلت أعلى كمية من الكاتالاز — حوالي 392 ملليغرام لكل غرام من الإسفنجة الجافة — ووصلت إلى حالة توازن خلال نحو ثماني ساعات. ثم فحص الباحثون مدى كفاءة الإنزيم المثبت مقارنةً بالكاتالاز الحر في المحلول. رغم أن السرعة القصوى للتفاعل لكل غرام من الإنزيم انخفضت بعض الشيء، أظهر الكاتالاز المثبت جاذبية ظاهرية أقوى كثيرًا للركيزة، بروكسيد الهيدروجين. عمليًا، يعني ذلك أن الإنزيم المرتبط أدى وظيفته بكفاءة أكبر عند مستويات ركيزة أقل، على الأرجح لأن الإسفنجة النحاسية المسامية والمملوءة بالماء ركّزت الركيزة بالقرب من الإنزيم وساعدت على الحفاظ على شكله النشط.
إنزيم يتحمل الزمن
واحدة من أكبر فوائد تثبيت الإنزيمات هي وعد قابلية إعادة الاستخدام وطول عمر الرف. هنا، أثبت الكاتالاز المربوط بكرايوجيل قائم على النحاس متانة أكبر بكثير من نظيره الحر. بعد 15 دورة استخدام متكررة، احتفظ الإنزيم المثبت بنحو ثُلث نشاطه الأولي، بينما عادةً ما يُتلف الكاتالاز الحر بعد استخدام واحد. في اختبارات التخزين عند درجة حرارة الثلاجة على مدى 70 يومًا، حافظ الكاتالاز المثبت على أكثر من 60% من نشاطه، أي ما يقارب ضعفي نشاط الإنزيم الحر. كما سمحت الإسفنجة بفصل الإنزيم وإعادة تحميله عدة مرات باستخدام محلول ملحي بسيط، ما يُظهر أن المادة نفسها يمكن إعادة استخدامها دون فقدان كبير في السعة.
ماذا يعني هذا للتطبيقات العملية
بالنسبة للقارئ غير المتخصص، الخلاصة الأساسية هي أن الباحثين طوروا نوعًا من «الإسفنجة الإنزيمية» القابلة لإعادة الاستخدام التي تثبت الكاتالاز بقوة ولكن بلطف، مما يساعده على العمل بشكل أفضل عند مستويات كيميائية أقل ويجعله يدوم لفترة أطول في الاستخدام والتخزين. من خلال الجمع بين كرايوجيل مسامي للغاية وPEI وأيونات النحاس، أنشأوا منصة تجمع بين تحميل مرتفع للإنزيم، كفاءة محسّنة، واستقرار طويل الأمد قوي. يمكن إدخال مثل هذه المواد في أنظمة صناعية أو بيئية لتحطيم بروكسيدات الهيدروجين والمواد ذات الصلة بشكل أكثر اعتمادية وبمخلفات أقل، مما يوفر خطوة عملية نحو تقنيات أكثر خضرة معتمدة على الإنزيمات.
الاستشهاد: Erol, K., Alkan, M.H. & Alacabey, İ. Engineering polyethylenimine–metal functionalized cryogels for superior catalase binding, activity, and long-term durability. Sci Rep 16, 7880 (2026). https://doi.org/10.1038/s41598-026-38040-6
الكلمات المفتاحية: تثبيت الإنزيمات, كاتالاز, كرايوجيل, بوليمرات مفعلة بالنحاس, التحفيز الحيوي