Clear Sky Science · ar
الإمكانات التآزرية التشكيلية المضادة للسرطان للتاموكسيفين مع النارينجين والديوسميتِن في خلايا سرطان الثدي MCF-7 وتوصيلهما على هيئة ليبوسومات
لماذا يهم اقتران دواء شائع بمركبات الحمضيات
يعالج سرطان الثدي غالبًا بالتاموكسيفين، حبة تمنع الهرمونات وقد أنقذت الكثير من الأرواح. لكن مع مرور الوقت، تتكيّف بعض الأورام مع الدواء، وقد تكون الآثار الجانبية للعلاج صعبة التحمل. تستكشف هذه الدراسة فكرة جذابة: هل يمكننا جعل التاموكسيفين يعمل بشكل أفضل وربما بجرعات أقل عبر اقترانه بمركبات طبيعية موجودة في ثمار الحمضيات، ثم تعبئتها معًا في فقاعات دهنية صغيرة تُسمى ليبوسومات حتى تصل إلى الخلايا السرطانية بشكل أكثر فعالية؟
مساعدو الحمضيات لدواء سرطاني قديم
ركز الباحثون على مركبين نباتيين، النارينجين والديوسميتِن، وهما فلافونويدان شائعان في الجريب فروت والبرتقال وأنواع أخرى من الحمضيات. في اختبارات مخبرية على خلايا سرطان الثدي الحساسة للإستروجين (MCF-7) وخط سرطاني آخر (T47D)، قاسوا أولًا مدى قدرة كل مركب بمفرده على إبطاء أو قتل الخلايا السرطانية. كان التاموكسيفين الأكثر قوة، لكن النارينجين والديوسميتِن قللا أيضًا من بقاء الخلايا السرطانية، خصوصًا في خلايا MCF-7، ما يوحي بأن لهذه الجزيئات الطبيعية تأثيرًا مضادًا للسرطان بحد ذاتها. ومهد ذلك الطريق لاختبار ما إذا كان الجمع بينها وبين التاموكسيفين سيؤدي إلى تأثير يفوق مجموع تأثيراتهما المنفردة.
أقوى معًا: اختبار تراكيب الأدوية
لفهم كيفية تفاعل الأدوية، عالج الفريق خلايا سرطان الثدي بالتاموكسيفين مع النارينجين، أو التاموكسيفين مع الديوسميتِن، أو الثلاثة معًا بنسب ثابتة مختلفة. باستخدام نهج رياضي معياري لأزواج الأدوية، أظهروا أن عدة تراكيب كانت تآزرية — أي أن الخليط قتل مزيدًا من الخلايا السرطانية مقارنةً بما كان متوقعًا من كل دواء بمفرده. كانت نسبة تقريبًا ضعف كمية الفلافونويد إلى التاموكسيفين (1:2) فعالة بشكل خاص، لا سيما في حالة التاموكسيفين مع النارينجين. في هذه الظروف، أمكن تحقيق نفس أثر قتل السرطان بكمِّيات أقل من التاموكسيفين، وهي ميزة رئيسية إذا تُرجمت إلى تقليل الآثار الجانبية لدى المرضى.
تحفيز انتحار الخلايا السرطانية
بعد ذلك، تساءل العلماء عما يحدث داخل الخلايا السرطانية. راقبوا الإجهاد التأكسدي — تراكم أنواع الأكسجين التفاعلية — وعلامات الموت المبرمج للخلايا أو الاستماتة. أدت التركيبات، خصوصًا المزيج الثلاثي من التاموكسيفين والnارينجين والديوسميتِن، إلى إجهاد تأكسدي أعلى وميزات استماتة أكثر وضوحًا مقارنةً بالتاموكسيفين وحده. تحت الميكروسكوب، أظهرت خلايا أكثر الشكل المنكمش والصبغ المشرق النموذجي للمراحل المتأخرة للموت الخلوي. دعمت تحليلات البروتين هذا: خفضت التركيبات مستويات Bcl-2 وBcl-xL، وهما بروتينان يساعدان عادة الخلايا السرطانية على مقاومة الموت، وزادت من الشكل المنشط لكاسبيز-3، وهو منفذ رئيسي للاستئصال في الاستماتة. بكلمات بسيطة، بدا أن مركبات الحمضيات تساعد على دفع الخلايا المعالجة بالتاموكسيفين إلى حافة الانتحار الخلوي.
تعبئة الأدوية في ناقلات دقيقة
على الرغم من أن التركيبات بدت واعدة، فإن النارينجين والديوسميتِن ليسا قابلين للذوبان جيدًا في الماء وقد يتم امتصاصهما بشكل ضعيف. لمعالجة ذلك، صنع الفريق ليبوسومات — كرات بمقياس النانومتر مصنوعة من دهون طبيعية — يمكنها حمل التاموكسيفين والفلافونويدات معًا. حَسَّنوا تركيب الدهون والمعالجة بحيث كانت الجسيمات الناتجة بحجم حوالي 150–210 نانومتر، وموحدة إلى حدٍ كبير، وتحمل شحنة سطحية تساعد على إبقائها مستقرة في المعلق. أكدت الصور أن الليبوسومات كانت ملساء وشكلها تقريبًا كروي. أظهرت الاختبارات أن جزءًا كبيرًا من كل دواء يمكن حشوه داخلها، وأن الإفراز إلى الوسط المحيط حدث ببطء على مدار 24 ساعة، متبعًا ديناميكيات انتشارية. مثل هذا الإطلاق المتحكم فيه مرغوب لأنه يمكن أن يحافظ على مستويات دواء ثابتة لفترات أطول.
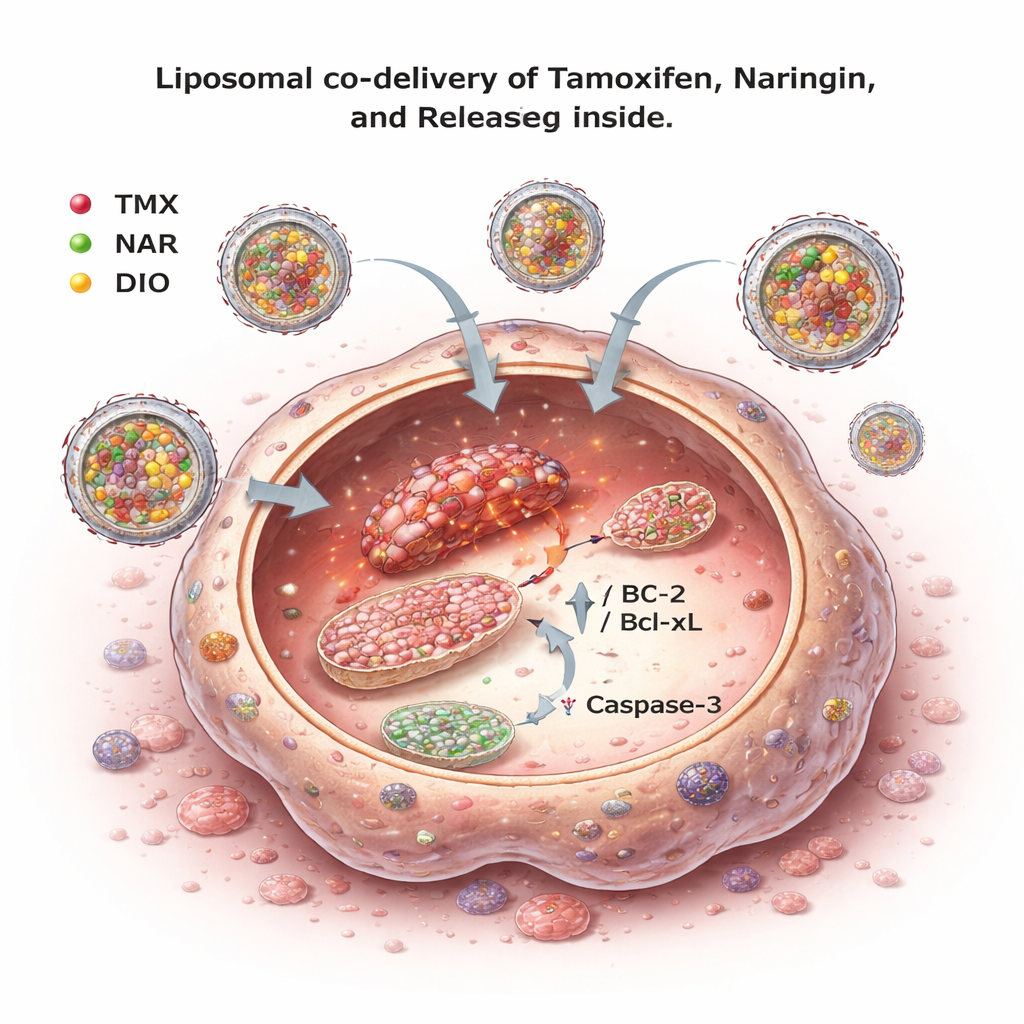
ضرب الأورام بشدة مع الحفاظ على سلامة الخلايا السليمة
عندما اختبرت هذه التركيبات الليبوسومية مرة أخرى على خلايا سرطان الثدي، كانت الليبوسومات الحاملة للأدوية الثلاثة (التاموكسيفين والnارينجين والديوسميتِن معًا) أكثر فعالية في تقليل بقاء الخلايا السرطانية من الليبوسومات التي تحتوي على التاموكسيفين فقط أو على اثنين من الأدوية فقط. والأهم من ذلك، عندما طُبقت نفس التركيبات على خط خلوي بشري غير سرطاني، كان السُمّية ضئيلة ضمن نطاق الجرعات المختبرة، مما يشير إلى درجة من الانتقائية للخلايا السرطانية. بشكل عام، تشير النتائج إلى أن جمع التاموكسيفين مع فلافونويدات مستمدة من الحمضيات وتوصيلها في ليبوسومات يمكن أن يعزز قتل الخلايا السرطانية مع السماح على الأرجح بجرعات تاموكسيفين أقل وأكثر أمانًا.
ماذا قد يعني هذا لرعاية سرطان الثدي في المستقبل
للقارئ العام، الخلاصة هي أن اقتران دواء قياسي لسرطان الثدي بمركبات طبيعية مناسبة، ثم تجميعها داخل ناقلات نانوية ذكية، قد يجعل العلاج أكثر فعالية وربما ألطف. تُظهر الدراسة، في مزروعات خلوية، أن التاموكسيفين يعمل بشكل أفضل مع النارينجين والديوسميتِن: يساعدان على تحويل الخلايا السرطانية من وضع البقاء إلى وضع الانتحار الذاتي ويتم ذلك بكفاءة عند توصيلهما معًا في ليبوسومات. وبينما لا تزال هذه الأعمال في مرحلة المختبر وتحتاج إلى تأكيد في حيوانات التجارب ولاحقًا في تجارب سريرية، فإنها ترسم استراتيجية واعدة: استخدام العلاج التوافقي إلى جانب تقنيات النانو للتغلب على الأورام المقاومة وتحسين النتائج الطويلة الأمد.
الاستشهاد: Uniyal, P., Das Pramanik, S., Pandey, S. et al. Synergistic combinatorial anticancer potential of Tamoxifen with Naringin and Diosmetin in MCF-7 breast cancer cells and their liposomal delivery. Sci Rep 16, 7646 (2026). https://doi.org/10.1038/s41598-026-37954-5
الكلمات المفتاحية: سرطان الثدي, تاموكسيفين, فلافونويدات, التوصيل الليبوسومي, العلاج التوافقي