Clear Sky Science · ar
توليد خلايا T ذات مستقبلات TCRγδ + من الخلايا الجذعية الجنينية البشرية
طرق جديدة لتسليح الجهاز المناعي
تتجه علاجات السرطان بشكل متزايد إلى استدعاء جهاز الجسم المناعي للبحث عن الأورام وقتلها. أحد أنواع الخلايا المناعية الواعدة بشكل خاص، المسماة خلايا تي جاما-دلتا، قادرة على قتل الخلايا السرطانية دون الحاجة إلى التعرف على نوع الأنسجة المحدد للمريض — مما يجعلها مرشحًا قويًا للعلاجات «جاهزة للاستخدام». لكن هذه الخلايا نادرة في دم البالغين، وتوسيع أعدادها صعب. تصف هذه الدراسة طريقة لزراعة خلايا تي جاما-دلتا في المختبر انطلاقًا من الخلايا الجذعية الجنينية البشرية، مما قد يفتح الباب أمام علاجات مناعية ضد السرطان أكثر سهولة في الوصول.
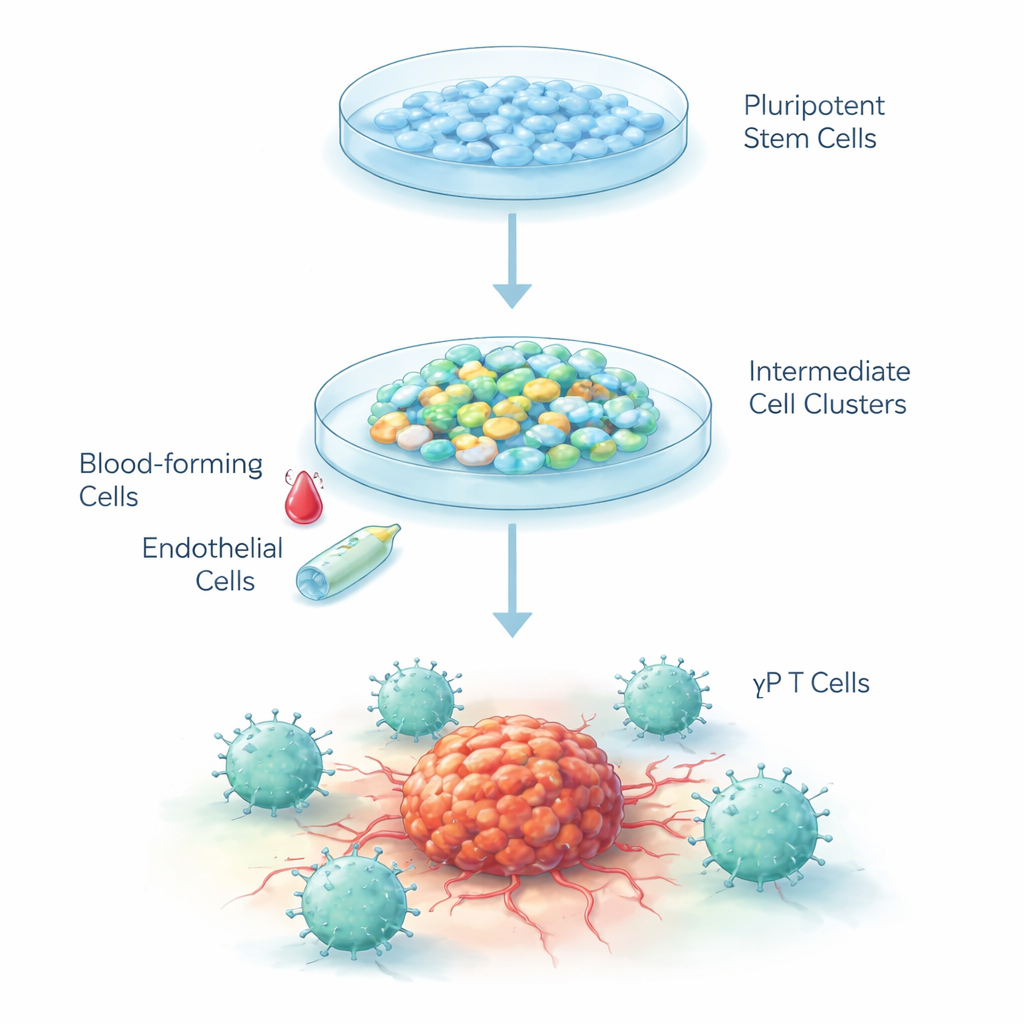
تحويل الخلايا الفارغة إلى مقاتلين ضد السرطان
الخلايا الجذعية الجنينية البشرية خلايا «فارغة» قادرة، من حيث المبدأ، على التحول إلى أي نسيج تقريبًا في الجسم. صمّم الباحثون وصفة خطوة بخطوة لحث هذه الخلايا على التطور على نفس المسار الذي تتبعه في الجنين عندما تتشكل الدم والجهاز المناعي لأول مرة. استخدموا عملية من ثلاث مراحل: توجيه الخلايا أولًا نحو خلايا شبيهة بالأوعية الدموية في المراحل المبكرة، ثم إلى خلايا بدائية مكوّنة للدم غير ناضجة، وأخيرًا إلى خلايا تي من النوع جاما-دلتا. نُميت الخلايا على شكل عناقيد ثلاثية الأبعاد في وسط سائل خاص تحت ظروف أكسجين منخفضة تحاكي الجنين النامي، ثم أعيدت إلى مستويات أكسجين طبيعية أثناء نضوجها.
بناء خط تجميع للخلايا المناعية
في المرحلة الأولى، دفعت الإشارات الكيميائية الخلايا الجذعية للتحول إلى الميزودرم، الطبقة المبكرة التي تنتج الدم والأوعية. خلال ستة أيام، أظهر نحو 40% من الخلايا في كل عنقود علامات «الخلايا البطانية المكوّنة للدم»، نوع من الخلايا الانتقالية القادرة على إعطاء خلايا دموية. في المرحلة الثانية، أدى تغيير عوامل النمو إلى تحفيز هذه الخلايا الشبيهة بالبِطَانة على التحول إلى خلايا بدائية دموية طافية. أكثر من 99% من هذه الخلايا الطافية حملت علامة مبكرة رئيسية للدم، وحوالي 90% عبّرت عن علامة أخرى للخلايا الدموية، مما يشير إلى توليفة نقية بشكل ملحوظ مع قدرة قوية على الاستمرار في مسار تكوين الخلايا المناعية.
الوصول إلى خلايا تي جاما-دلتا
في المرحلة النهائية، زوّد الفريق الخلايا بإشارات معروفة بتشجيع تطور خلايا تي، بما في ذلك بروتين منشط لمسار Notch يحاكي الإشارات الموجودة عادة في الغدة الصعترية (الثيموس). بعد 25 يومًا، نضج أكثر من 40% من الخلايا إلى خلايا تي جاما-دلتا، تم تحديدها بواسطة مستقبلاتها السطحية المميزة وبالملف «السالب المزدوج» (باستثناء علامات CD4 وCD8 الشائعة في معظم خلايا تي الأخرى). والأهم من ذلك أن خلايا تي ألفا-بيتا التقليدية نُتجت بكميات ضئيلة جدًا، مما يظهر أن البروتوكول يفضّل بقوة فرع جاما-دلتا. أظهر التحليل الجيني مع الزمن أن الخلايا شغّلت وأوقفت مجموعات من الجينات بتسلسل منظم يحاكي عن كثب كيفية تشكل الدم وخلايا تي داخل الجسم.
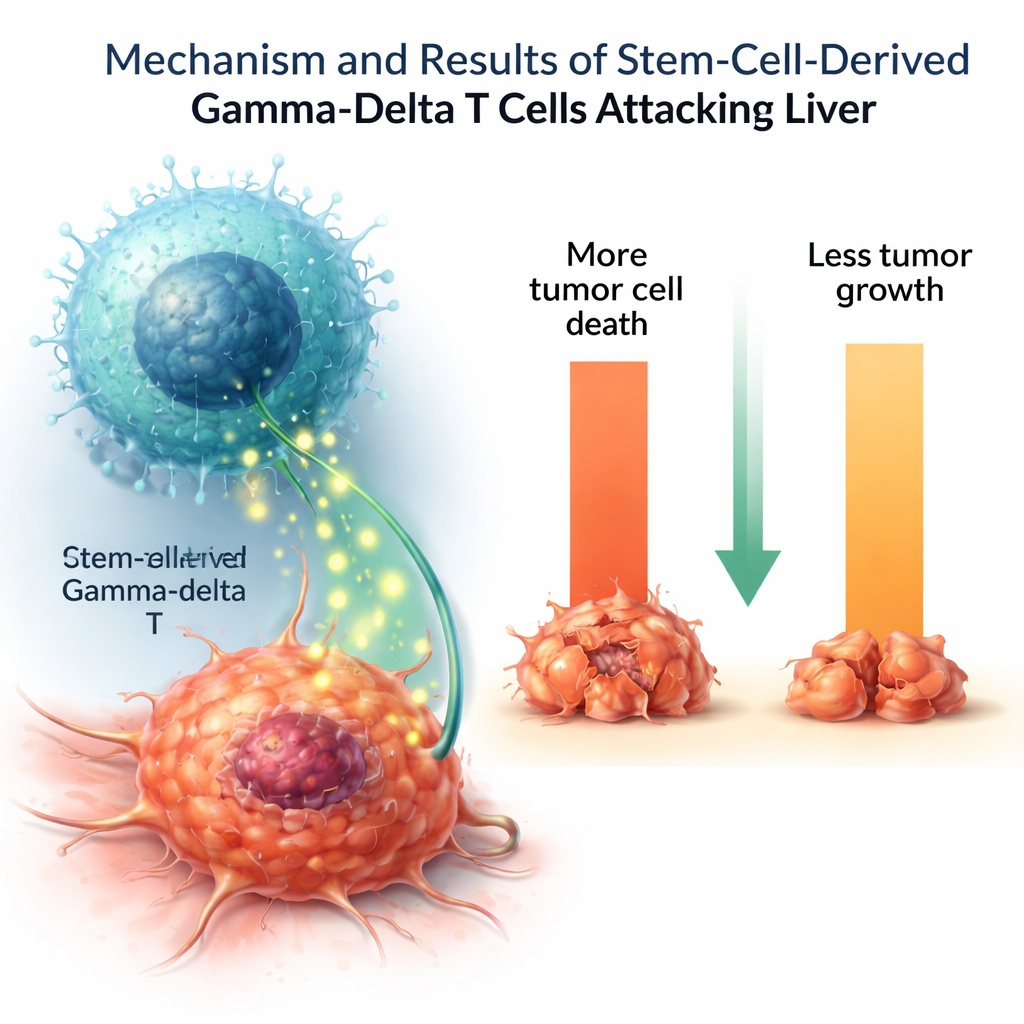
اختبار الخلايا المُجَنّسة مختبريًا
لاختبار ما إذا كانت هذه الخلايا المصنوعة مخبريًا تعمل كمقاتلين حقيقيين للسرطان، عرضها الباحثون لعدة خطوط خلايا أورامية بشرية. قتلت خلايا تي جاما-دلتا نسبة كبيرة من خلايا سرطان الكبد وأبطأت نموها، بينما كان تأثيرها ضئيلًا على الخلايا السليمة الضابطة. عند تحفيزها، أفرزت جزيئات مرسلة مناعية مهمة مثل عامل نخر الورم (TNF) والإنترلوكين-2، التي تساعد في تنسيق وتكبير الهجمات المناعية. بعض جزيئات القتل الأخرى وُجدت بمستويات أدنى مقارنة بخلايا تي جاما-دلتا الطبيعية، مما يوحي بأن الخلايا المزروعة مخبريًا قد لا تكون ناضجة تمامًا أو قد تمثل نوعًا وظيفيًا فرعيًا محددًا.
ماذا قد يعني هذا لرعاية السرطان مستقبلًا
من خلال إعادة إنشاء نسخة مبسطة من تطور الدم المبكر في طبق تجريبي — دون استخدام خلايا مغذية حيوانية — أنتج العلماء أعدادًا كبيرة من خلايا تي جاما-دلتا في أقل من شهر، بسرعة وبساطة أكثر من الطرق السابقة. بينما لا يزال هناك عمل مطلوب لتنقية المزيج النهائي من الخلايا، وتوسيع الإنتاج، وتكييف الوصفة لتوافق شروطًا سريرية معتمدة وخالية من المصل، تشير هذه المقاربة إلى مصدر متجدد لخلايا تي جاما-دلتا موحّدة القياس. إذا ثبتت سلامة وفعالية هذه الخلايا في اختبارات لاحقة، فقد تصبح لبنة متاحة على نطاق واسع للعلاجات المناعية الجاهزة من الجيل القادم ضد سرطانات مثل أورام الكبد.
الاستشهاد: Zhang, X., Chen, C., Fu, Y. et al. Generation of TCRγδ + T cells from human embryonic stem cells. Sci Rep 16, 6762 (2026). https://doi.org/10.1038/s41598-026-37941-w
الكلمات المفتاحية: خلايا تي جاما-دلتا, المناعة المضادة للسرطان, الخلايا الجذعية الجنينية البشرية, تمايز الخلايا, سرطان الكبد