Clear Sky Science · ar
التعرُّف الحاسوبي والوصف الآلي للآلية لمركبات المنتجات الطبيعية المستهدفة لنفق ربط البريْنيل في PDE6D
تحويل مفتاح السرطان المفضل ضِدَّ نفسه
تعتمد العديد من أخطر أنواع السرطان — من البنكرياس إلى القولون والرئتين — على مفتاح جزيئي واحد "مفتوح" يُدعى RAS. عندما يعلّق هذا المفتاح في وضع التشغيل، تنمو الخلايا بلا ضابط. كافح مطوِّرو الأدوية لعقود لإيقاف RAS مباشرة. تستكشف هذه الدراسة تكتيكاً مختلفاً: البحث عن مركبات طبيعية يمكن أن تسد بهدوء بروتين المساعد الذي يحتاجه RAS للوصول إلى موقع عمله، مما قد يخفّف إشارته دون الحاجة إلى استهداف RAS بشكل مباشر. 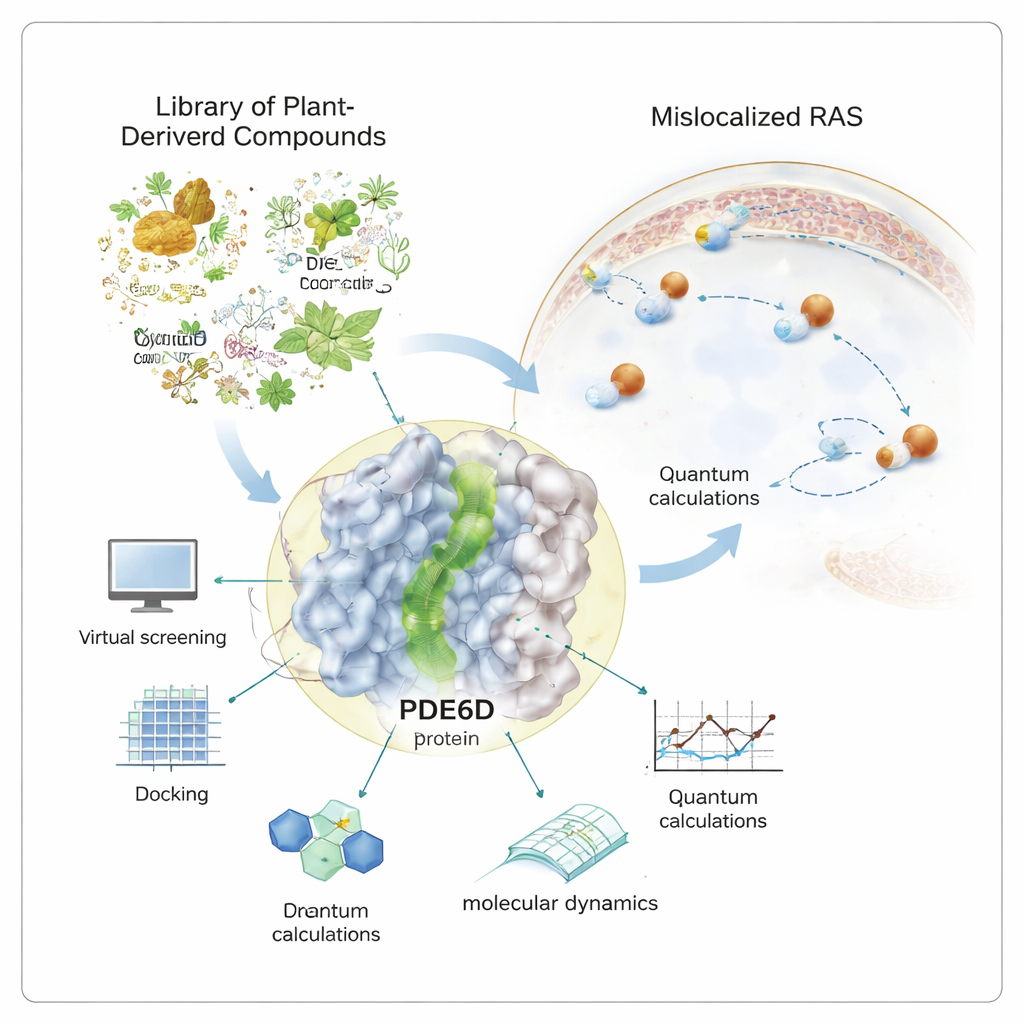
مساعد مخفي داخل خلايا السرطان
يجب أن تجلس بروتينات RAS على السطح الداخلي لغشاء الخلية لإرسال إشارات النمو. للوصول إلى هناك، تحمل ذيلاً دهنيّاً يسمح لها بالالتصاق بالغشاء. يعمل بروتين مرافق يُدعى PDE6D مثل سيارة الأجرة، حيث يحمي هذا الذيل بينما ينتقل RAS عبر وسط الخلية المائي. لدى PDE6D نفقٌ ضيّق مبطّن بالزيت يقبض ذيل RAS. إذا تم سد هذا النفق، فمن المرجح أن ينتهي RAS في المكان الخطأ، مما يضعف قدرته على دفع السرطان. وبما أن العديد من أدوية RAS الحالية تعمل فقط على مجموعة صغيرة من الطفرات، فإن الباحثين حريصون على استكشاف PDE6D كهدف غير مباشر لكنه ذا صلة أوسع.
استخدام الحاسوب للتنقيب في مكتبة الطبيعة الكيميائية
بدلاً من الاعتماد على المواد الكيميائية الصناعية وحدها، لجأ المؤلف إلى مكتبة مُنقَّحة تضم أكثر من ألف منتج طبيعي قابل للشراء — جزيئات مشتقة أصلاً من النباتات والميكروبات ومصادر حية أخرى. استُخدمت أدوات حاسوبية قوية لفحص هذه المكتبة مقابل البنية ثلاثية الأبعاد لـ PDE6D. في هذا الاختبار الافتراضي، سُدِّت كل جزيئة داخل النفق لتُقيَّم مدى ملاءمتها وقوة ارتباطها المحتملة. ثم فُحصت أفضل المرشحين بدقة أكبر باستخدام حسابات على مستوى الكم، التي تستكشف كيف تُرتَّب الإلكترونات في كل جزيء ومدى سهولة مشاركتها في تفاعلات تثبيت داخل جيب البروتين.
اختبار القوة للحالات الواعدة أثناء الحركة
البروتينات والجزيئات الصغيرة لا تبقى ثابتة داخل الخلايا، لذا ذهبت الدراسة أبعد من اللقطات الثابتة. باستخدام محاكاة ديناميكية جزيئية طويلة تتتبع حركة الذرات على مدى نصف ميكروثانية، راقب الباحث كيف تصرف كل مركب طبيعي واعد داخل نفق PDE6D مع مرور الوقت. بقي زوجان من المرشحين، المعلّمان MolPort-039-052-621 وMolPort-002-507-186، مثبتين داخل النفق مع شبكات اتصال مستقرة، بينما انجرف جزيء ثالث نحو مخرج النفق وأصبح ارتباطه أضعف. خرائط تحليلية إضافية أظهرت أي أجزاء من بنية PDE6D كانت مرنة أو هادئة عند الارتباط، وكيف استكشف المُجمَّع "منظور الطاقة" الخاص به — أي الأشكال الأكثر راحة وطول أمد بقاءها. 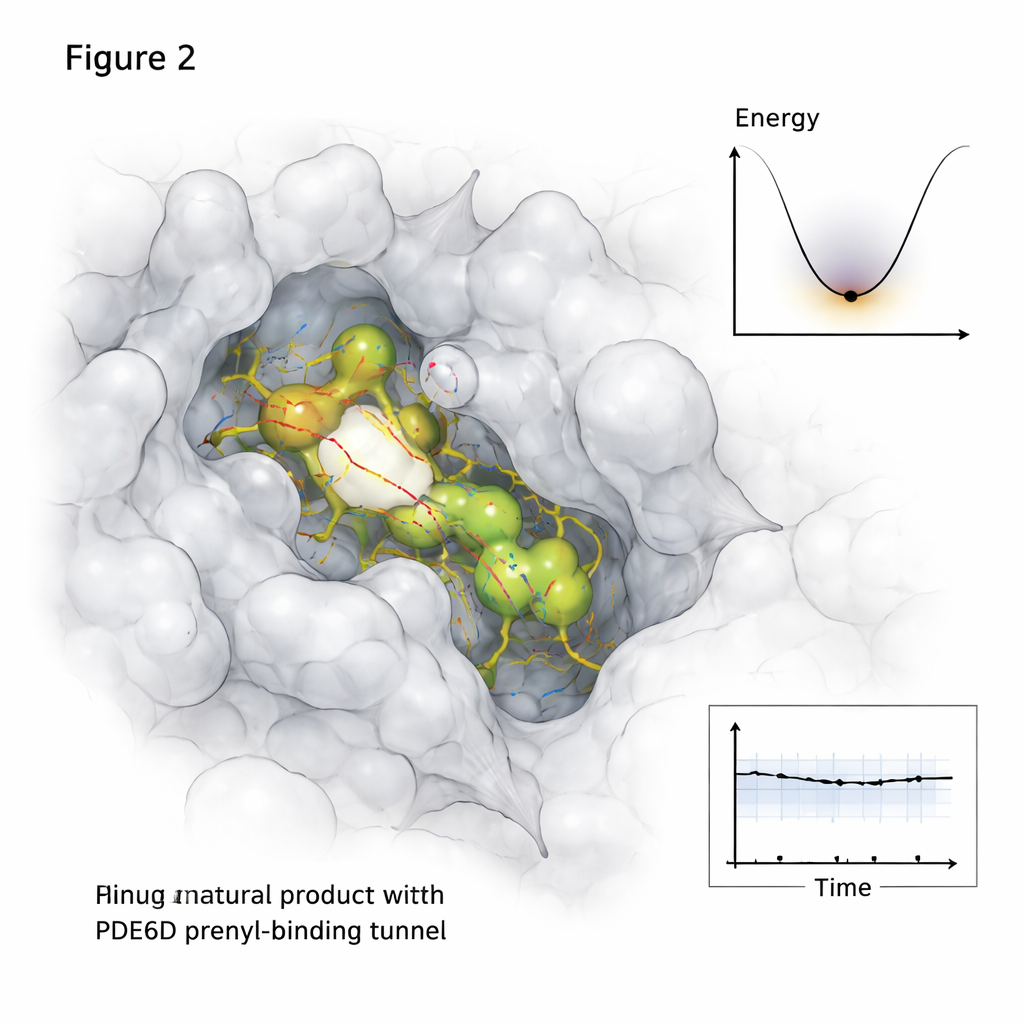
موازنة قوة الارتباط والسلوك المشابه للأدوية
استخدمت الدراسة أيضاً أدوات تنبؤية عبر الإنترنت لتقييم ما إذا كانت هذه المركبات الطبيعية تبدو كنقاط انطلاق واقعية للأدوية. أظهرت القمم الثلاث جميعها سمات كيميائية تتوافق مع "شبه دوائية" أساسية، لكن كلّاً منها حمل علامات حمراء. تكهنت بعض الأدوات بانخفاض الامتصاص أو الذوبان؛ وأشارت أخرى إلى احتمالات سمية محتملة، مثل تأثيرات على نظم النبض القلبي أو على الحمض النووي. هذه المشكلات تعني أن الجزيئات كما هي بعيدة عن أن تكون أدوية جاهزة. وبدلاً من ذلك، من الأفضل اعتبارها قوالب هيكلية قد يعدلها الكيميائيون، محتفظين بميزات ملاءمة النفق مع تقليم الأجزاء المسببة للمشاكل.
ما الذي يعنيه هذا لعلاجات السرطان المستقبلية
بعبارة بسيطة، لا تُقدّم هذه العملُ دواءً جديداً للسرطان، لكنها ترسم مساراً واعداً. من خلال تجميع طبقات عدة من الحسابات — من التثبيت السريع إلى المحاكاة التفصيلية وحسابات الكم — تضيق الدراسة مجموعة ضخمة من الجزيئات الطبيعية إلى مجموعة صغيرة تبدو ملائمة لسد نفق PDE6D. إذا أكدت التجارب المخبرية المستقبلية أن هذه المركبات فعلاً تضلل RAS داخل الخلايا وتبطئ نمو الأورام المدفوعة بـ RAS، فقد تُلهم فئة جديدة من العلاجات التي تستهدف "اللوجستيات" الخاصة بالسرطان بدلاً من مهاجمة العامل الرئيسي مباشرةً.
الاستشهاد: Alshahrani, M.M. Computational identification and mechanistic characterization of natural product binders targeting the PDE6D prenyl binding tunnel. Sci Rep 16, 6571 (2026). https://doi.org/10.1038/s41598-026-37939-4
الكلمات المفتاحية: إشارات RAS, مثبطات PDE6D, منتجات طبيعية, اكتشاف دوائي حاسوبي, علاج السرطان