Clear Sky Science · ar
النشاط المضاد للسرطان للكيركومين المحمّل في نظام هجين من جسيمات السيليكا الوظيفية بالأمين والمطهّمة بالفضة
تحويل بهار المطبخ إلى مقاتل للسرطان أكثر ذكاءً
يحتوي الكركم، البهار الأصفر الزاهي المستخدم في العديد من الكاريّات، على الكركومين — مركب طبيعي يُشاد به منذ زمن لفوائده الصحية، بما في ذلك النشاط المضاد للسرطان. لكنَّ الكركومين بمفرده يذوب بصعوبة في الماء، ويتحلل بسرعة داخل الجسم، ويكافح للوصول إلى الأورام بجرعات فعّالة. تصف هذه الدراسة طريقة جديدة لتغليف الكركومين داخل جسيمات مهندسة دقيقة بحيث يصبح أكثر استقرارًا، وأكثر استهدافًا للأورام، وأكثر قوة ضد خلايا السرطان، مع السعي إلى تقليل الضرر للأنسجة السليمة.
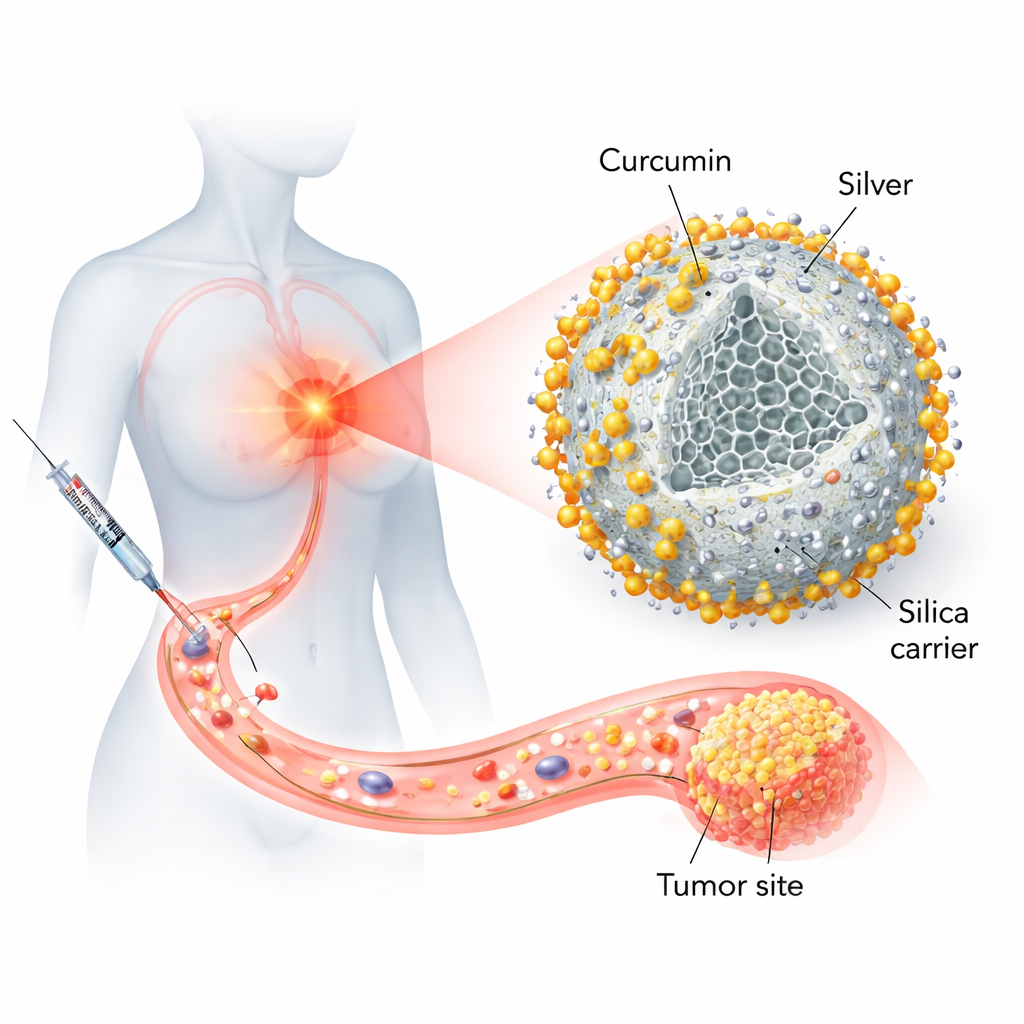
لماذا يحتاج دواء طبيعي واعد إلى ناقل أفضل
يمكن للكركومين تعطيل عمليات متعددة تعتمد عليها خلايا السرطان للنمو والبقاء. ومع ذلك، عند تناول الأشخاص للكركومين، لا يصل معظمُه إلى الورم: فهو يتكتل بدلًا من الذوبان، ويُزال من مجرى الدم بسرعة، ولا يمكن حقنه بجرعات عالية بأمان. حسنت أنظمة التوصيل الموجودة — مثل الجسيمات الدهنية أو الكبسولات البوليمرية — الوضع إلى حد ما، لكنها غالبًا ما تحمل كمية صغيرة فقط من الدواء، أو قد تكون غير مستقرة، أو تتطلب تصنيعًا معقدًا. في الوقت نفسه، تُعرف الجسيمات النانوية الفضية بأنها تُسبب ضررًا للبكتيريا وخلايا السرطان عبر توليد جزيئات تفاعلية داخلها، إلا أنها أيضًا قد تكون غير مستقرة وأحيانًا سامة. سعى الباحثون لدمج هذين العاملين — الكركومين والفضة — داخل غلاف من السيليكا مصمّم بعناية ليُثبّت كلا المكوّنَين ويطلق الدواء حيث يكون مطلوبًا أكثر.
بناء حاملات دقيقة من الرمل والفضة والكركومين
ابتكر الفريق أولًا جسيمات نانوية من السيليكا — كرات على مقياس النانومتر مصنوعة من نفس المادة الأساسية كالرمح — باستخدام طريقة مائية تُكوّن جُسيمات متجانسة ومساميَّة. ثم زَيَّنوا السطح بمجموعات أمين، خطاطيف كيميائية تُحسّن ارتباط أيونات الفضة والكركومين على حد سواء. أُدخلت الفضة بحيث ترتبط بقوة بهذه الأمينات لتُشكّل إطارًا هجينًا من الفضة والسيليكا. أخيرًا، حُمّل الكركومين المستخرج من جذور الكركم إلى هذا الهيكل من محلول كحولي. كانت الجسيمات الناتجة، المسماة CUR@Ag-AFS، تحمل كمية مرتفعة نسبيًا من الدواء مع بقاءها صلبة ومتجانسة. أكدت سلسلة من تقنيات المختبر أن الجسيمات كروية، وأن العناصر السيليكون والأكسجين والنيتروجين والكربون والفضة كلها موجودة، وأن الكركومين مدمج في شكل أكثر عدم انتظام واستقرارًا بدلًا من أن يكون في هيئة بلورات هشة.
مصممة لإطلاق المزيد من الدواء داخل الأورام
لاختبار سلوك الحاملات الجديدة في بيئات مختلفة، وضع الباحثون هذه الحاملات في سوائل تحاكي الدم والأنسجة الطبيعية (قريبة من الحموضة المتعادلة) مقابل المحيط الأكثر حموضة النموذجي للأورام ومقسّمات خلايا السرطان. على مدى 24 ساعة، أطلقت الجسيمات الكركومين ببطء وبثبات، لكن مع اعتماد واضح على قيمة الحموضة: أفرجت عن معظم الدواء — أكثر من 90 في المئة من حمولتها — تحت ظروف حمضية مشابهة لتلك داخل خلايا الورم، وبمعدل أقل بكثير في الظروف المتعادلة. أظهر التحليل الرياضي لبيانات الإفراز أن الكركومين ينتشر أساسًا عبر مسام السيليكا، مع إضعاف الحموضة لجذب الكركومين إلى سطح الجسيم. عمليًا، يعني هذا أن النظام مُعدّ ليبقى هادئًا نسبيًا في الأنسجة السليمة لكنه يصبح نشطًا بدرجة أكبر في الأنسجة السرطانية، مما قد يقلل الآثار الجانبية مع الحفاظ على تأثير موضعي قوي.
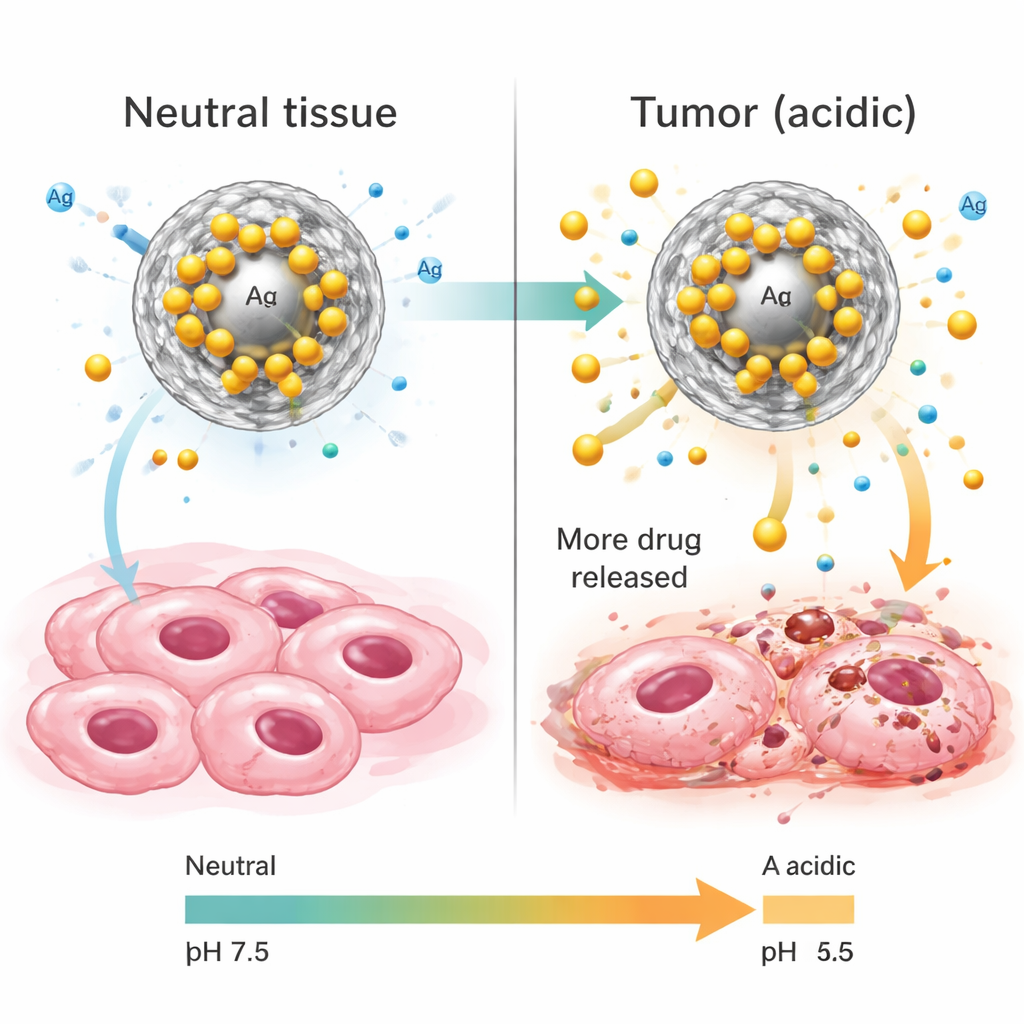
اختبار الجسيمات ضد خلايا السرطان
عرض الفريق بعد ذلك خلايا سرطان الثدي البشرية (MCF-7) لتراكيبات مختلفة: سيليكا خالصة، سيليكا مع مجموعات أمين، سيليكا مع الفضة، كركومين حر، والجسيمات الهجينة CUR@Ag-AFS. قاسوا بقاء الخلايا بعد العلاج باستخدام اختبار تغيير اللون القياسي الذي يعكس النشاط الأيضي. من بين جميع أنظمة الجسيمات النانوية، كان الهجين المكوَّن من الكركومين والفضة والسيليكا الأكثر فعالية في قتل خلايا السرطان، ثانيًا فقط بعد دوكسوروبيسين، دواء العلاج الكيميائي التقليدي المستخدم كعنصر ضابط إيجابي. حققت الجسيمات الهجينة نفس مستوى موت خلايا السرطان بتركيزات أقل بكثير من الكركومين الحر أو الجسيمات المحتوية على الفضة بمفردها، مما يشير إلى تأثير تآزري. ومن المهم أن إطار السيليكا نفسه أظهر سمية منخفضة نسبيًا، مما يدل على أن معظم الفعالية المضادة للسرطان جاءت من مزيج الكركومين والفضة وطريقة توصيلهما.
ماذا يمكن أن يعني هذا لرعاية السرطان في المستقبل
بعبارات مبسطة، بنى الباحثون نوعًا من الإسفنجة المجهرية الذكية من السيليكا تمتص الكركومين والفضة، تحميهما أثناء الدوران في الجسم، ثم تطلقهما بشكل أسرع عند وصولهما إلى البيئة الحمضية للورم. يعزّز هذا التصميم قدرة الكركومين على قتل السرطان ويساعد في توجيهه مباشرة إلى الخلايا المريضة، بينما تضيف بنية السيليكا الاستقرار والتحكم. وعلى الرغم من أن هذا العمل أُجري في المختبر وعلى مزروعات خلوية — وليس بعد في حيوانات أو مرضى — فإنه يشير إلى مستقبل يمكن أن تساهم فيه مركبات طبيعية مثل الكركومين، مقترنة بمواد نانوية مهندسة بعناية، في علاجات سرطانية أكثر استهدافًا، أطول أمداً، وربما أقل ضررًا لبقية الجسم.
الاستشهاد: Shafqat, S.S., Wakeel, M., Zubair, M. et al. Anticancer activity of curcumin loaded hybrid system of silver-amine functionalized silica nanoparticles. Sci Rep 16, 7026 (2026). https://doi.org/10.1038/s41598-026-37829-9
الكلمات المفتاحية: جسيمات نانوية من الكركم, العلاج المستهدف للسرطان, حاملات نانوية فضية, توصيل دوائي مستجيب لدرجة الحموضة, خلايا سرطان الثدي