Clear Sky Science · ar
تثبيط SIRT3 لتقدّم سرطان الكلى عبر تنظيم أستلة IDH2
لماذا تهم هذه الدراسة عن سرطان الكلى
سرطان الكلى، لا سيما نوع يسمى سرطان الخلايا الكلوية، يزداد شيوعًا وغالبًا ما يكون صعب العلاج عندما ينتشر. تبحث هذه الدراسة في آليات داخل خلايا السرطان لتبين كيف تساعد تغييرات دقيقة في مصانع الطاقة داخل الخلية، الميتوكوندريا، على نمو الأورام — وكيف قد يساعد مركب نباتي طبيعي، الهونوكول، في إبطاء ذلك. للقراء، تمنح الدراسة لمحة عن كيفية أن فهم «صيانة» الخلية قد يفتح خيارات جديدة تتجاوز الأدوية الحالية.
فرامل خفية داخل خلايا الكلى
تدير خلايانا باستمرار إنتاج الطاقة والنواتج الضارة. في خلايا الكلى السليمة، يعمل بروتين يُدعى SIRT3 كمشرف صيانة داخل الميتوكوندريا، يحافظ على عمل البروتينات الأخرى بشكل صحيح. فحص المؤلفون قواعد بيانات سرطانية عامة واسعة وعينات نسيجية من مرضى، ووجدوا أن مستويات SIRT3 كانت أقل باستمرار في أورام الكلى مقارنة بالنسيج السليم المجاور. الأورام التي انخفضت فيها مستويات SIRT3 أبدت أنماط جينية مرتبطة بنمو أسرع وقدرة أكبر على الحركة، مما يشير إلى أنه عندما تُفقد هذه الفرملة الخلوية، تصبح خلايا السرطان أكثر عدوانية.
كيف تحوّل خلايا السرطان توازن طاقتها
لاختبار ما إذا كان فقدان SIRT3 يدفع فعلاً سلوك السرطان، قلل الباحثون من مستوى SIRT3 في خطوط خلايا سرطان الكلى المزروعة مخبريًا. الخلايا التي كان فيها SIRT3 أقل تكاثرت بشكل أسرع وكونت مستعمرات أكثر، وهو علامة على بقاء ونمو معززين. عندما زُرعت هذه الخلايا المعدلة في الفئران، كانت الأورام الناتجة أكبر وأثقل من أورام الخلايا الضابطة. تُظهر هذه التجارب مجتمعة أن SIRT3 ليس مجرد بروتين مفقود في سرطان الكلى، بل يقيّد نمو الورم فعليًا عندما يكون موجودًا.
إنزيم رئيسي ومشكلة «التأكسد» داخل الخلايا
ركز الفريق بعد ذلك على بروتين ميتوكوندري آخر، IDH2، الذي يساعد في إنتاج NADPH، جزيء يغذي أنظمة تدير جزيئات الأكسجين التفاعلية (ROS)—مواد ضارة تشبه «الصدأ» الخلوي. يمكن أن يتغير سلوك IDH2 بوضع علامة كيميائية صغيرة تسمى مجموعة الأستيل. يُعرف عن SIRT3 أنه يزيل مثل هذه العلامات. في خلايا سرطان الكلى، ارتبط SIRT3 فعليًا بـIDH2 ونزع مجموعات الأستيل عند موقع محدد (K413). عندما انخفض SIRT3، تراكمت هذه العلامة الأستيلية، وقلَّت كفاءة IDH2، نزلت مستويات NADPH، وارتفعت مستويات ROS. فقدت الميتوكوندريا جزءًا من فرق الجهد الغشائي، علامة على ضعف الوظيفة. باستخدام نسخ معدّلة من IDH2 تحاكي الحالة الأستيلية أو غير الأستيلية، أظهر المؤلفون أن الشكل الأستيلاتي قد يلغي تأثير SIRT3 المبطئ للنمو، رابطين فرملة الورم مباشرة بهذه النقلة الكيميائية المفردة.
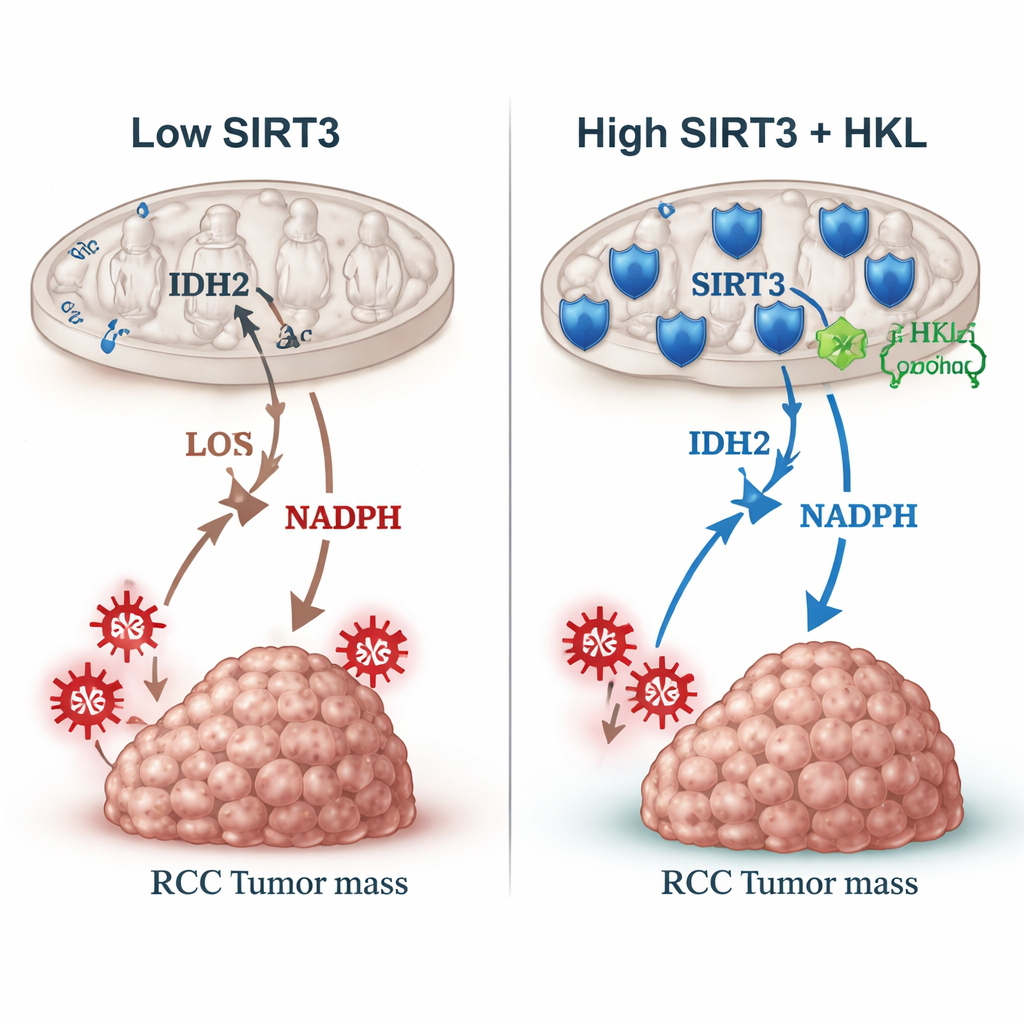
إعادة تفعيل الفرملة بمركب نباتي
نظرًا لأن SIRT3 يبدو واقيًا، تساءل المؤلفون عما إذا كان يمكن تعزيز مستوياته بعلاج دوائي. اختبروا الهونوكول، جزيء طبيعي مستخلص من لحاء شجرة الماغنوليا ومعروف بالفعل بتأثيره على مسارات سرطانية متعددة. بجرعة مُختارة بعناية لم تؤدِ إلى قتل الخلايا مباشرة، زاد الهونوكول مستويات SIRT3 مع الزمن في خلايا سرطان الكلى، جنبًا إلى جنب مع منظميْن مرتبطين (p-AMPK وPGC-1α). مع ارتفاع SIRT3، فقد IDH2 علامة الأستيل، انخفضت مستويات ROS، وتباطأ نمو الخلايا وتشكيل المستعمرات. عندما جُمِع الهونوكول مع سونيتينيب، دواء قياسي لسرطان الكلى، كبح الزوجان النمو أكثر من سونيتينيب وحده، جزئيًا عن طريق تخفيف فائض ROS الذي قد يسببه السونيتينيب نفسه. لوحظت تأثيرات مماثلة عند استخدام مضاد أكسدة تقليدي، ما يدعم الفكرة أن ضبط الإجهاد التأكسدي يمكن أن يجعل العلاجات الحالية تعمل بشكل أفضل.
ماذا قد يعني هذا للعلاجات المستقبلية
للغير متخصصين، الخلاصة هي أن هذه الدراسة تحدد SIRT3 كفرملة طبيعية للورم في سرطان الكلى، تعمل عبر تحكم دقيق في IDH2 والتوازن بين الجزيئات الوقائية والضارة داخل الميتوكوندريا. عندما يكون SIRT3 منخفضًا، تتراكم ROS المسببة للضرر وتكتسب الخلايا ميزة نمو. قد يؤدي استعادة نشاط SIRT3 — ربما عبر الهونوكول أو أدوية أكثر دقة في المستقبل — إلى إبطاء نمو الورم ومساعدة العلاجات الحالية على الأداء بشكل أفضل. رغم أن الهونوكول نفسه لا تزال تواجه عقبات، بما في ذلك كيفية امتصاصه وتعدد أهدافه، فإن العمل يشير إلى مسار واضح، محور SIRT3–IDH2–الأحوال التأكسدية، الذي يمكن لمطوري الأدوية استهدافه لتصميم علاجات مستقبلية تراعي أيض سرطان الخلايا الكلوية.
الاستشهاد: Li, L., Tian, Y., Chen, S. et al. SIRT3 suppresses renal cancer progression by regulating IDH2 acetylation. Sci Rep 16, 7619 (2026). https://doi.org/10.1038/s41598-026-37783-6
الكلمات المفتاحية: سرطان الكلية, SIRT3, الميتوكوندريا, الإجهاد التأكسدي, هونوكول