Clear Sky Science · ar
الاستهداف التآزري لمحور ARID2–MYC بواسطة بوماليدومايد وبانوبينوستات يتغلب على المقاومة الجوهرية لمضادات IMiD في الورم النخاعي المتعدد
لماذا يهم هذا البحث المرضى
الورم النخاعي المتعدد هو نوع من السرطان يصيب الخلايا المنتجة للأجسام المضادة في نخاع العظم، وقد أصبحت علاجاته أفضل خلال السنوات الأخيرة ولكن نادرة هي حالات الشفاء التام. كثير من المرضى يتوقفون في نهاية المطاف عن الاستجابة للأدوية القياسية، مما يترك للأطباء خيارات محدودة. تستكشف هذه الدراسة سبب قدرة الجمع بين نوعين موجودين من الأدوية — ما يُسمى IMiDs مثل بوماليدومايد والأدوية التي تؤثر على تغليف الحمض النووي مثل مثبطات ناقل الأسيتيل الهيستوني (HDAC) كالبانوبينوستات — على العمل سوياً لقتل خلايا المييلوم حتى عندما يكون السرطان مقاوماً لمضادات IMiD وحدها. فهم هذا التآزر على المستوى الجزيئي قد يوجِّه تركيبات علاجية أفضل ويساعد المزيد من المرضى على الاستفادة من أدوية متاحة بالفعل.
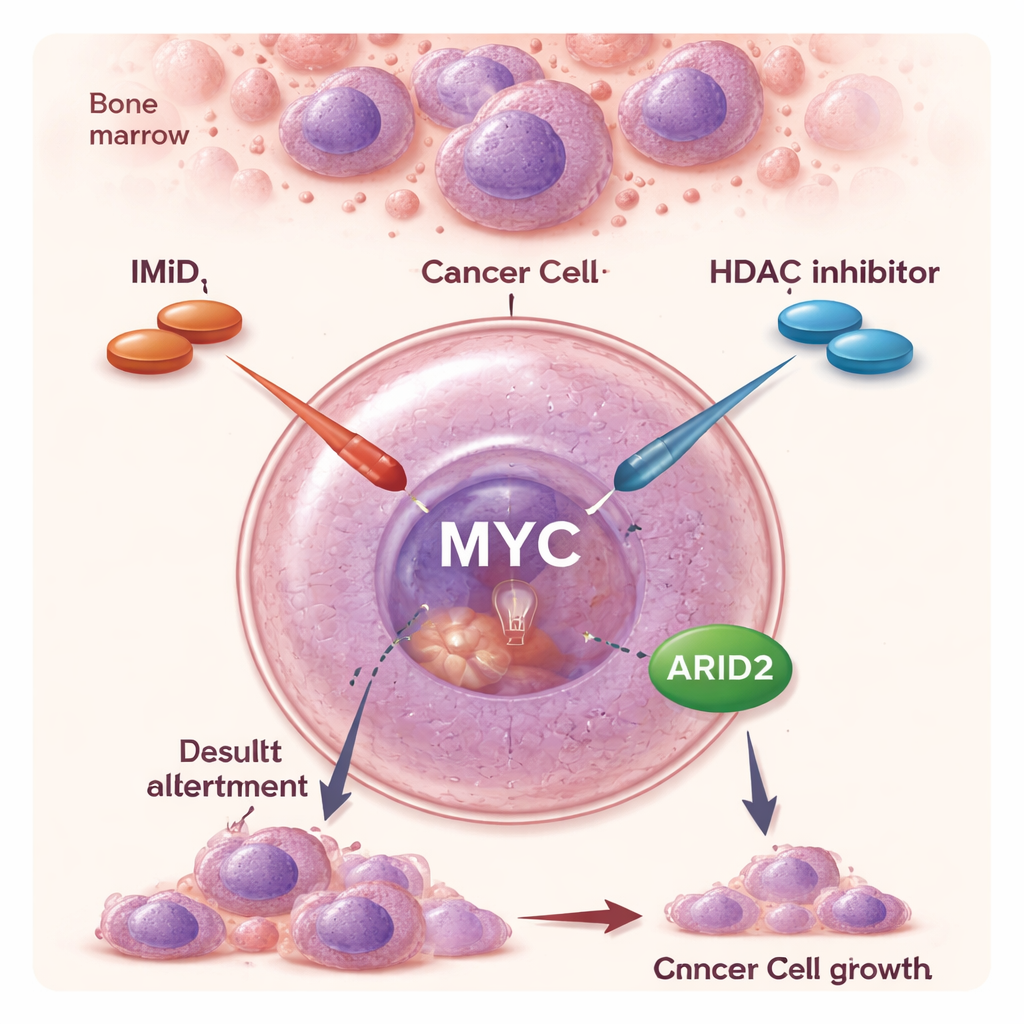
فئتان علاجيتان قديمتان، شراكة جديدة
خلال العقدين الماضيين، وسّعت IMiDs وأدوية مستهدفة أخرى بشكل كبير من متوسط العمر للأشخاص المصابين بالورم النخاعي المتعدد. تعمل IMiDs بطريقة غير تقليدية: بدلًا من مجرد حجب بروتين، تتسبب في تمييز بروتينات معينة للتدمير، مما يؤدي فعلياً إلى إزالتها من الخلية. بذلك تضعف إشارات البقاء الأساسية التي تعتمد عليها خلايا المييلوم. تعمل مثبطات HDAC مثل بانوبينوستات بطريقة مختلفة: فهي تُرخي التغليف الضيق للحمض النووي وتُعيد تشكيل نمط تشغيل الجينات على نطاق واسع. كمستحضرات منفردة، تُظهر مثبطات HDAC تأثيرات متواضعة وقد تسبب آثاراً جانبية، لكن تجارب سريرية ألمحت إلى أن إقرانها مع IMiDs ينتج استجابة مضادة للسرطان أقوى بكثير، بما في ذلك في مرضى لم تعد أمراضهم تستجيب لمضادات IMiD بمفردها. ومع ذلك، ظل السبب الجزيئي لهذا التآزر غامضاً.
نقطة ضغط مشتركة: كبح MYC
اختبر الباحثون منهجياً تراكيبات من عدة IMiDs مع مثبطات HDAC مختلفة عبر مجموعة من خطوط خلايا المييلوم، مستخدمين نظام تسجيل موحّد لقياس مدى قوة التأثيرات التآزرية مقارنة بكل دواء على حدة. وجدوا أن بوماليدومايد مع بانوبينوستات أظهرتا تآزراً قوياً بشكل خاص في معظم النماذج الخلوية، وأن هذا التأثير اعتمد على بروتين يُدعى سِيريبلون (cereblon)، الذي تستخدمه IMiDs لاستهداف «ضحايا» البروتين للتدمير. من خلال تحليل النشاط الجيني الشامل، اكتشفت المجموعة أن بانوبينوستات ومثبط HDAC واسع التأثير ذي صلة يخفضان بقوة تعبير MYC، وهو جين رئيسي للنمو يُوصف غالباً بأنه «محرك الأورم» في الخلايا السرطانية، وأن IMiDs تضيف ضغوطاً إضافية على نفس النقطة. عندما أجبر العلماء خلايا المييلوم على الاستمرار في إنتاج MYC من مصدر غير حساس للأدوية، تلاشى التأثير القوي لزوج الأدوية إلى حد كبير، مما يبيّن أن كبح MYC مركزي لتعاونهما.
كسر المقاومة عبر طريق بديل
بعض خلايا المييلوم مقاومة بطبيعتها لمضادات IMiD: على الرغم من أن الأهداف المبكرة المتوقعة تُدمر، فإن MYC وإشارات البقاء الأخرى لا تُطمس بشكل مناسب، فيستمر نمو الخلايا. في أحد نماذج المقاومة هذه، كان المسار القياسي للـIMiD الذي يربط الأهداف المبكرة بـMYC «غير موصول». تساءل الفريق عما إذا كان طريق بديل قد يربط IMiDs بـMYC. ركزوا على ARID2، مكوّن من آلة إعادة تشكيل الحمض النووي الكبيرة المعروفة بمجمع SWI/SNF. أظهرت أعمال سابقة أن بوماليدومايد يمكن أن يؤشر ARID2 للتدمير وأن هذا يساعد على خفض MYC. في الخلايا المقاومة، قلل بوماليدومايد وحده ARID2 بشكل معتدل فقط، جزئياً لأن الخلية زادت إنتاج ARID2 استجابة لذلك. عند إضافة بانوبينوستات، كبتت الجين ARID2 نفسه، متجاوزة حلقة التغذية الراجعة هذه. معاً خفض الدواءان بروتين ARID2 ثم MYC بشكل قوي، مما أدى إلى قتل فعّال لخلايا السرطان حتى في خطوط مقاومة لـIMiD.
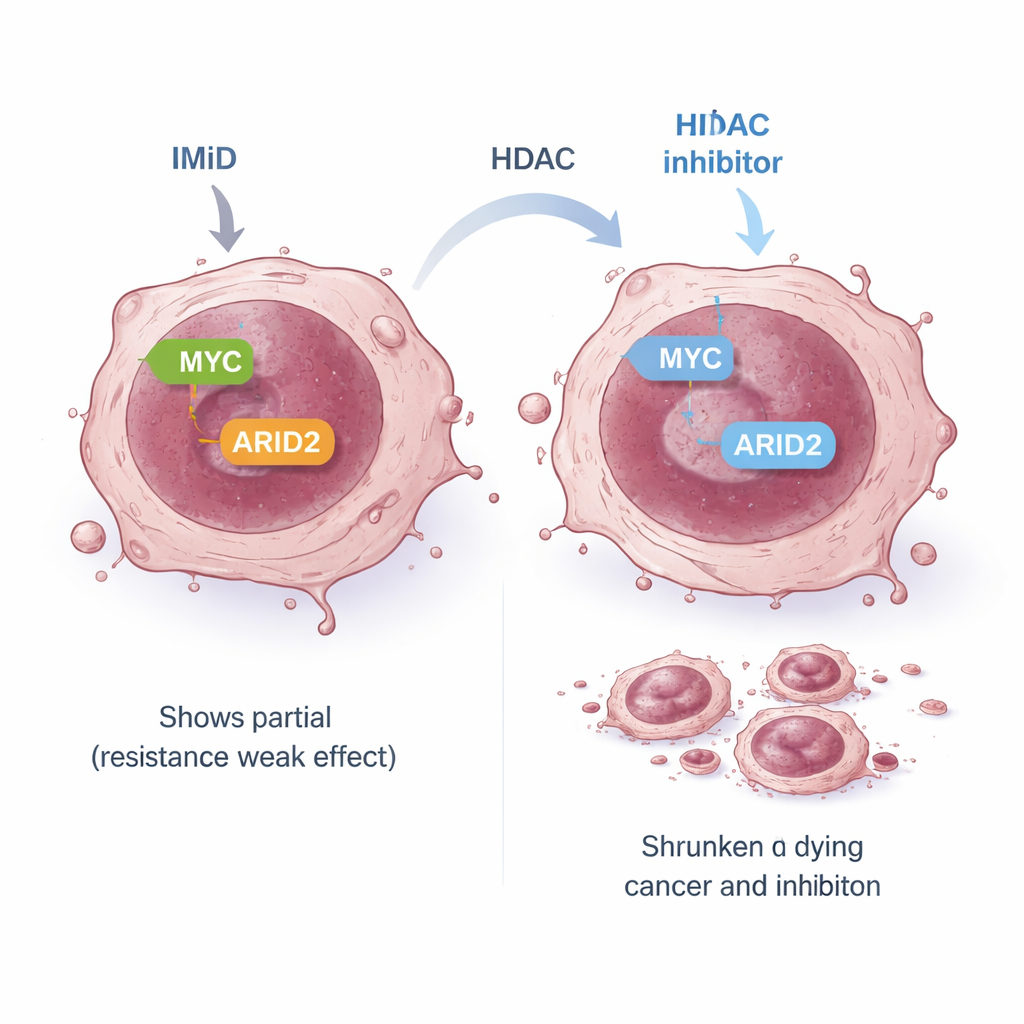
الكشف عن نقطة ضعف أوسع في الخلايا السرطانية
بما أن ARID2 عضو واحد فقط في مجمع SWI/SNF، تساءل المؤلفون عما إذا كان المجمع بأكمله قد يكون نقطة ضعف علاجية. وجدوا أن مثبطات HDAC تُخفض مستويات عدة مكوّنات من SWI/SNF، وأن دواء صغير مستقل مصمم لعرقلة محركات القلب للمجمع (BRG1/BRM) يمكنه وحده إبطاء نمو خلايا المييلوم وتقليل MYC. والأهم من ذلك، أن هذا المثبط لمجمع SWI/SNF عمل أيضاً بتآزر مع كل من بوماليدومايد وبانوبينوستات، وأن تركيبة ثلاثية دفعت ARID2 وMYC إلى انخفاض أكبر مع كبح قوي لتكاثر الخلايا. من خلال استقصاء أي إنزيمات HDAC محددة متورطة، أبرز الباحثون HDAC1 كلاعب رئيسي يساعد في الحفاظ على مسار ARID2–MYC، بينما يبدو أن HDACات أخرى تؤثر على MYC عبر مسارات موازية.
ما الذي يعنيه هذا لعلاج المييلوم في المستقبل
للغير متخصصين، الرسالة المركزية هي أن خلايا المييلوم تبدو معتمدة على «محور تحكم بالنمو» مشترك يتمحور حول MYC، وأن هناك أكثر من طريق يؤدي إلى ذلك المحور. العلاج القياسي بـIMiD يضرب عادة طريقاً واحداً؛ في بعض الأورام المقاومة، يكون ذلك الطريق مسدوداً، فيبقى MYC نشطاً. تظهر هذه الدراسة أن طريقاً بديلاً — يمر عبر ARID2 ومجمع SWI/SNF — يبقى مفتوحاً، وأن استخدام بانوبينوستات إلى جانب بوماليدومايد يمكن أن يُغلقه. من خلال الجمع المتعمد لأدوية تضغط على MYC من اتجاهات متعددة، قد يتمكن الأطباء من التغلب على بعض أشكال المقاومة الفطرية للأدوية مع احتمال استخدام جرعات أقل من كل دواء. رغم أن هناك حاجة لمزيد من الأعمال قبل السريرية والسريرية، فإن النتائج تقدم مخططاً أوضح لتصميم تراكيبات قائمة على الآلية لمرضى الورم النخاعي المتعدد صعب العلاج.
الاستشهاد: Yamamoto, J., Asatsuma-Okumura, T., Ito, T. et al. Synergistic targeting of the ARID2–MYC axis by pomalidomide and panobinostat overcomes intrinsic IMiD resistance in multiple myeloma. Sci Rep 16, 7375 (2026). https://doi.org/10.1038/s41598-026-37740-3
الكلمات المفتاحية: الورم النخاعي المتعدد, مقاومة للأدوية, بوماليدومايد, بانوبينوستات, MYC