Clear Sky Science · ar
AT-101 يثبط تكاثر وغزو خلايا سرطانة اللسان الحرشفية عن طريق استهداف محور miR-21-5p/FDX1
لماذا تهم هذه الدراسة حول سرطان اللسان
يمكن أن يؤثر سرطان اللسان بشكل كبير على الأنشطة اليومية مثل الكلام والأكل والبلع، والعلاجات الحالية غالبًا ما تضر بهذه الوظائف مع استمرار فشلها أحيانًا في السيطرة التامة على المرض. تستكشف هذه الدراسة مركبًا مشتقًا من نبات، AT-101، وتكشف كيف يمكنه إبطاء نمو وانتشار سرطانة الخلايا الحرشفية للسان في نماذج مخبرية. من خلال فك شفرة مفتاح تحكم وراثي صغير داخل خلايا الورم، يشير الباحثون إلى طريقة جديدة وأكثر استهدافًا لعلاج هذا السرطان الصعب.
مشكلة الرعاية الحالية لسرطان اللسان
سرطانة الخلايا الحرشفية في اللسان هي من أكثر أشكال سرطان الفم شيوعًا وعدوانية. لأن اللسان أساسي للكلام والمضغ، يتوجب على الجراحين الموازنة بين إزالة كمية كافية من النسيج الورمي والحفاظ على الوظيفة، وحتى بعد ذلك يواجه العديد من المرضى تكرارًا محليًا وانتشارًا إلى العقد اللمفاوية. يمكن أن تكون الكيمياء العلاجية القياسية سامة وتفقد فعاليتها مع تطور مقاومة الأورام. دفعت هذه القيود البحث عن علاجات تعمل بدقة أكبر على الآليات الجزيئية التي تسمح لخلايا سرطان اللسان بالنمو والحركة وغزو الأنسجة المحيطة.
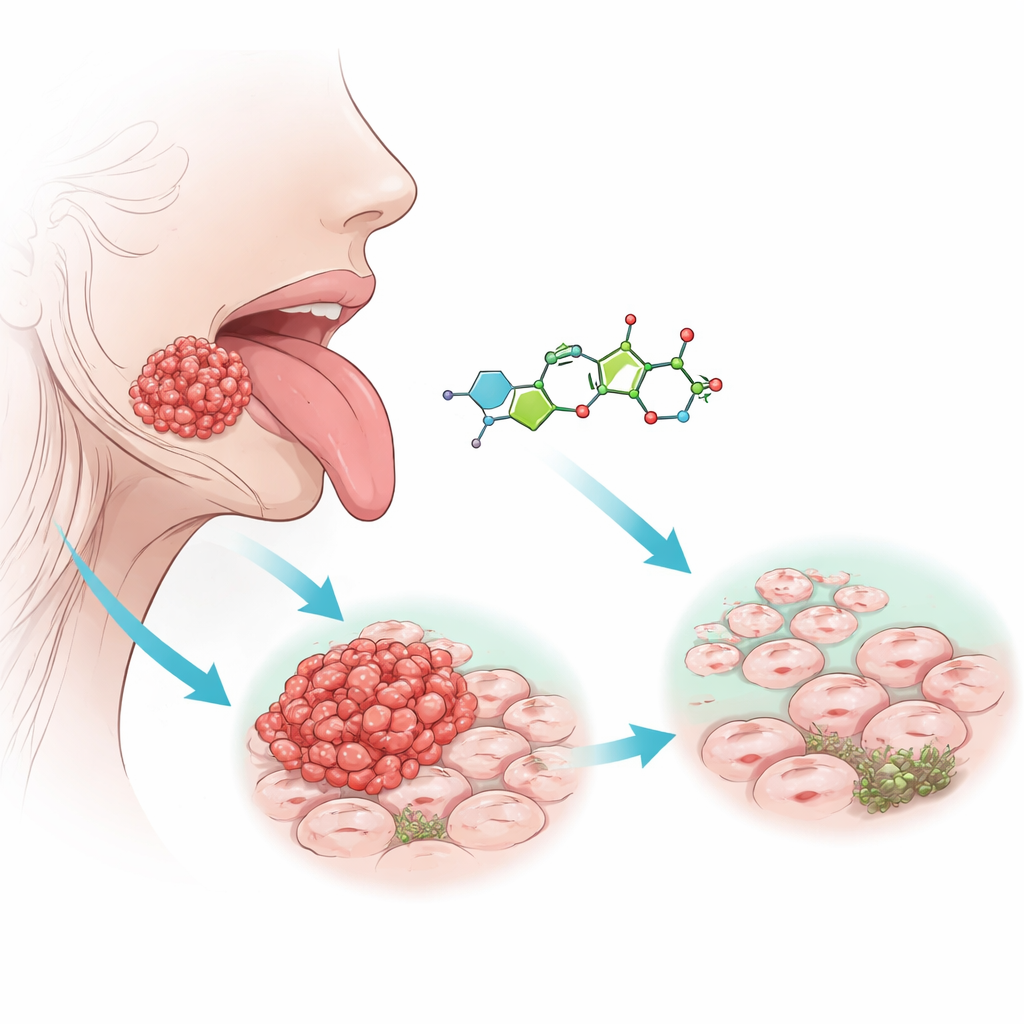
مفتاح RNA صغير وبروتين وقائي
ركز الفريق على جزيئات تنظيمية صغيرة تُدعى الميكروRNA، التي تعمل كعصي تعتيم لنشاط الجينات. أحدها، miR-21-5p، معروف بأنه يتصرف كدعسة تسريع في كثير من السرطانات، دافعا الخلايا للنمو ومقاومة موت الخلية. باستخدام قواعد بيانات جينية عامة متعددة وتجارب في خطوط خلايا سرطان اللسان وعينات مرضى، وجد الباحثون أن مستويات miR-21-5p مرتفعة بشدة في أورام اللسان، بينما ينخفض بروتين يسمى FDX1 بشكل ملحوظ. يساعد FDX1 في الحفاظ على استقلاب خلوي سليم داخل الميتوكوندريا، مراكز طاقة الخلية، ويبدو أنه يعمل كفرامل على السلوك السرطاني. كلما زاد إنتاج الخلايا لـ miR-21-5p، قل لديها من FDX1، كاشفًا عن محور تحكم مرتبط ارتباطًا وثيقًا.
إثبات علاقة التشغيل والإيقاف في الخلايا والأورام
في خلايا سرطان اللسان المزرعة، أدى رفع miR-21-5p إلى تكاثر الخلايا بشكل أسرع وزيادة حركتها وغزوها، بينما أدى خفضه إلى العكس. أظهر الباحثون أن miR-21-5p يمكنه الارتباط مباشرة بالرسالة الوراثية التي تشفر FDX1 وبالتالي إيقاف إنتاجه. عندما قلّ مستوى FDX1 نفسه، قلدت الخلايا السلوكات العدوانية المرصودة مع ارتفاع miR-21-5p؛ وعندما أعيد FDX1، تبطّأ نمو الخلايا، وحركتها أقل، وغزت عبر الأغشية الاصطناعية أقل. في فئران زُرعت فيها خلايا سرطان لسان بشرية، أدى تعزيز FDX1 إلى أورام أصغر وبها خلايا أكثر ميتة، بينما أدى إسكات FDX1 إلى أورام أكبر وأكثر نشاطًا، مما يؤكد دوره الوقائي.
مركب مشتق من القطن يعيد توصيل المحور
AT-101 هو شكل مُنقَّى من الجوسيبول، مادة طبيعية من نباتات القطن درست سابقًا لقدرتها على دفع الخلايا السرطانية نحو الانتحار الخلوي. اكتشف المؤلفون أن AT-101 يخفض مستويات miR-21-5p في خلايا سرطان اللسان بينما يستعيد FDX1. عند جرعات مختارة بعناية، قلل AT-101 بشدة من نمو الخلايا السرطانية وهجرتها وغزوها، لكن كانت آثاره أخف بكثير على الخلايا الفموية الطبيعية. عندما رُفع miR-21-5p اصطناعيًا، استطاع جزئيًا إنقاذ الخلايا السرطانية من تأثيرات AT-101 المثبطة للنمو، بينما عزز حجب miR-21-5p تأثير الدواء. بالمقابل، أخفّ إزالة FDX1 من فوائد AT-101، مما يوحي بأن المركب يعمل إلى حد كبير عن طريق تحرير FDX1 من قمع miR-21-5p.
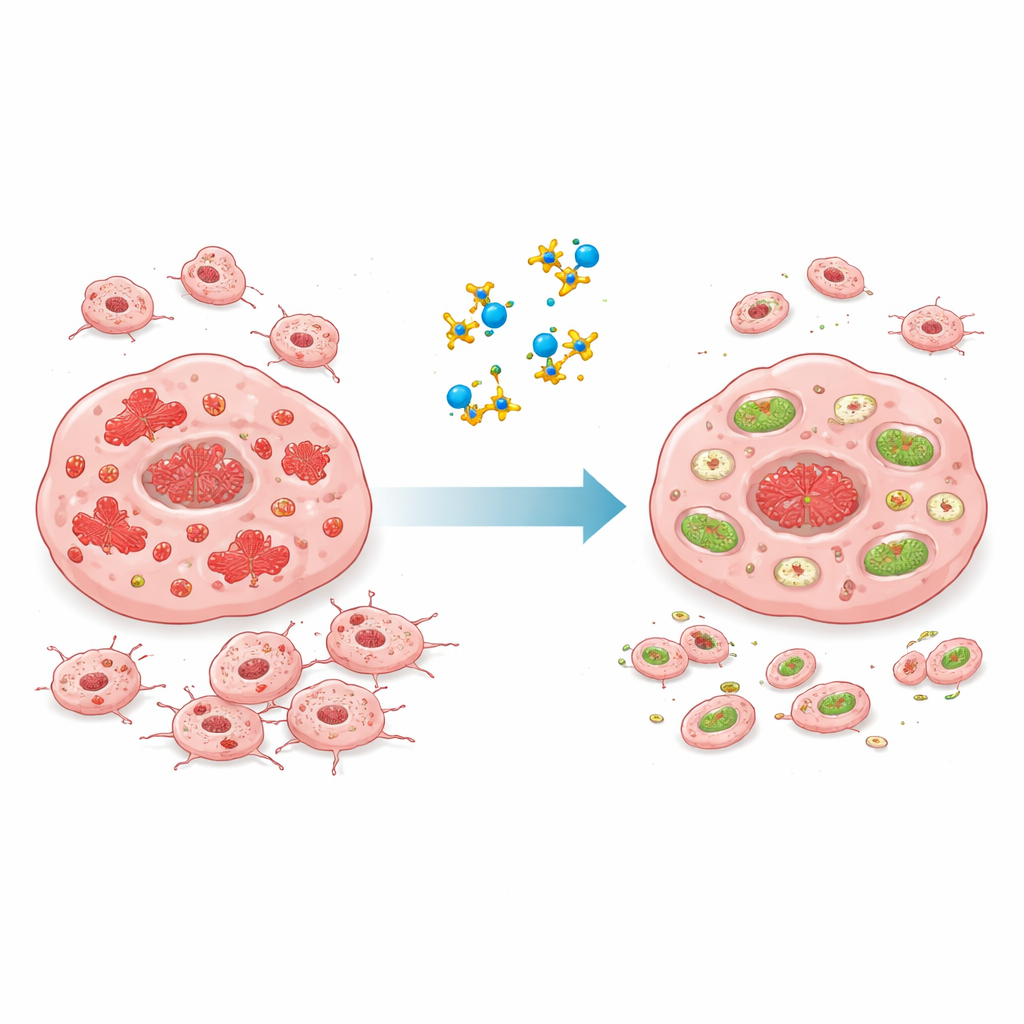
ماذا قد يعني هذا للعلاجات المستقبلية
للغير متخصصين، الرسالة الأساسية هي أن الباحثين تتبعوا سلسلة من السبب والنتيجة: ميكروRNA مفرط النشاط (miR-21-5p) يصمّت صوت بروتين وقائي (FDX1)، مما يسمح لخلايا سرطان اللسان بالنمو والانتشار، بينما يقطع المركب الطبيعي AT-101 هذه السلسلة ويتيح لـ FDX1 أداء دوره الوقائي. على الرغم من أن هذه النتائج لا تزال في مرحلة المختبر ودراسات الحيوانات، فإنها تشير إلى أن أدوية مصممة على غرار AT-101، أو مجموعات تستهدف نفس الدائرة الصغيرة RNA–البروتين هذه، قد توفر علاجات أكثر دقة لسرطان اللسان مع آثار جانبية أقل. تقدم هذه الدراسة خارطة جزيئية واضحة لتصميم علاجات مستقبلية تعطل مفاتيح السرطان الداخلية بدلاً من الاعتماد فقط على الجراحة والكيمياء العلاجية واسعة الطيف.
الاستشهاد: Fu, S., Cui, Qy., Tuo, Xy. et al. AT-101 inhibits the proliferation and invasion of tongue squamous carcinoma cells by targeting the miR-21-5p/FDX1 axis. Sci Rep 16, 10361 (2026). https://doi.org/10.1038/s41598-026-37710-9
الكلمات المفتاحية: سرطان اللسان, الميكرو RNA, العلاج الموجه, مركبات طبيعية, تمثيل الخلايا