Clear Sky Science · ar
كايمبفيرول يثبط تمايز الخلايا الهادمة للعظم وامتصاص العظم من خلال استهداف مسارات الإشارة TNF-α/NF-κB و SRC/PI3K/AKT
قوة النباتات للعظام الهشة
مع التقدّم في العمر، قد تصبح العظام رقيقة وهشة، ما يحوّل سقوطًا بسيطًا إلى كسور خطيرة. يعاني العديد من كبار السن والنساء بعد سن اليأس من هذه الحالة الصامتة، هشاشة العظام، والأدوية المستخدمة لعلاجها قد تكون مكلفة أو تسبب آثارًا جانبية. تبحث هذه الدراسة فيما إذا كان الكايمبفيرول — مركب طبيعي يوجد في أطعمة يومية مثل الشاي والبروكلي والتوت، وفي العديد من أعشاب الطب الصيني التقليدي — يمكن أن يساعد في إبطاء فقدان العظام عن طريق تهدئة الخلايا التي تلتهم العظم من الداخل.
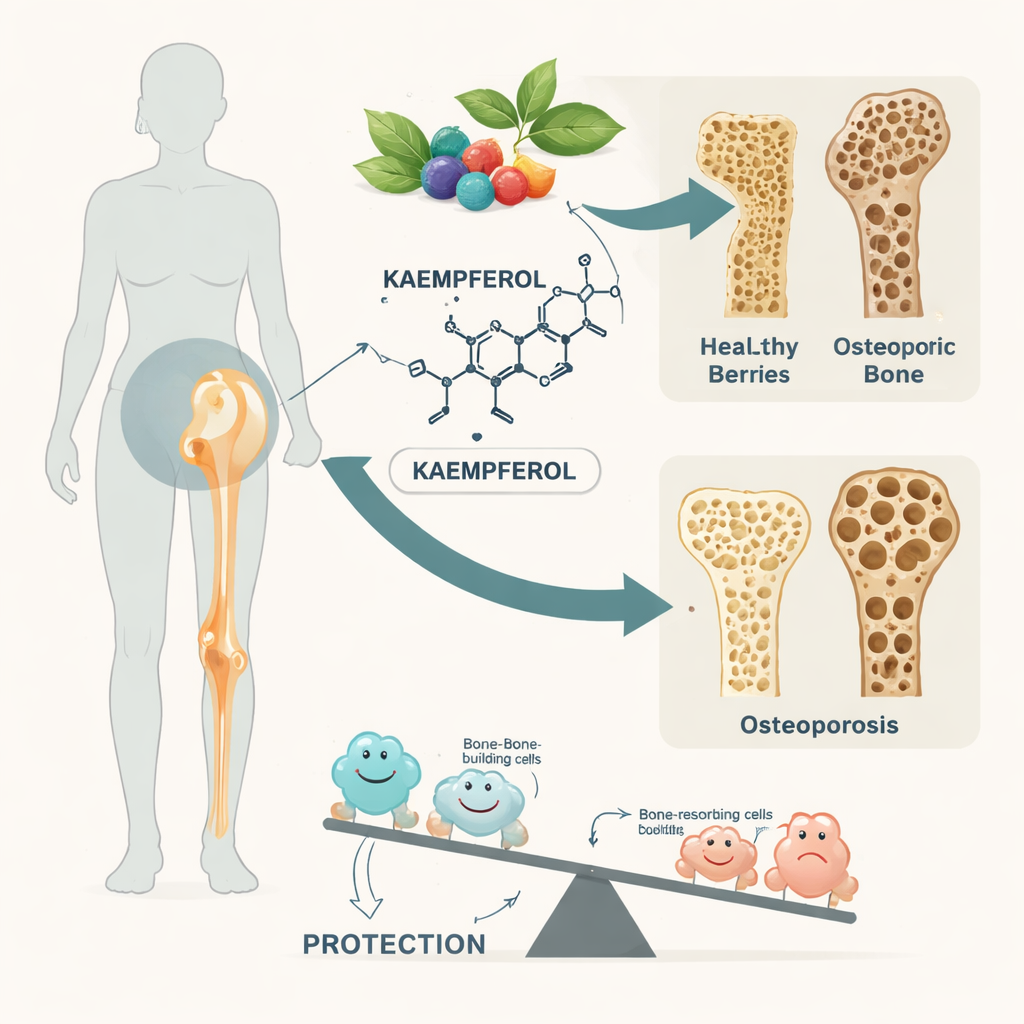
تأرجح بناء العظم وفقدانه
هيكلنا العظمي يتجدد باستمرار بواسطة فريقين متقابلين من الخلايا. فريق يبني عظمًا جديدًا، بينما الآخر، المكوَّن من خلايا تُدعى الخلايا الهادمة للعظم، يهدم العظم القديم. في حالة هشاشة العظام، يفوز فريق الهدم: يصبح العظم أخف وزنًا وأكثر مسامية وأسهل للكسر. ركز الباحثون على ما إذا كان الكايمبفيرول يمكن أن يكبح الخلايا الهادمة للعظم، موازنًا الميزان مرة أخرى لصالح عظام أقوى. واستندوا أيضًا إلى ممارسات الطب الصيني التقليدي، حيث استُخدمت أعشاب غنية بالكايمبفيرول منذ زمن طويل في تركيبات يُقال إنها «تقوّي العظام»، ليروا ما إذا كانت الأدوات الحديثة يمكن أن تفسر هذه الملاحظات القديمة.
البحث عن الأهداف الخفية للمركب
لكشف كيفية عمل الكايمبفيرول في الجسم، لجأ الفريق أولًا إلى قواعد بيانات حاسوبية كبيرة تسرد أي الجينات والبروتينات البشرية من المرجح أن تؤثر عليها جزيئات مختلفة. حدّدوا نحو 200 هدفًا لبروتين محتمل للكايمبفيرول وما يقرب من 1000 جين مرتبط بهشاشة العظام، ثم بحثوا عن التداخل. أسفرت هذه المطابقة عن 56 هدفًا مشتركًا ومجموعة أصغر من البروتينات الأساسية التي تشكل شبكة مترابطة داخل الخلايا. عدةٌ من هذه البروتينات، بما في ذلك TNF و SRC و PI3K و AKT، معروفة كمتحكمات في الالتهاب وبقاء الخلايا وإعادة تشكيل العظم. بعد ذلك أشارت محاكاة الالتحام الجزيئي الحاسوبي إلى أن الكايمبفيرول قد يرتبط بقوة بهذه البروتينات، مما يوحي بأنه قد يتداخل مباشرة مع الإشارات التي تحث على تَفكُّك العظم.
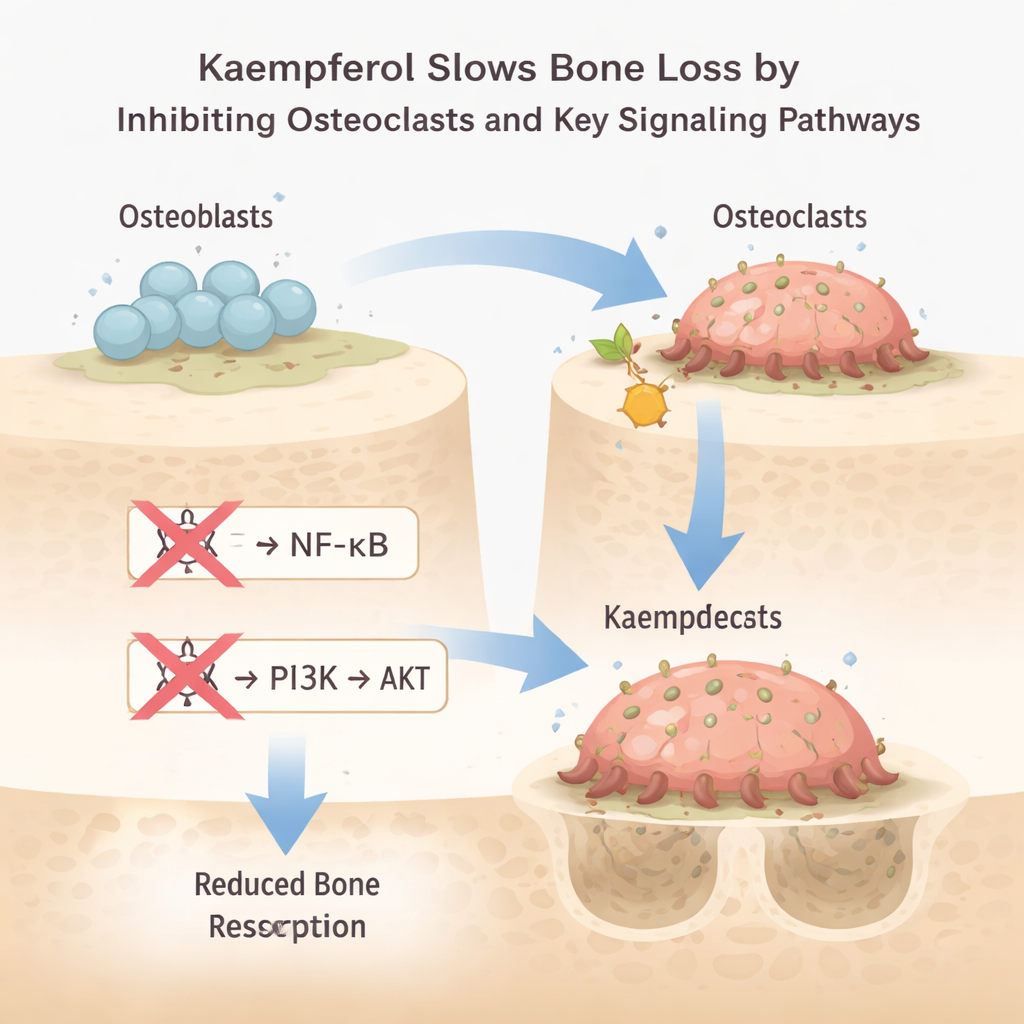
اختبار الكايمبفيرول في خلايا تلتهم العظم
تم التحقق من التنبؤات الحاسوبية لاحقًا في المختبر باستخدام خلية مناعية فئوية يمكن تحويلها إلى خلايا هادمة للعظم عن طريق إضافة إشارة تُدعى RANKL. عندما عالج الباحثون هذه الخلايا بجرعات متزايدة من الكايمبفيرول، لاحظوا انخفاضًا في عدد الخلايا الهادمة الناضجة وعدد الحفر المحفورة في قطع صغيرة من العظم، ما يدل على أن المركب قلّل مباشرة من نشاط امتصاص العظم. ومن المهم أن الكايمبفيرول لم يضر ببقاء الخلايا؛ بل إن أعلى جرعة حسَّنت بصفة متواضعة من قابلية بقاء الخلايا، ما يوحي بأن تأثيره المضاد للامتصاص ليس ببساطة نتيجة سمّية.
تخفيف الإجهاد التأكسدي والإشارات المفرطة
فحصت الدراسة أيضًا كيف يؤثر الكايمبفيرول على «الإجهاد التأكسدي»، شكل من أشكال تآكل داخلي تقوده جزيئات الأكسجين التفاعلية التي يمكن أن تضر الخلايا وتفاقم فقدان العظم. عند الجرعات المتوسطة والعالية، خفّض الكايمبفيرول مؤشرات الأكسدة الضارة وعزّز نشاط مضادات الأكسدة الواقية. في الوقت نفسه، قلّل من نشاط عدة جينات وبروتينات تحفز تكوّن ووظيفة الخلايا الهادمة للعظم. والأهم من ذلك، أنه خفّض نشاط مسارين رئيسيين داخل هذه الخلايا: أحدهما يشمل رسولًا التهابيًا قويًا (TNF) ومفتاح تشغيل رئيسي يُدعى NF-κB، والآخر يشمل SRC و PI3K و AKT، التي تُعزّز معًا تنشيط الخلية وبقائها. لم يغيّر الكايمبفيرول الكمّ الكلي لهذه البروتينات إلى حد كبير لكنه منع أشكالها المفعّلة، الفوسفورية.
ماذا قد يعني هذا لصحة العظام مستقبلًا
تُظهر النتائج مجتمعة أن الكايمبفيرول يمكن أن يبطئ في آن واحد نشوء خلايا هادمة للعظم الجديدة، ويقلّل الضرر الذي تُسبّبه، ويخفّض الإجهاد التأكسدي — وكل ذلك عبر تهدئة إشارات التهابية وإشارات بقاء أساسية. ورغم أن هذه النتائج مأخوذة من تجارب خلوية ولا تزال بحاجة لتأكيدها في نماذج حيوانية ودراسات بشرية، فإنها تقدّم تفسيرًا بيولوجيًا حديثًا لسمعة العديد من الأعشاب والأطعمة الغنية بالكايمبفيرول في حماية العظم. على المدى البعيد، قد يساعد الكايمبفيرول أو مركبات نباتية مماثلة في إلهام علاجات ألطف أو استراتيجيات تغذوية للحفاظ على عظام أقوى لفترة أطول.
الاستشهاد: Yu, Q., Jiang, T., Zhao, Y. et al. Kaempferol inhibits osteoclast differentiation and bone resorption by targeting the TNF-α/NF-κB and SRC/PI3K/AKT signaling pathways. Sci Rep 16, 6269 (2026). https://doi.org/10.1038/s41598-026-37688-4
الكلمات المفتاحية: هشاشة العظام, كايمبفيرول, امتصاص العظم, الخلايا الهادمة للعظم, الطب الصيني التقليدي