Clear Sky Science · ar
تحديد الطفرات الضارة في كامل النسخ الجينية في جينات مرشحة مرتبطة بالْجَدْر البقري (باراتوبيركولوز)
جينات خفية وراء مرض مكلف للأبقار
الْجَدْر البقري، المعروف أيضاً بمرض جوهن، يقوّض بصمت صحة وإنتاجية قطعان الألبان حول العالم، متسبباً بخسائر مالية تصل إلى مئات الملايين من الدولارات سنوياً ومثيراً قلقاً بشأن صلات محتملة باضطرابات معوية لدى البشر. تتفحّص هذه الدراسة المكوّنات الوراثية في أبقار هولشتاين لتطرح سؤالاً بسيطاً لكنه جوهري: ما الفروقات الجينية التي قد تساعد بعض الحيوانات على مقاومة هذا العدو بينما تنهار أخرى؟ من خلال قراءة الحمض النووي الريبي — النسخ العاملة من الجينات — في الدم وأنسجة الأمعاء، تتبّع الباحثون كيف يمكن لتغيرات طفيفة في الحمض النووي في جينات مناعية رئيسية أن توجه مسار المرض.
لماذا يهم هذا المرض البقري
يسبّب الْجَدْر البقري البكتيريا Mycobacterium avium من النوع الفرعي paratuberculosis (MAP). تُصاب الأبقار عادة في وقت مبكّر من حياتها، لكن العلامات تظهر غالباً بعد سنوات. في المراحل الصامتة وما قبل السريرية تبدو الحيوانات سليمة ومع ذلك قد تفرز كميات منخفضة من البكتيريا وتنتج حليباً أقل. في المراحل السريرية تتطور لديها إسهالات مزمنة وفقدان شديد للوزن وانخفاض كبير في إنتاج الحليب. قد تتجاوز معدلات العدوى على مستوى القطيع 50% في مناطق عديدة، بما في ذلك أجزاء من أوروبا وأمريكا الشمالية، مما يشكل تحدياً اقتصادياً ورفاهياً للحيوان. وبما أن هذه البكتيريا قد تعمل أيضاً كمحفّز بيئي لأمراض التهابية بشرية مثل مرض كرون، فهناك ضغط متزايد لتحسين استراتيجيات المكافحة في الأبقار.
قراءة الجينوم العامل
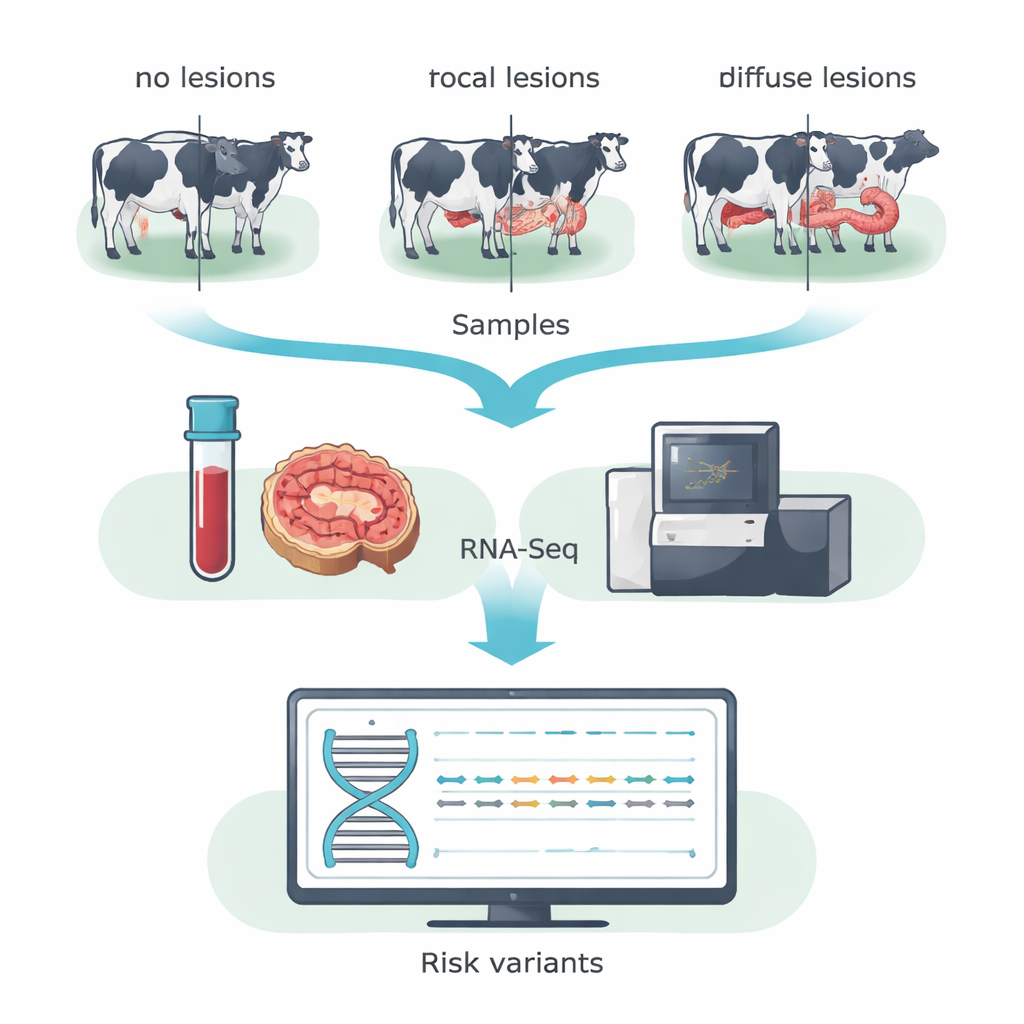
بدلاً من مسح التسلسل الكامل للحمض النووي، استخدم الفريق تسلسل الحمض النووي الريبي (RNA-Seq) للتركيز على الجينات النشطة فعلياً في الحيوان. جمعوا عينات دم وأنسجة من الصمام اللفائفي الأعوري — منطقة معوية تتأثر بشدة بـ MAP — من 14 بقرة هولشتاين في مزرعة ألبان إسبانية. استناداً إلى الفحص المجهري لأنسجة الأمعاء، تم تصنيف الأبقار إلى ثلاث فئات: حيوانات بلا آفات قابلة للكشف، وحيوانات ذات آفات صغيرة وموضعية (بؤرية) نموذجية للعدوى الطويلة ما قبل السريرية، وحيوانات ذات آفات شديدة ومنتشرة (انتشارية) مرتبطة بالمرض السريري. عبر دمج بيانات الدم والأمعاء داخل كل مجموعة، عزز الباحثون قدرتهم على اكتشاف تغييرات حرفية مفردة في الحمض النووي في الجينات المعبر عنها، والمعروفة باسم SNPs ترميزية.
اكتشاف تغييرات ضارة في جينات مناعية رئيسية
من بين مئات الآلاف من المتغيرات، ركز الفريق على تلك التي تغير تسلسل البروتين وتُتوقَّع أن تضر بوظيفة البروتين — ما يُسمى بالمتغيرات الضارة. طبقوا مرشحات صارمة لضمان ثقة عالية، ثم استخدموا أدوات تنبؤ معتمدة لوضع علامات على التغيرات الخطرة. كشفت هذه عملية الفرز عن 31 متغيراً من هذا النوع فريدة للأبقار بلا آفات، و15 فريدة لأبقار ذات آفات بؤرية، و31 فريدة لأبقار ذات آفات انتشارية. وقع العديد منها في جينات تقود كيفية تعرف خلايا المناعة على العدوى وإزالتها وتنظيم موت الخلايا وإدارة الأيض. كان من أبرزها عائلة جينات BOLA، النسخة البقرية لمركب التوافق النسيجي الكبير من الفئة الثانية، الذي يساعد خلايا المناعة على عرض أجزاء بكتيرية لخلايا T. وُجدت متغيرات مضرة مختلفة في BOLA في جميع المجموعات الثلاث من الأبقار، مما يوحي أن نسخاً محددة من BOLA قد تميل بالحيوان نحو المقاومة أو التحكم في العدوى أو الالتهاب المضر.
من متغيرات الحمض النووي إلى مسارات مرضية
لفهم ما قد تعنيه هذه التغيرات الجينية عملياً، فحص الباحثون أي المسارات البيولوجية كانت مثرية في كل مجموعة. أظهرت الأبقار بلا آفات متغيرات معدّلة في جينات مرتبطة بمعالجة المستضدات، ونقل الحويصلات، وتوازن المناعة المعوية، بما في ذلك BOLA وAP3B1 وCHGA. قد تعزز هذه التغيرات هضم البكتيريا داخل خلايا المناعة وبيئة معوية مستقرة تحد من الضرر. في الأبقار ذات الآفات البؤرية تركزت المتغيرات الضارة في جينات (ORMDL3 وKANK2) التي تُخفّض موت الخلايا المبرمج وتعدّل أيض الخلايا، مما قد يساعد المضيف على إبقاء أعداد البكتيريا منخفضة خلال مرحلة فرط طويلة ما قبل السريرية. في الأبقار ذات الآفات الانتشارية، أشارت الجينات المتأثرة إلى مسارات مناعية مفرطة النشاط مثل تمايز خلايا Th1/Th2 وعرض المستضدات، إلى جانب نقل الصفراء ومسارات استجابة الأدوية. هنا، قد تقود خواص متغيرة في عائلة BOLA إلى رد التهابي قوي، أحياناً مضر ذاتياً، مما يعكس أنماطاً تُرى في العديد من الأمراض الالتهابية والمناعية الذاتية لدى البشر.
دلائل لتربية قطعان أكثر صلابة
بعيداً عن إلقاء الضوء على كيفية تشكيل المتغيرات الجينية المختلفة للاستجابة المناعية تجاه MAP، ربطت الدراسة أيضاً هذه التغيرات الخطرة بمناطق معروفة من الجينوم البقري المرتبطة بصفات صحية، بما في ذلك القابلية للإصابة بالْجَدْر البقري وعدوى أخرى. وبينما تتطلب هذه النتائج مزيداً من التحقق في قطعان أكبر ولا يمكن استخدامها حالياً كمؤشرات تشخيصية مستقلة، فإنها تقدّم فهرساً واعداً من المتغيرات والجينات المرشحة. بعبارة بسيطة، تشير النتائج إلى أن بعض الأبقار تحمل نسخاً جينية تساعدها على السيطرة الهادئة على العدوى، بينما تحمل أخرى نسخاً توفّر مناخاً للالتهاب المفرط والمرض الشديد. في المستقبل، قد تدعم مثل هذه المعلومات التهجين الانتقائي والاختبارات الجينية التي توجّه القطعان نحو مقاومة طبيعية أكبر، مما يقلل الخسائر الاقتصادية والحاجة إلى إجراءات مكثفة لمكافحة المرض.
الاستشهاد: Badia-Bringué, G., Lam, S., Cánovas, Á. et al. Whole-transcriptome identification of deleterious variants in candidate genes linked to bovine paratuberculosis. Sci Rep 16, 6243 (2026). https://doi.org/10.1038/s41598-026-37675-9
الكلمات المفتاحية: الْجَدْر البقري (باراتوبيركولوز), جينات مرض جوهن, مناعة الأبقار الحلوب, تسلسل الحمض النووي الريبي, تربية مقاومة الأمراض