Clear Sky Science · ar
إشارات الإنترفيرون من النوع الأول تحدد بصمة مرضية جديدة في الخلايا القرنية البشرية لمتلازمة البِقَع الجِلْدية المبللة من النوع C
لماذا يمكن أن يكون ضوء الشمس خطيراً للغاية بالنسبة لبعض الناس
بالنسبة لمعظمنا، يعني ضوء الشمس الدفء وفيتامين D. لكن بالنسبة للأشخاص المصابين بحالة وراثية نادرة تُدعى البِقَع الجِلْدية المبللة من النوع C (XP-C)، قد يؤدي التعرض المعتدل للضوء النهاري إلى تلف جلدي شديد ومخاطر كبيرة للإصابة بسرطان الجلد. تتجاوز هذه الدراسة المشكلة المعروفة في إصلاح الحمض النووي في XP-C وتكشف عن طبقة مخفية من إشارات شبيهة بالجهاز المناعي مفرطة النشاط داخل خلايا الجلد لديهم، ما يقدم دلائل جديدة حول سبب كون بشرتهم عرضة ومُلتهبة بشدة بعد التعرض للشمس.
عندما يفشل إصلاح الحمض النووي في الجلد
تُصلح خلايا جلدنا باستمرار تلف الحمض النووي الناتج عن الأشعة فوق البنفسجية B (UVB) من الشمس. يعد البروتين المسمى XPC واحداً من أوائل «أجهزة الاستشعار» التي تكتشف الآفات الناتجة عن الأشعة فوق البنفسجية وتطلق فريق إصلاح واسع. في حالة XP-C، تُضعِف الطفرات في جين XPC هذه الخطوة التحذيرية المبكرة، فيتراكم تلف الأشعة فوق البنفسجية بدلاً من إصلاحه. يصاب مرضى XP-C بسرطانات الجلد بمعدلات تزيد عن المعدلات العامة بمقدار آلاف المرات ويجب عليهم تجنب ضوء الشمس بحذر شديد. ومع أن عيب إصلاح الحمض النووي هذا معروف جيداً، فإن كيفية إعادة توصيل شبكات الاتصال الداخلية في الخلايا—وخاصة تلك التي تتحكم بالالتهاب—كانت أقل وضوحاً كثيراً.
استكشاف إشارات الخلايا مع مرور الوقت
لمعالجة هذه المسألة، مهندس الباحثون خلايا قرنية بشرية—وهي الخلايا الرئيسية في الطبقة الخارجية للجلد—لتفتقر تماماً إلى XPC، وقارنوها مع خلايا طبيعية متماثلة بخلاف ذلك. عرضوا كلا النوعين من الخلايا لمستوى UVB مختار بعناية ومماثل لجرعة حروق شمس معتدلة. ثم فحصوا الخلايا في مرحلتين. بعد ساعة من الإشعاع، قاسوا نشاط العديد من الإنزيمات المسماة كينازات التيروسين البروتينية، التي تُشغّل الإشارات أو تُطفئها بإضافة علامات فوسفات صغيرة. وبعد أربع وعشرين ساعة، استخدموا مطيافية الكتلة المتقدمة للحصول على لقطة واسعة لآلاف البروتينات ومعرفة أيها ازداد أو انخفض في الوفرة. سمح لهم هذا النهج المكوّن من خطوتين بتتبع كل من «أجراس الإنذار» المبكرة والاستجابات «اللاحقة المتتالية» داخل الخلايا.
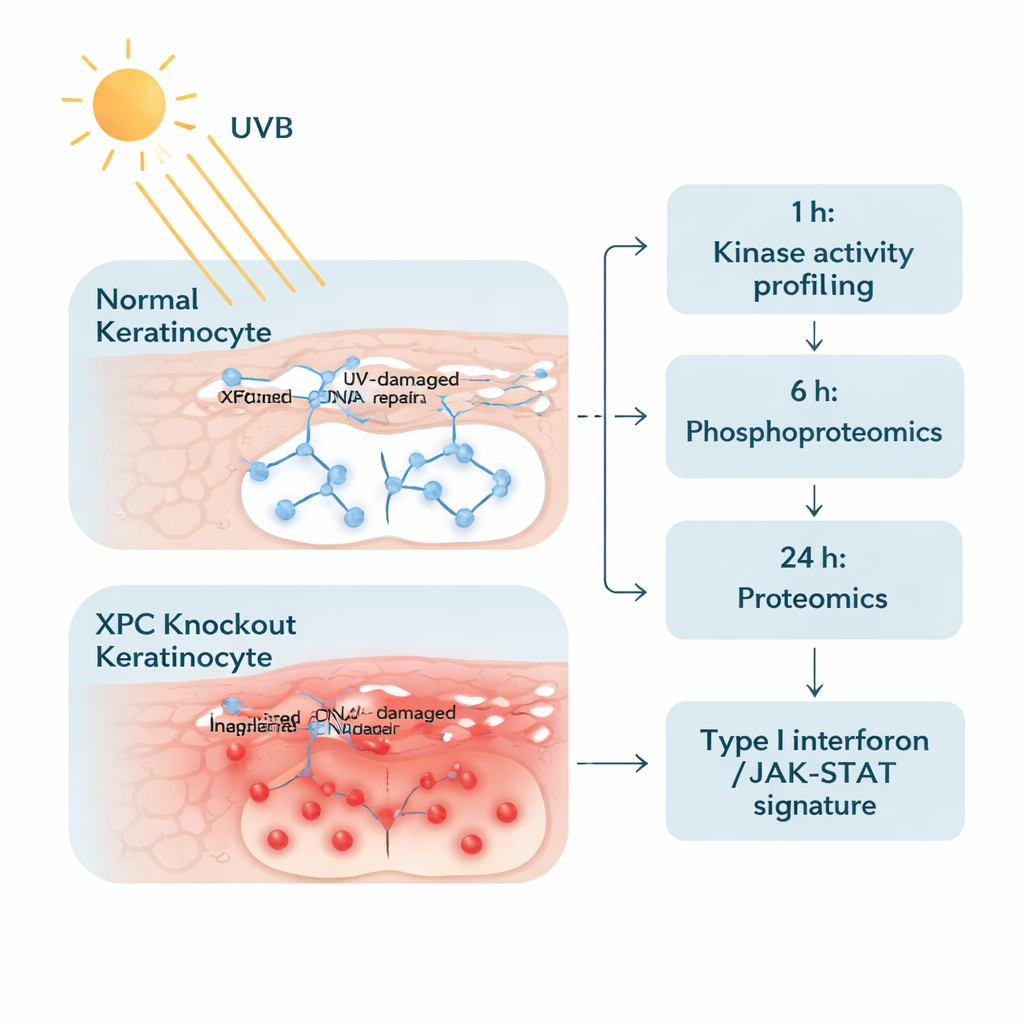
مسار التهابي يضيء
كشفت الشاشة المبكرة للكينازات أن الخلايا القرنية المحرومة من XPC تستجيب لـ UVB بطفرة في الفسفرة على أكثر من مائة موقع مقارنة بالخلايا الطبيعية. ولاحظ الباحثون أن العديد من هذه التغيرات تركزت في مسار إشارات JAK/STAT—وهو مسار اتصال مركزي تُستخدمه عادة المراسلات المناعية مثل الإنترفيرونات. كانت العلامات المرتبطة بـ JAK1 وJAK2 وJAK3 وTYK2 وبروتينات STAT أكثر نشاطاً في خلايا XP-C، حتى قبل التعرض لـ UVB، وزادت أكثر بعد الإشعاع. يشير ذلك إلى أن الخلايا كانت متهيئة في حالة «يقظة عالية»، جاهزة لتكثيف رسائل الالتهاب كلما واجهت إجهاداً ناشئاً عن الأشعة فوق البنفسجية.
جينات إنذار على غرار الإنترفيرون في خلايا الجلد
أكد الاستطلاع البروتيني الأوسع والأحدث هذه الصورة ووسعها. في الخلايا المطوية لـ XPC، وخصوصاً بعد UVB، تغيرت مئات البروتينات، وارتبطت مجموعة كبيرة بجينات تُشغّل عادةً بواسطة إنترفيرونات النوع الأول—نفس الإشارات المضادة للفيروسات التي يستخدمها الجسم لمقاومة العدوى. ارتفعت مستويات بروتينات مثل MX1 وMX2 وIFIT1 وIFIT2 وIFIT3 وISG15 وOAS1 وIRF9، وهي «جينات مُحفَّزة بالإنترفيرون» نموذجية، بشكل قوي. ربطت تحليلات الشبكات والمسارات هذه البروتينات مرة أخرى بمسار JAK/STAT وإشارات الإنترفيرون من النوع الأول كالسمة المهيمنة. أكدت تجارب وسترن بلوت اللاحقة أن بروتينات STAT الرئيسية كانت أكثر فسفرة، وأن هذه البروتينات المستجيبة للإنترفيرون أنتجت بمستويات أعلى بكثير في خلايا XP-C مقارنة بالخلايا القرنية الطبيعية، سواء في السكون أو بشكل خاص بعد UVB.
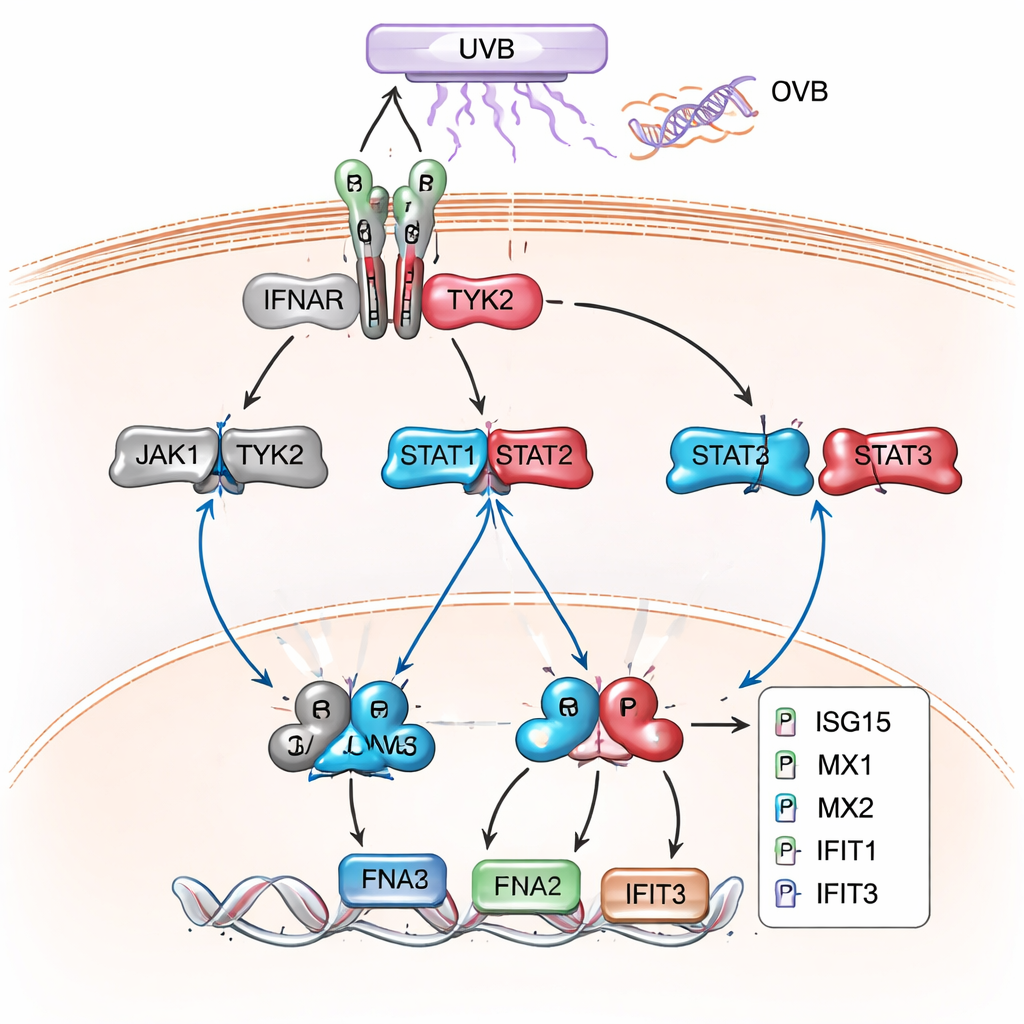
ماذا يعني هذا للمرضى والعلاجات المستقبلية
تظهر هذه النتائج مجتمعة أن XP-C ليس مرضاً ناتجاً عن عطب إصلاح الحمض النووي فحسب؛ بل يتميز أيضاً بحالة التهابية مستمرة تشبه الإنترفيرون داخل خلايا الجلد، يقودها مسار JAK/STAT وتتفاقم بفعل الضوء فوق البنفسجي. للمختص غير المتخصص، يعني هذا أن خلايا XP-C القرنية تتصرف كما لو أنها تقاتل عدوى غير مرئية باستمرار كلما تعرضت لضوء الشمس، مضيفة التهاباً مزمناً فوق تلف الحمض النووي غير المصحح. وبينما لا تختبر الدراسة علاجات مباشرة، فإنها تفتح احتمال أن الأدوية المصممة بعناية لاستهداف JAK/STAT أو الدوائر الالتهابية ذات الصلة قد تساعد يوماً ما في تقليل الضرر الناجم عن الأشعة فوق البنفسجية في XP-C وربما في حالات جلدية التهابية أخرى تشترك في هذه البصمة الجزيئية.
الاستشهاد: Nasrallah, A., Rezvani, HR., Belmudes, L. et al. Type I interferon signaling defines a novel disease signature in xeroderma pigmentosum C human keratinocytes. Sci Rep 16, 6559 (2026). https://doi.org/10.1038/s41598-026-37662-0
الكلمات المفتاحية: البِقَع الجِلْدية المبللة, سرطان الجلد, إصلاح الحمض النووي, إشارات الإنترفيرون, مسار JAK STAT