Clear Sky Science · ar
Wnt-3a يزيد إنتاج TNF-α في الخلايا الدبقية الصغيرة المنشَّطة بـ LPS بغض النظر عن مسار β-catenin الكلاسيكي
لماذا يهم التهاب الدماغ
اتضح أن العديد من اضطرابات الدماغ، بما في ذلك مرض باركنسون، تنطوي على التهاب مزمن. في هذه العملية، يمكن للخلايا المناعية المقيمة في الدماغ، المسماة بالخلايا الدبقية الصغيرة، أن تتحول من مساعدين حمايين إلى مهاجمين مفرطي النشاط يضرون بالخلايا العصبية المجاورة. تطرح هذه الدراسة سؤالاً معاصراً: هل يمكن لجزيء إشارية يُدعى Wnt‑3a، والذي كان يُعتقد طويلاً أنه يوفر تأثيرات مهدئة وحامية، أن يزيد الالتهاب في ظروف معينة؟ يتضح أن الإجابة أكثر تعقيداً من المتوقع، وتُبرز سبب إمكانية أن يكون نفس الجزيء مفيدًا في سياق وضارًا في آخر.
مرسل بوجهين
بروتينات Wnt هي عائلة من الرسل الكيميائية التي تساعد في توجيه تطور الدماغ، والحفاظ على الخلايا الدماغية في البالغين، وتشكيل استجابة الخلايا للإصابة. أحد أعضاء هذه العائلة الذي دُرس على نطاق واسع، Wnt‑3a، يرتبط عادة بمسار إشارية "كلاسيكي" يستقرل بروتينًا يسمى β‑catenin داخل الخلايا. في العديد من الأنظمة، يبدو أن تفعيل هذا المسار يخفف الالتهاب ويدعم بقاء الخلايا العصبية، لذا تساءل بعض الباحثين عما إذا كان تعزيز Wnt‑3a قد يساعد في حماية الخلايا المنتجة للدوبامين المعرضة للخطر في مرض باركنسون. ومع ذلك، يمكن لبروتينات Wnt أن تنقل الإشارة أيضًا عبر مسارات بديلة "غير كلاسيكية" قد تدفع نحو الالتهاب، والمسار المسيطر يعتمد على نوع الخلية وحالتها.
عندما تبقى الخلايا الهادئة هادئة
لاستكشاف هذه الاحتمالات، درس الباحثون خلايا دبقية صغيرة أولية مستزرعة من أدمغة الفئران. نظروا أولاً إلى الخلايا الدبقية في حالة راحة وتعرضت فقط لـ Wnt‑3a. في هذه الظروف الهادئة، لم يزد Wnt‑3a من إفراز جزيئات التهابية رئيسية مثل TNF‑α أو IL‑1β. وعلى الرغم من أن بعض الإشارات داخل الخلايا قد تفاعلت، لم تتحول الخلايا الدبقية إلى نمط التهابي قوي. هذا يشير إلى أنه في دماغ صحي وغير ملتهب، قد يكون لإضافة Wnt‑3a بمفردها تأثير مباشر ضئيل على إنتاج الخلايا الدبقية للمواد الالتهابية.
عندما تُدفع الخلايا الملتهبة إلى الأمام
تغيرت الصورة بشكل كبير بمجرد إثارة الخلايا الدبقية إلى حالة التهابية أولاً باستخدام الليبوفولسيكاريد البكتيري (LPS)، وهو أداة مخبرية قياسية لمحاكاة العدوى. كما هو متوقع، أدى LPS وحده إلى زيادة قوية في إنتاج TNF‑α. لكن عندما أُضيف Wnt‑3a معا مع LPS، أطلقت الخلايا الدبقية كميات أكبر بشكل ملحوظ من TNF‑α مقارنةً بـ LPS وحده، بينما لم يزد IL‑1β أكثر. أظهرت القياسات التفصيلية أن هذه الزيادة في TNF‑α لم تنجم عن تنشيط أكبر للمسار الالتهابي المعروف NFκB ولا عن تنشيط إضافي للمسار الكلاسيكي β‑catenin. إيقاف مسار β‑catenin بواسطة بروتين يسمى DKK1 ترك زيادة TNF‑α المدفوعة بـ Wnt‑3a دون تغيير، مما يشير إلى أن المسار «المضاد للالتهاب» المتوقع لم يكن مسؤولاً.
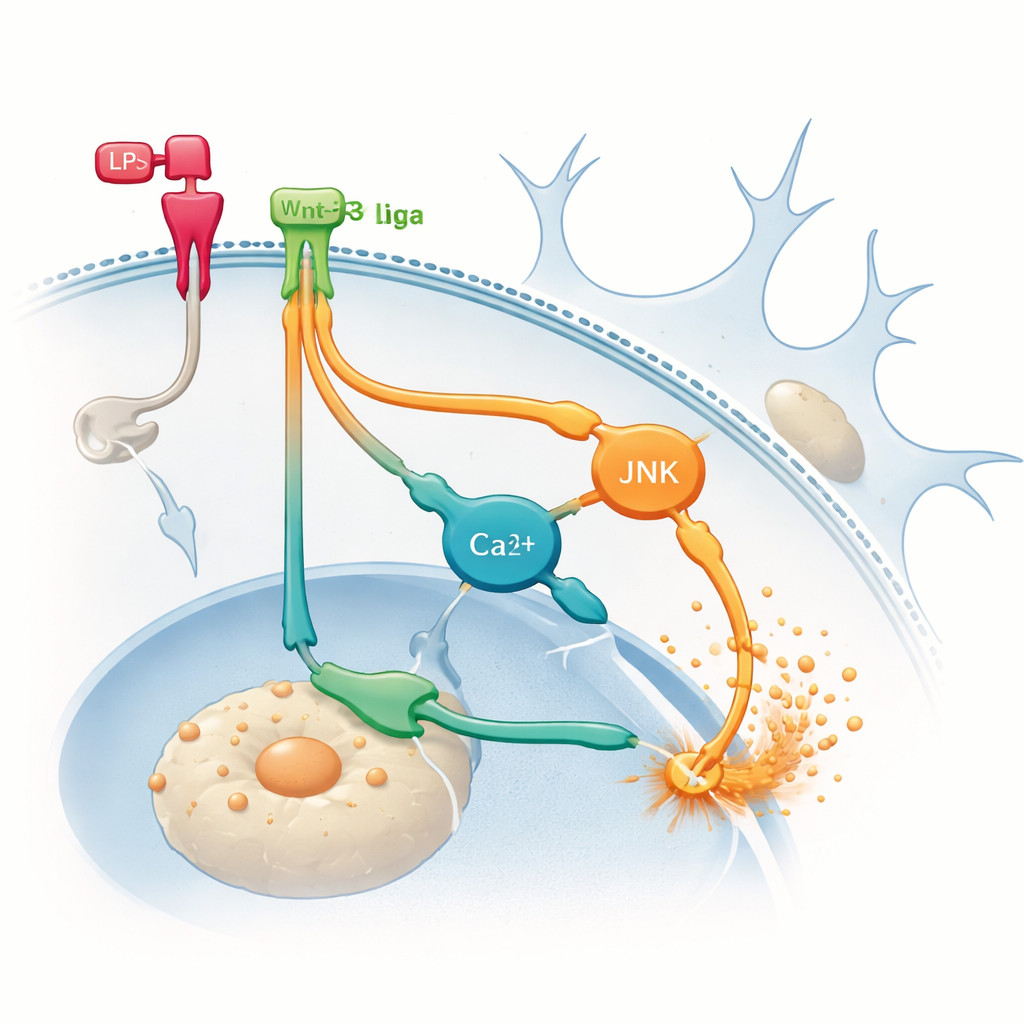
مسارات خفية تؤجج النيران
للبحث عن مصدر الالتهاب الإضافي، تحول الفريق إلى المسارات غير الكلاسيكية البديلة التي يمكن لبروتينات Wnt أن تستخدمها. قاموا بحجب فرعين إشاريين داخل الخلايا الدبقية دوائياً: أحدهما يشمل بروتينًا يسمى JNK، والآخر مرتبطًا بتغيرات في مستويات الكالسيوم داخل الخلية. أدى تثبيط أي من الفرعين إلى خفض إنتاج TNF‑α المحفَّز بواسطة LPS، والأهم من ذلك، منع Wnt‑3a من تعزيز TNF‑α أكثر. تشير هذه النتائج إلى أنه، بمجرد أن تكون الخلايا الدبقية ملتهبة بالفعل، يمكن لـ Wnt‑3a أن يتحول إلى استخدام المسارات غير الكلاسيكية بشكل أساسي لتضخيم الإشارات الالتهابية بدل تهدئتها. بعبارة أخرى، يمكن للمرسل نفسه أن يسلك مسارًا داخليًا مختلفًا اعتمادًا على الحالة الابتدائية للخلية، مع نتائج مختلفة تمامًا.
الاختبار في نموذج لباركنسون
ثم تساءل الباحثون عما إذا كان هذا السلوك لـ Wnt‑3a في الخلايا الدبقية سينعكس على تأثيرات أكبر على الخلايا العصبية في دماغ حي. أداروا Wnt‑3a مباشرة إلى بطينات الدماغ في فئران تلقت السم MPTP، وهو نموذج مستخدم على نطاق واسع لضرر يشبه باركنسون في خلايا الدوبامين وتفعيل الخلايا الدبقية. كما كان متوقعًا، خفض MPTP عدد خلايا الدوبامين وزاد أعداد الخلايا الدبقية في منطقة وسط الدماغ الحرجة للحركة. ومع ذلك، لم يزد Wnt‑3a الإضافي من فقدان الخلايا العصبية أو يغير بشكل كبير أعداد الخلايا الدبقية مقارنةً بالحيوانات التي عولجت بالمذيب. في هذا السياق المعقد داخل الكائن الحي، لم ينقذ Wnt‑3a الخلايا العصبية ولا زاد بوضوح من تأثيرات السم الضارة خلال إطار الزمن الذي درس.
ما الذي يعنيه هذا للعلاجات المستقبلية
بشكل عام، تُظهر الدراسة أن Wnt‑3a ليس مفتاح تشغيل/إيقاف بسيطًا لالتهاب الدماغ. في الخلايا الدبقية الهادئة له تأثير ضئيل، ولكن في الخلايا الملتهبة بالفعل يمكنه أن يزيد بشكل انتقائي إفراز TNF‑α عبر مسارات إشارية غير كلاسيكية، مستقلاً عن المسار الكلاسيكي β‑catenin. وفي الوقت نفسه، لم تُظهر إضافة Wnt‑3a في نموذج فأري يشبه باركنسون حماية واضحة أو ضررًا إضافيًا للخلايا المنتجة للدوبامين على المدى القصير. بالنسبة للراغبين في تطوير علاجات مستقبلية، الرسالة الأساسية هي أن استهداف إشارات Wnt سيتطلب فهماً دقيقاً لسياق الخلايا. قد تساعد العلاجات المبنية على Wnt‑3a أو جزيئات ذات صلة في مواقف معينة لكنها قد تضر في أخرى إذا أدت بطريق الخطأ إلى تكثيف الالتهاب الضار.
الاستشهاد: Federici, G., Stayte, S., Rentsch, P. et al. Wnt-3a exacerbates production of TNF-α in LPS stimulated microglia independent of the β-catenin canonical pathway. Sci Rep 16, 8222 (2026). https://doi.org/10.1038/s41598-026-37653-1
الكلمات المفتاحية: التهاب الدماغ, الخلايا الدبقية الصغيرة, إشارة Wnt, مرض باركنسون, TNF-alpha