Clear Sky Science · ar
مجموعات بروتين APOL1 في غشاء البلازما تقاوم التحلل السريع للبروتين
لماذا تهم «حيلة الاختفاء» لبروتين الكلية
تم ربط جزء كبير من حالات أمراض الكلى الشديدة لدى الأشخاص ذوي الأصول الإفريقية الحديثة بنسختين متغيرتين من جين واحد، APOL1. ومع ذلك لا يزال العلماء يكافحون لتوضيح كيف يضر هذا الجين بخلايا الكلى دون أن يؤذي معظم حامليه. تطرح هذه الدراسة سؤالًا يبدو بسيطًا لكنه ذا تبعات كبيرة: بعد أن يُصنَع بروتين APOL1 داخل الخلايا، كم من الوقت يبقى موجودًا وأين يكون أكثر استقرارًا؟ تكشف الإجابات عن شخصية منقسمة مفاجئة — فـ APOL1 يُدمَّر بسرعة داخل الخلايا لكنه يظل ثابتًا بعناد عندما يكون مدمجًا في سطح الخلية الخارجي، وهو دليل قد يوجه العلاجات المستقبلية.
جين الخطر ذو الحدين
يساعد جين APOL1 في حماية البشر من طفيليات معينة، وهي ميزة تطورية تفسر على الأرجح شيوع متغيراته الخطرة، المسماة G1 وG2، في السكان الأفارقة. للأسف، الأشخاص الذين يرثون نسختين من هذه المتغيرات يواجهون خطرًا مرتفعًا بشكل كبير للإصابة باضطرابات كلية تُصنف كأمراض كلوية بوساطة APOL1. أظهرت أعمال سابقة أنه عندما ترتفع مستويات APOL1 — غالبًا استجابة للالتهاب — قد يصبح البروتين سامًا، لا سيما في الخلايا المرشِّحة الدقيقة للكلى المعروفة باسم الخلايا الجذعية الحويصلية (podocytes). لكن معظم الدراسات ركزت على ما يُفعِّل APOL1. وكان معروفًا أقل بكثير كيف تطفئه الخلايا مرة أخرى، على سبيل المثال عن طريق تحطيم البروتين.
تتبع بروتين هش داخل الخلايا
لاستكشاف ثبات APOL1، مهندس الباحثون خطوط خلايا بشرية لإنتاج نسخ من APOL1 وقريبته الأقرب APOL2 موسومة بمؤشرات فلورية. سمح لهم ذلك بمراقبة كمية كل بروتين تتراكم أو تختفي تحت ظروف مختلفة باستخدام الواسترن بلوت والمجهر والقياس الخلوي بالتدفق. أعاقوا جهاز تكسير البروتين الرئيسي في الخلية، البروتيازوم، ومنعوا بصورة منفصلة تصنيع البروتين الجديد. عندما تم تثبيط البروتيازومات، ارتفعت مستويات APOL1 بسرعة، مما يدل على أنه عادةً ما يُكسر بوتيرة سريعة. وعندما أوقفوا تخليق البروتين الجديد، انخفضت مستويات APOL1 بسرعة. على النقيض التام، لم يتغير APOL2 تقريبًا تحت أي من العلاجين، كاشفًا عنه كبروتين أكثر استقرارًا بكثير. ومن المهم أن نعترف بأن معدل دوران APOL1 العالي كان نفسه للنسخة الطبيعية (G0) ولنسخ الخطر (G1 وG2)، وكان ذلك عبر عدة أشكال طبيعية لـ APOL1 تختلف في كيفية وجودها داخل الأغشية.
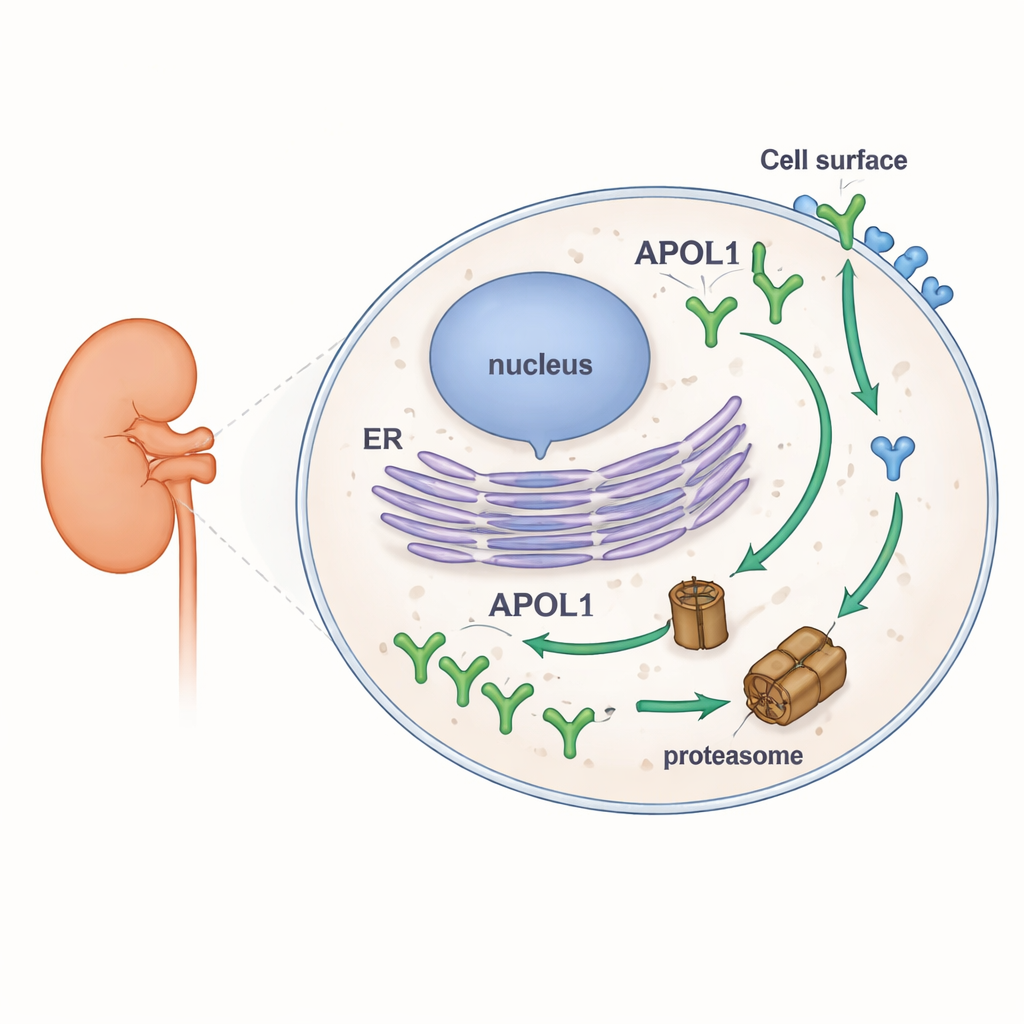
دلائل متسلسلية وقصة حيين متباينين
غاص الفريق في بنية البروتين، واستخدموا أدوات حاسوبية لمسح APOL1 وAPOL2 بحثًا عن مقاطع رخوة وغير منظمة تُعرف بالمناطق intrinsically disordered. غالبًا ما تعمل مثل هذه المناطق كإشارات «كُلني» للبروتيازوم. حدَّدوا منطقتين مرشحتين قويتين في APOL1 كانت غائبة إلى حد كبير في APOL2. لاختبار ما إذا كان الطرف الأميني الفريد لـ APOL1 يساهم في هشاشته، صنعوا هجينات: APOL1 مقصوص يفتقد أول 59 حمض أميني، وشيميرا من APOL2 تحمل ذلك المقطع من APOL1. إضافة القطعة الطرفية الأمينية لـ APOL1 إلى APOL2 جعلت APOL2 يتحلل أسرع، بينما ظل APOL1 المقطوع غير مستقر، مما يوحي بأن أكثر من جزء واحد في APOL1 يشجع على التحلل السريع. مجتمعة، تربط هذه النتائج مقاطع APOL1 المرنة غير الاعتيادية بدورانها السريع، من دون ربط هذا السلوك تحديدًا بالمتغيرات المسببة للمرض.
بروتين عنيد على سطح الخلية
برز الأثر الأكثر لفتًا عندما ميَّز المؤلفون بين APOL1 داخل الخلية وAPOL1 على سطح الخلية. باستخدام أجسام مضادة تتعرف فقط على الجزء من APOL1 المكشوف إلى الخارج، قاسوا مستويات السطح بشكل منفصل عن المستويات الكلية. داخل الخلية، تصرف APOL1 كما هو متوقع: تراكم عندما تم حجب البروتيازومات واختفى بسرعة عندما أوقف تخليق البروتين الجديد. أما APOL1 السطحي فلم يتغير تقريبًا تحت أي من الحالتين. بمجرد أن وصلت جزيئات APOL1 إلى غشاء البلازما، ثبت أنها مقاومة للغاية للتحلل السريع. علاوة على ذلك، على الرغم من أن المتغيرات المسببة للخطر أنتجت إجمالي APOL1 أقل من النسخة الطبيعية، كانت مستوياتها السطحية متشابهة. يشير ذلك إلى أن المتغيرات الخطرة والطبيعية تُنقَّى بمعدلات مشابهة داخل الخلية، لكن مجموعات البروتين المدمجة في الغشاء — التي يُعتقد أنها تشكل قنوات أيونية وتقود السمية — محفوظة في جميع المتغيرات.
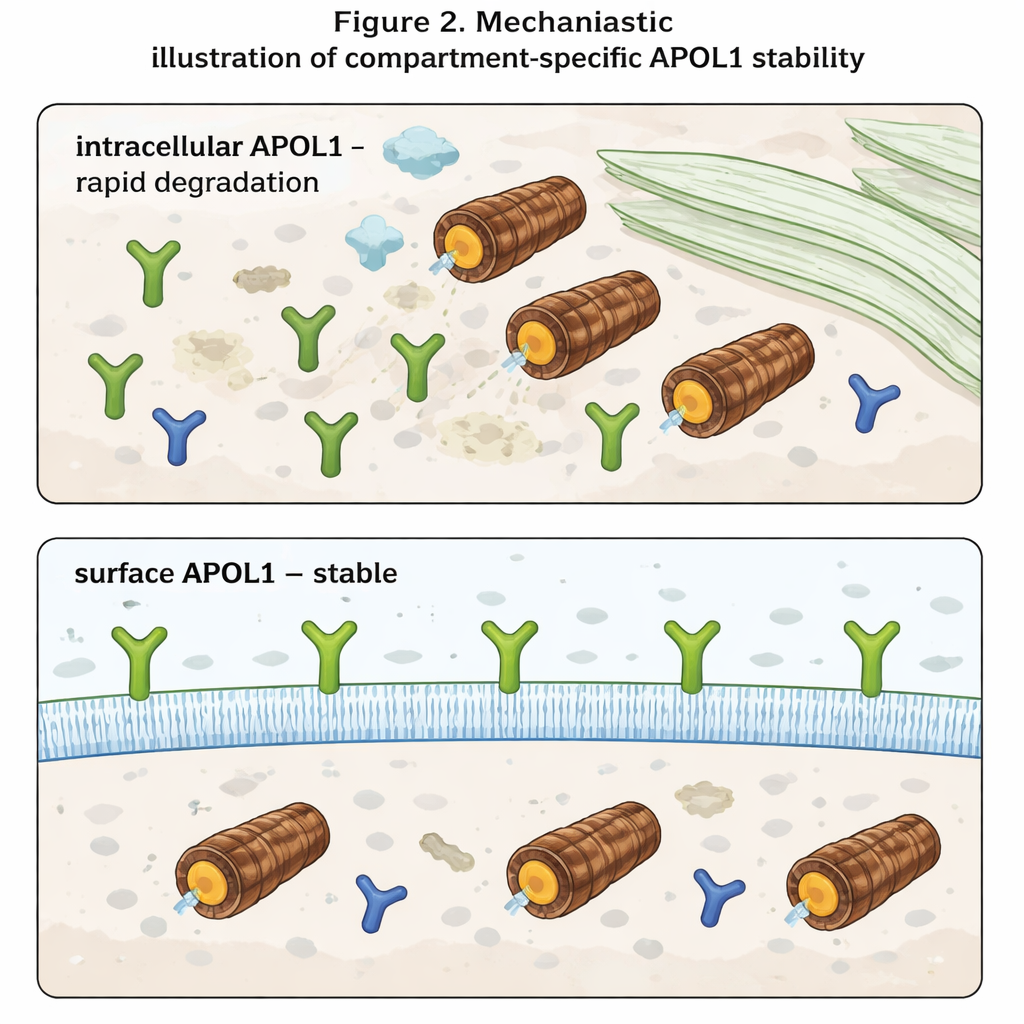
ماذا يعني هذا للعلاجات المستقبلية
لغير المتخصصين، الخلاصة هي أن APOL1 يتصرف بشكل مختلف للغاية اعتمادًا على مكان وجوده. داخل الخلية، هو بروتين قصير العمر، يُعرف ويُدمر بسرعة. على سطح الخلية، يصبح طويل العمر ومحميًا نسبيًا، حتى عندما يتغير جهاز التحلل في الخلية. وبما أن المرض يبدو أنه ينشأ عندما تُخلُّ قنوات APOL1 السطحية بتوازن أيونات مثل الصوديوم والبوتاسيوم، فقد تحتاج العلاجات إلى التركيز أقل على مستويات APOL1 الإجمالية وأكثر على كمية ما يصل إلى غشاء البلازما ويستمر هناك. قد تقلل الاستراتيجيات التي تقلل نقل APOL1 إلى السطح أو تزعزع استقرار المجموعة السطحية انتقائيًا من تلف الكلى دون حجب الوظائف المناعية المفيدة للجين تمامًا.
الاستشهاد: Höffken, V., Alvermann, L., Niggemeier, D. et al. APOL1 plasma membrane pools resist rapid protein degradation. Sci Rep 16, 6718 (2026). https://doi.org/10.1038/s41598-026-37647-z
الكلمات المفتاحية: APOL1, أمراض الكلى, تحلل البروتين, غشاء البلازما, بروتيازوم