Clear Sky Science · ar
الخصائص الحُليّة للنطاق الحفّاز لإنزيم إزالة أستلة الهيستون 5 البشري في المختبر
لماذا تهمّ هذه المفاتيح الصغيرة في تغليف حمضنا النووي
داخل كل خلية، يلتف حمضنا النووي حول بروتينات تعمل كبكرات، مما يساعد على وضع أمتار من المادة الوراثية في مساحة مجهرية. سواء تم تشغيل جين أم إيقافه غالباً ما يعتمد على علامات كيميائية صغيرة على هذه البروتينات البكرية. تركز هذه الدراسة على مفتاح بروتيني محدد يُدعى HDAC5، المرتبط بأمراض القلب واضطرابات الدماغ والسرطان والمزيد. من خلال فهم كيفية عمل HDAC5 على المستوى الجزيئي، يأمل الباحثون تمهيد الطريق لأدوية أكثر دقّة وبآثار جانبية أقل.
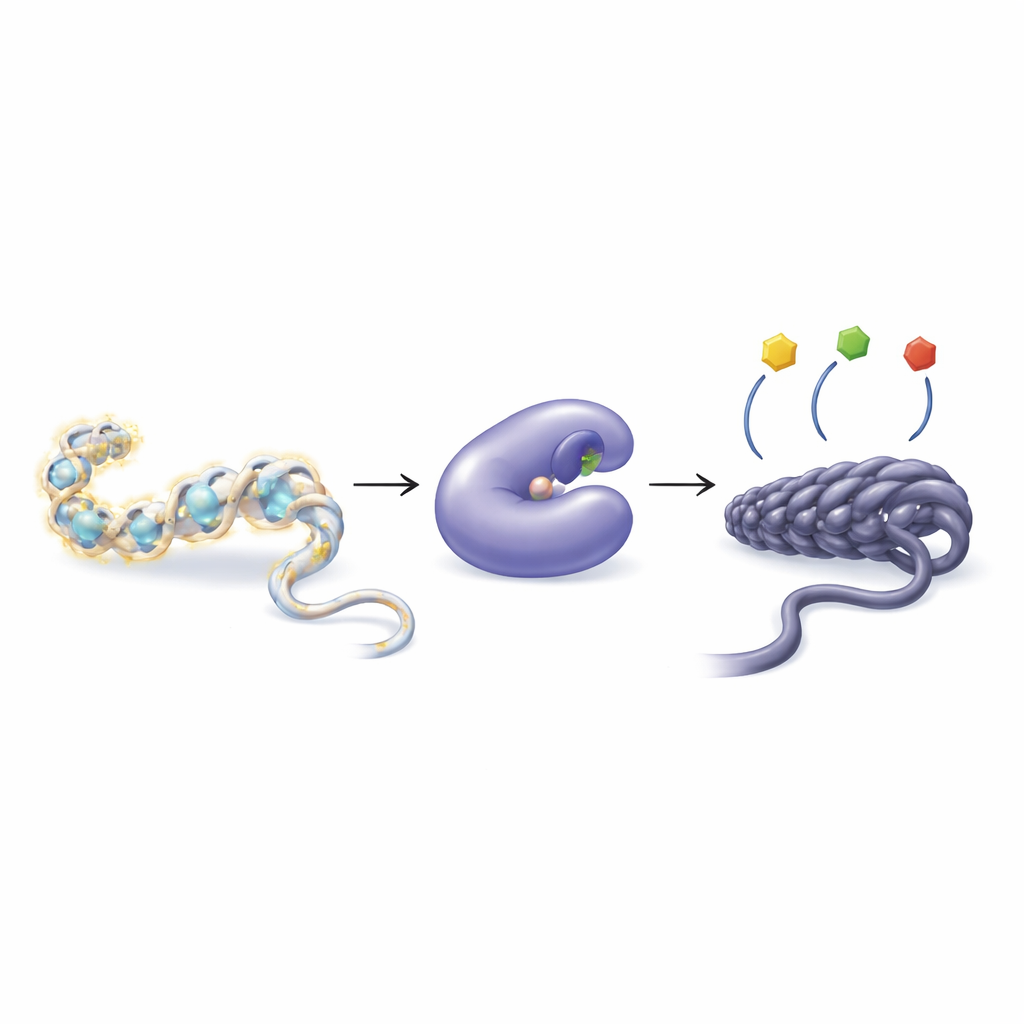
كيف تضبط الخلايا الجينات بعلامات كيميائية صغيرة
لا يطفو حمضنا النووي بحرية بل يلتف حول بروتينات تُسمى الهيستونات، مكوِّنة هيكلًا يعرف بالكروماتين. يمكن للخلايا إضافة أو إزالة مجموعات كيميائية صغيرة، مثل مجموعات الأسيتيل، من ذيول الهيستونات لجعل الكروماتين أكثر ارتخاءً أو إحكامًا. يؤدي التغليف الأرخَص عمومًا إلى سهولة قراءة الجينات؛ بينما يميل التغليف الأحكم إلى كبتها. تدير مجموعتان من الإنزيمات هذا التوازن: ناقلات الأسيتيل على الهيستون تضيف مجموعات الأسيتيل، بينما مُزيلات أسيتيل الهيستون (HDACs) تزيلها. عندما يُخلّ هذا التوازن، يمكن أن يساهم ذلك في مجموعة واسعة من الأمراض بما في ذلك السرطان ومشاكل القلب وهزال العضلات واضطرابات المناعة.
لماذا يُعد HDAC5 هدفًا دوائيًا واعدًا لكنه معقَّد
تنتمي إنزيمات HDAC إلى عائلة كبيرة من الإنزيمات المتقاربة والمقسمة إلى عدة فئات. كثير من الأدوية الموجودة سريريًا تحجب أنواعًا عديدة من HDACs دفعة واحدة، ما قد يعيق وظائف طبيعية مهمة ويتسبب في آثار جانبية قوية. تبرز فئة IIa من HDACs، بما في ذلك HDAC5، لأنها غنية في أنسجة محددة مثل الدماغ والقلب والعضلات الهيكلية، وتتعاون مع بروتينات أخرى لتنظيم شبكات جينية رئيسية. غالبًا ما يعمل HDAC5 كجسر، يجلب إنزيمًا شريكًا شديد النشاط (HDAC3) إلى جينات معينة حتى يُحكَم الكروماتين وتُكبت هذه الجينات. وبسبب هذه الأدوار الموجهة، يُنظر إلى HDAC5 كهدف جذاب لأدوية أكثر انتقاءً، لكن هناك نقصًا في البيانات البيوكيميائية المفصلة ولا توجد بنية عالية الدقة لنواته الفعالة، ما يجعل تصميم الأدوية العقلاني صعبًا.
إعادة بناء HDAC5 في أنبوب اختبار
لمعالجة هذه الفجوة، أنتج الباحثون النواة الحفّازة فقط من HDAC5 البشري — الجزء الذي يُجري التفاعل الكيميائي — في بكتيريا، ونقَّوها، وتأكدوا من أنها تشكل بروتينًا مستقرًا ووحيد الوحدة في المحلول. ثم اختبروا مدى كفاءتها تحت مستويات ملح وحموضة مختلفة. بقيت نشاطية HDAC5 قوية عبر نطاق واسع من الملح وبلغت ذروتها في ظروف قاعدية خفيفة، مماثلة لتلك الموجودة داخل العديد من الخلايا. باستخدام جزيئات اختبار فلورية خاصة، وجدوا أن الشكل الطبيعي من HDAC5 يتعرّف على نوع واحد محدد فقط من الركائز المستخدمة عادة لفحص إنزيمات الفئة IIa. مستفيدين من أعمال سابقة على HDACs ذات صلة، استبدلوا حمض أميني واحد (الهستيدين) بتيروزين في موقع حرج. بشكل لافت، سمح هذا التغيير البسيط للنسخة الطافرة من HDAC5 بمعالجة كلا نوعي ركائز الاختبار بكفاءة، مكشوفًا كيف يوجّه بقاعدة واحدة في موقع الفعالية تفضيلات الإنزيم الكيميائية.
اختبار ومقارنة مرشحين دوائيين جديدين
بعد ذلك فحص الفريق جزيئين تجريبيين يثبّطان HDAC5، معروفين باسم NT160 وFFK24. تستخدم هذه المركبات مجموعة ربط جديدة للزنك تتجنب بعض سمية وقلة انتقائية الأدوية القديمة المبنية على الهيدروكسامات. بقياس مدى إبطاء كل مثبط لنشاط HDAC5 في تفاعلات مُتحكَّم بها بعناية، حدَّد المؤلفون ثوابت تثبيط منخفضة جدًا في مدى النانومولار، ما يعني أن كلا المركبين يرتبطان بقوة بالإنزيم. ارتبط NT160 باستمرار بقوة تقارب عشرة أضعاف أقوى من FFK24. لفهم السبب، استخدم الباحثون محاكاة ربط بمساعدة الحاسوب مع بنية نواة HDAC5 المتوقعة بواسطة AlphaFold. تشارك كلا المثبطين منطقة رأس مشتركة استقرت عميقًا داخل الجيب الفعّال وتلامست مع أيون المعدن، لكن ذيل NT160 كوَّن تلامسات إضافية مثبتة مع أحماض أمينية محددة في الجيب. هذه التفاعلات الإضافية تفسر على الأرجح فعاليته الأكبر.
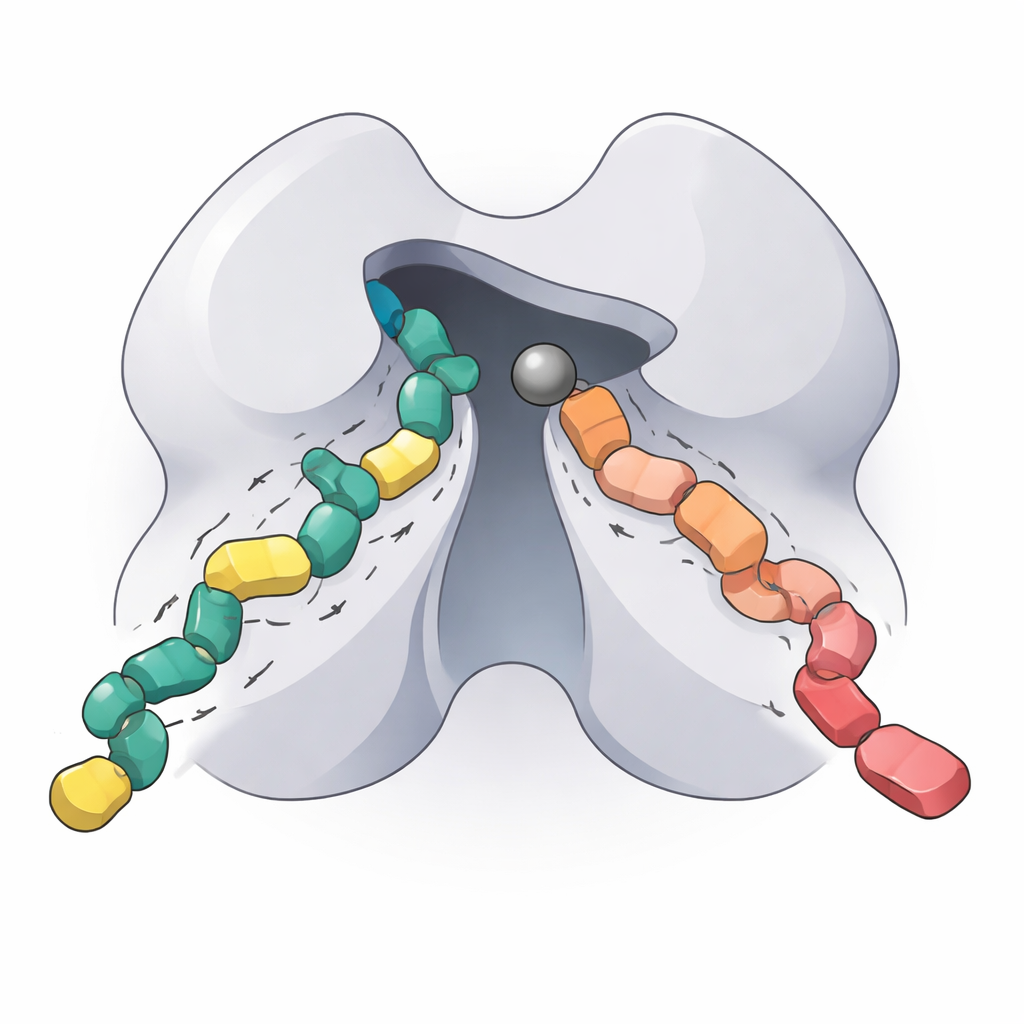
ما الذي يعنيه هذا لعلاجات موجَّهة مستقبلية
من خلال إعادة تجميع النواة العاملة لـ HDAC5، وتحديد ظروف عمله المثلى، وتفكيك كيفية تغيير سلوكـه بواسطة تغيير حمض أميني واحد، وقياس مدى ارتباط مثبطين من الجيل القادم، تقدّم هذه الدراسة "بصمة" بيوكيميائية مفصّلة لإنزيم مهم لكنه كان يفتقر إلى وصف كافٍ سابقًا. للخارجين عن التخصص، الخلاصة الأساسية هي أن HDAC5 يساعد في التحكم بما إذا كانت جينات معينة مُشغلة أم مطفأة، وأن ضبط هذا المفتاح بدقة قد يكون ذا قيمة في علاج أمراض القلب والتنكس العصبي والسرطان واضطرابات المناعة. يجب أن تساعد الرؤى والأدوات الجديدة المقدَّمة هنا الباحثين في تصميم أدوية انتقائية لـ HDAC5 والفئة IIa تعمل في المواقع المطلوبة مع تقليل التأثيرات غير المرغوب فيها في أجزاء أخرى من الجسم.
الاستشهاد: Mammen, C., Hornung, F.M., Anzenhofer, C. et al. In vitro characterization of the catalytic domain of human histone deacetylase 5. Sci Rep 16, 7935 (2026). https://doi.org/10.1038/s41598-026-37633-5
الكلمات المفتاحية: إزالة أستلة الهيستون 5, التنظيم فوق الجيني, مثبطات HDAC, علاج السرطان الموجَّه, بنية الكروماتين