Clear Sky Science · ar
تغيرات في نشاط EGFR بعد تعديل CRISPR/Cas9 لمجال ربط EGF
لماذا يهم إعادة توجيه إشارة سرطانية
غالبًا ما يعتمد سرطان عنق الرحم على مفتاح نمو قوي يُعرف بمستقبل عامل النمو البشري (EGFR). تمتلك العديد من الأورام أعدادًا هائلة من هذه المستقبلات، ومع ذلك فإن الأدوية المصممة لإيقافها أفادت جزءًا ضئيلاً فقط من المرضى. طرحت هذه الدراسة سؤالًا جوهريًا ذا انعكاسات علاجية كبيرة: ماذا يحصل إذا أزلت قدرة EGFR على التقاط إشارة النمو المفضلة له، عامل النمو البشرة (EGF)، من دون إزالة المستقبل نفسه؟
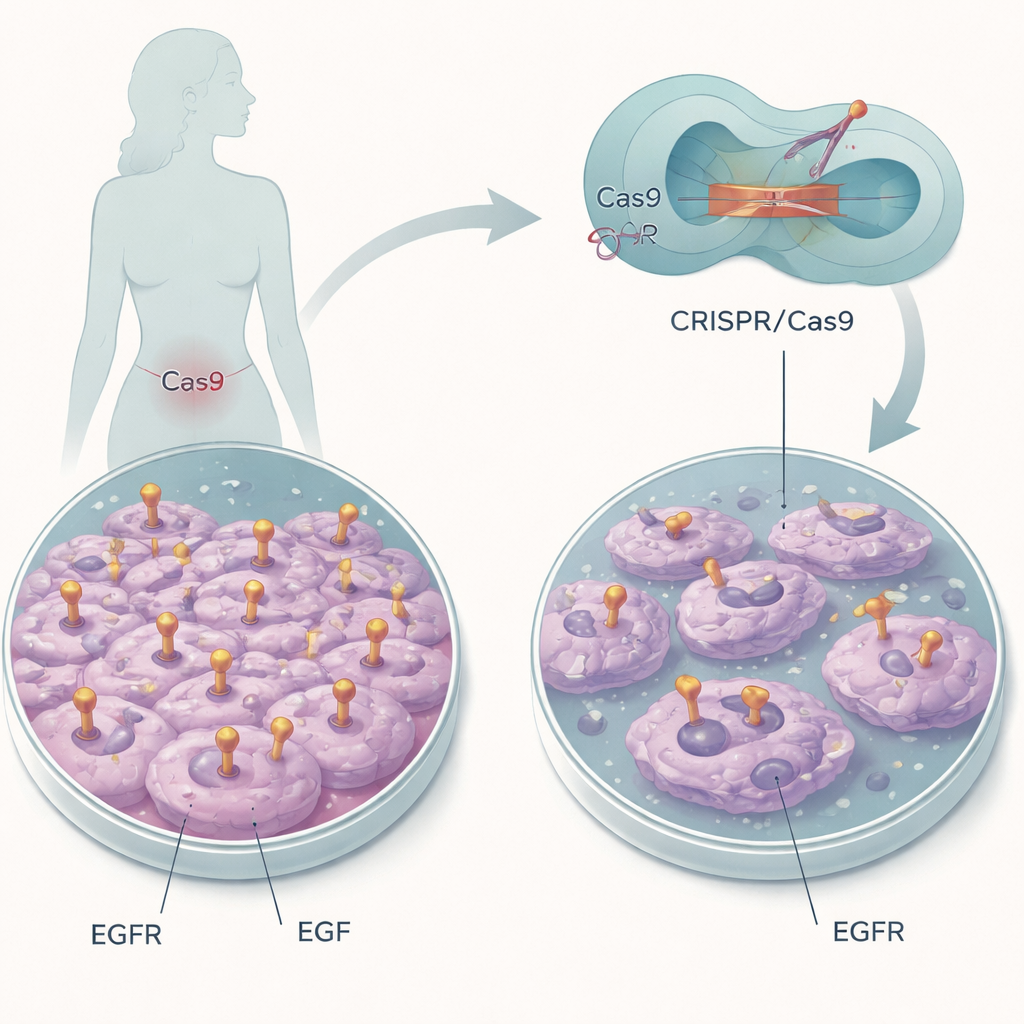
إطفاء «مفتاح التشغيل» الجزيئي
ركز الباحثون على سلالة خلوية لسرطان عنق الرحم تحمل كميات كبيرة من EGFR السليم غالبًا. بدلًا من تدمير الجين، استخدموا تحرير الجينوم CRISPR/Cas9 كجراحة دقيقة لتغيير عدد قليل من الأحماض الأمينية في جيب ربط EGF الخاص بـ EGFR. موقعان محددان، يطلق عليهما L14 وY45، يساعدان EGF على الالتحام بالمستقبل. من خلال استبدال هذين المكوّنَين بمكوّنات أخرى، هدفت المجموعة إلى إبقاء EGFR موجودًا لكنه أعمى أمام EGF، مما سمح لهم بعزل دور هذا التفاعل الفردي في سلوك الخلايا السرطانية.
بناء سلالات خلوية مصممة
في خطوة أولى، اختبر الفريق هذه الطفرات في خلايا باستخدام بلازميدات تُنتج مؤقتًا إما EGFR طبيعيًا أو معدلًا. كشف EGF الموسوم فلوريًا أن جميع النسخ الطافرة ارتبطت بLigand بدرجة أقل بكثير من المستقبل الطبيعي، خاصة عندما تغيرت L14 وY45 معًا. ثم أدخل الباحثون هذه التغييرات مباشرة في جينوم الخلايا السرطانية باستخدام CRISPR/Cas9، مولدين عدة نسخ خلوية جديدة. حملت بعض النسخ طفرة مفردة، في حين حملت أخرى الطفرة المزدوجة على نسخة EGFR واحدة وتغييرات معطلة على النسخة الأخرى. أظهرت نمذجة الحاسوب لأشكال البروتين الناتجة أن هذه التعديلات شوهت موقع الربط بما يكفي لإضعاف أو إلغاء التحام EGF، وهو ما يتوافق مع اختبارات الارتباط.
عندما يتحرك المستقبل لكن تبقى الخلايا حية
أظهرت التصويرات التفصيلية أن المستقبلات المعدلة تصرفت بشكل مختلف جدًا داخل الخلية. في الخلايا السرطانية غير المعدلة، يجلس EGFR على سطح الخلية، يلتقط EGF، ثم يتحرك إلى الداخل بينما ينشط كيميائيًا عبر الفسفرة. في النسخ الحاملة للطفرات المزدوجة، تكاد تختفي ارتباطات EGF ولم يُعد يُرى EGFR على الغشاء؛ بدلاً من ذلك، تراكمت الكمية الصغيرة المتبقية من المستقبل داخل الخلية. حتى تغيير واحد في Y45 خفّض الارتباط بشكل كبير وخفّض مستويات EGFR الإجمالية. ومع ذلك، ورغم هذا التعطيل لمسار الإشارة التقليدي EGF–EGFR، بقيت الخلايا السرطانية قابلة للحياة واستمرت في النمو في الثقافة مع تغيّرات متواضعة فقط في أنماط دورة الخلية.
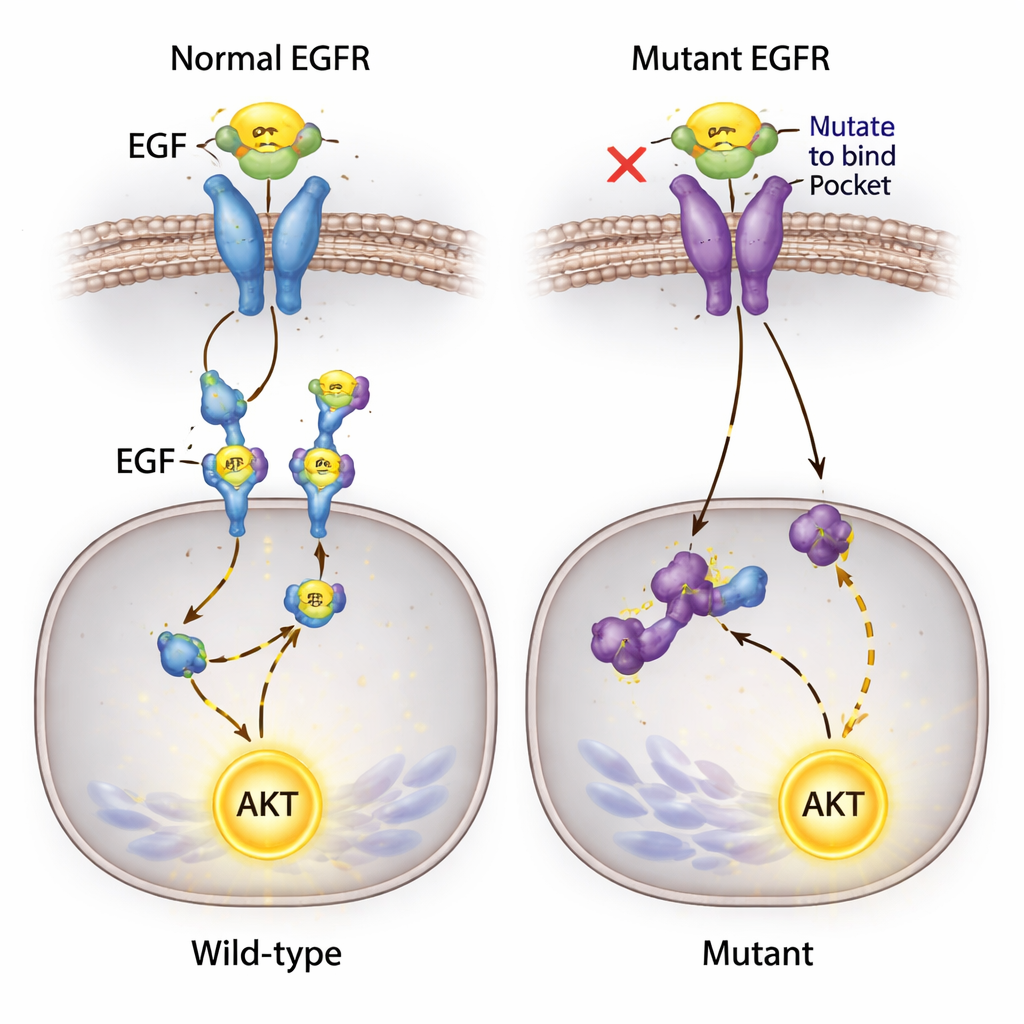
إشارة غير متوقعة لا تتوقف
إحدى النتائج الأكثر دهشة شملت بروتينًا رئيسيًا يدعم بقاء الخلية يُدعى AKT، والذي عادةً ما ينشط ضمنيًا بعد EGFR. توقع الباحثون أن حجب ارتباط EGF–EGFR سيُسكت هذا المسار. بدلًا من ذلك، عندما أُضيف EGF إلى الوسط، نشط AKT بقوة في جميع الخطوط الخلوية — بما في ذلك تلك التي لم يعد بإمكان EGF الالتحام بـ EGFR فيها والتي لم تُظهر فسفرة للمستقبل. وبما أن هذه الخلايا تحمل طفرة معروفة في جين إشاري آخر، PIK3CA، يشتبه الفريق أن مسارات بديلة قد تسمح لـ EGF بالمساهمة في تفعيل AKT، ربما عبر بروتينات سطحية أخرى أو طفرات خلفية، متجاوزةً EGFR المعدل.
تغييرات جينية خفية والعلاجات المستقبلية
للتأكد من أن CRISPR لم يتسبب في تعديلات غير مقصودة على نطاق واسع، نسخ العلماء الجينومات الكاملة للنسخ الخلوية الجديدة. أكدوا وجود طفرات EGFR المطلوبة ولم يجدوا دليلًا على قصات في مواقع خارج الهدف المتوقعة لأدلة CRISPR. مع ذلك، اكتشفوا العديد من الطفرات التلقائية المبعثرة عبر الجينوم، بعضها قد يؤثر في سلوك الخلايا. يسلط هذا الضوء على أن حتى عندما يصيب CRISPR العنوان المقصود، فإن الحمض النووي غير المستقر للخلايا السرطانية يمكن أن يعقّد تفسير النتائج التجريبية وتصميم علاجات جينية دقيقة.
ماذا يعني هذا للمرضى
للغير متخصص، الخلاصة أن مجرد إيقاف المصافحة بين EGF وEGFR — حتى بدقة ذرية — لا يوقف تلقائيًا خلايا السرطان عن تلقي أوامر "النمو والبقاء". تظهر الدراسة أن الخلايا السرطانية قادرة على إعادة توجيه إشارات رئيسية مثل تفعيل AKT حول مستقبل محجوب، وأن تعديل CRISPR نفسه يجب تقييمه بعناية في مثل هذه الجينومات غير المستقرة. توفر هذه الخلايا الهندسية الآن نموذجًا مختبريًا قويًا للبحث عن المسارات الاحتياطية التي تحافظ على الأورام المعتمدة على EGFR، وهي معلومات قد تؤدي في النهاية إلى علاجات مركبة تستهدف كلًا من EGFR وشركائه المخفيين.
الاستشهاد: Popović, J., Hahut, A., Torres, G.E. et al. Changes in EGFR activity following CRISPR/Cas9-editing of the EGF binding domain. Sci Rep 16, 6797 (2026). https://doi.org/10.1038/s41598-026-37579-8
الكلمات المفتاحية: EGFR, سرطان عنق الرحم, CRISPR, إشارة EGF, مسار AKT