Clear Sky Science · ar
تكاثر نسخ الجين يدفع فرط التعبير عن IFI30 وتنشيطًا منسقًا للمناعة، محددًا هدفًا تشخيصيًا وعلاجيًا جديدًا في سرطان غدة المعدة
لماذا تهم بروتينات المعدة
يعد سرطان المعدة من أكثر السرطانات فتكا في العالم، ويرجع ذلك إلى حد كبير إلى اكتشافه المتأخر وصعوبات علاجه. تركز هذه الدراسة على بروتين غير معروف على نطاق واسع يدعى IFI30، يوجد في خلايا تساعد جهاز المناعة على التعرف على المهددات. من خلال تتبُّع كيفية تغير IFI30 في أورام المعدة وكيف يشكل دفاعات الجسم، يقترح الباحثون أنه قد يصبح أداة قوية للتشخيص المبكر وللاختيار الأفضل للعلاجات المخصصة والفعالة.
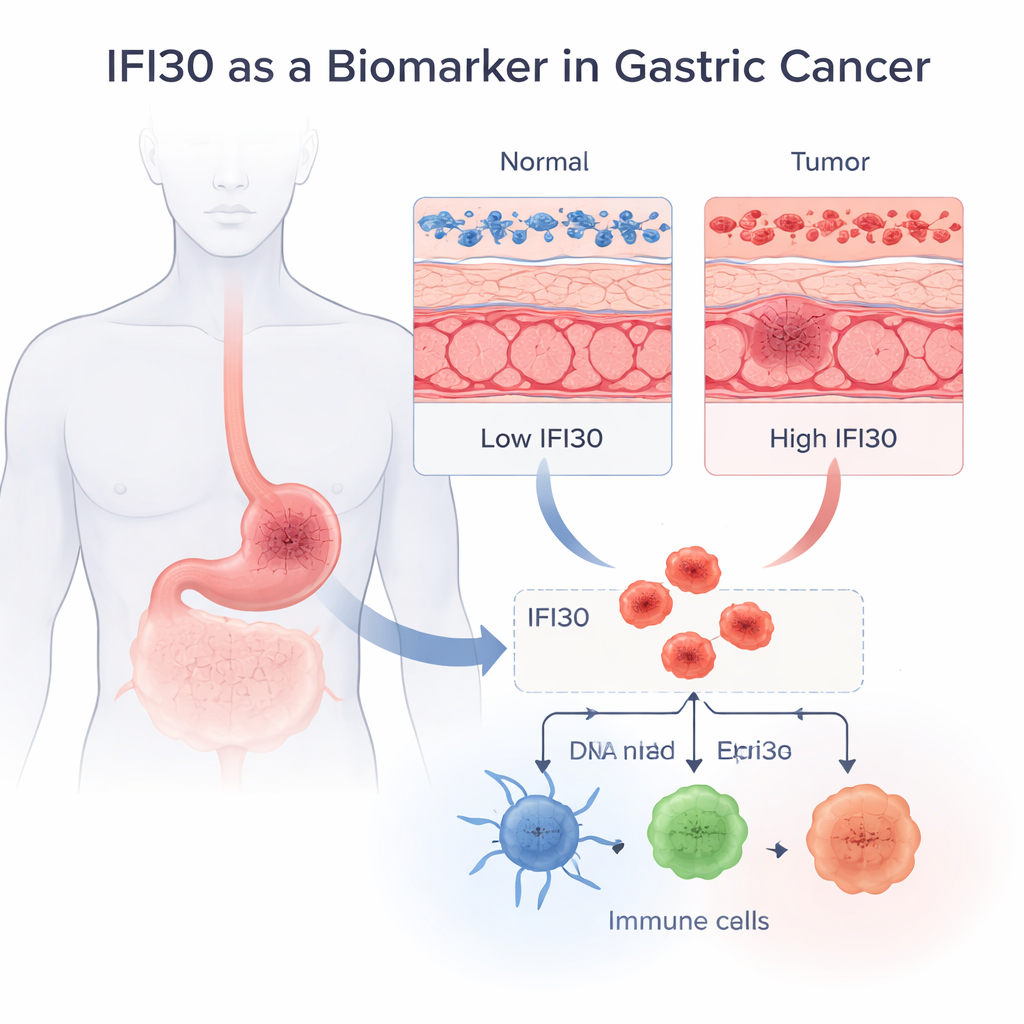
إشارة مخفية في أورام المعدة
بدأ الفريق بطرح سؤال أساسي: هل يوجد IFI30 بمستويات مختلفة في نسيج المعدة السليم مقارنةً بالنسيج السرطاني؟ باستخدام مجموعات بيانات عامة واسعة تجمع نشاط الجينات من آلاف العينات، وجدوا أن IFI30 أعلى باستمرار في سرطان غدة المعدة — أكثر أنواع سرطان المعدة شيوعًا — مقارنةً ببطانة المعدة الطبيعية. وقد تَبَيَّن هذا عبر مجموعات مرضى مستقلة متعددة وعلى مستويي الرنا والبروتين. وعند اختبار مدى قدرة IFI30 وحده على تمييز النسيج الورمي عن النسيج السليم، كانت أداؤه ملحوظًا: دقة تشخيصية (AUC) بمقدار 0.92، وهو مستوى ممتاز لعلامة واحدة. كما وضعت صور المجهر IFI30 داخل نظام إعادة التدوير الداخلي للخلية، حيث تُعالَج المستضدات لتعرضها على جهاز المناعة.
تغيرات الحمض النووي التي ترفع IFI30
بعد ذلك، بحث الباحثون عن سبب ارتفاع مستوى IFI30 في هذه الأورام. عبر فحص جينومات السرطان من مرصد جينوم السرطان (TCGA)، وجدوا أن النسخ الإضافية من جين IFI30 — المعروفة بتكبير عدد النسخ — كانت المحرك الرئيسي لفرط التعبير عنه. تميل الأورام التي لديها تضخيم في IFI30 إلى إظهار عدم استقرار جينومي أكبر عمومًا وغالبًا ما تحمل طفرات معروفة مثل TP53 وPIK3CA. ومع زيادة عدد نسخ IFI30، ارتفعت أيضًا مستويات الرنا الخاصة به، مما يوحي بوجود صلة مباشرة بين التغيرات الهيكلية في الحمض النووي وزيادة إنتاج هذا البروتين. يضع هذا IFI30 ليس كمجرد مراقب سلبي، بل كجزء من نمط أوسع من سلوك الورم العدواني.
تواصل مناعي حول الورم
نظرًا لارتباط IFI30 بمعالجة المواد التي تعرضها خلايا الجهاز المناعي كـ «ملصقات مطلوب القبض عليها» لخلايا T، استكشف الفريق موقعه داخل البيئة الدقيقة للورم. أظهر التسلسل خلية بخلية، الذي يقرأ تعبير الجينات في الخلايا الفردية، أن IFI30 غني بشكل خاص في الخلايا الشجرية (dendritic cells) والبلعمية (macrophages) وخلايا T CD8 — وهي لاعبون أساسيون في إطلاق والمحافظة على المناعة ضد الأورام. كشفت تحليلات الشبكات عن تواصل مكثف بين الخلايا المناعية الغنية بـ IFI30 والخلايا الورمية والخلايا الداعمة المحيطة. أظهرت الأورام ذات المستويات العالية من IFI30 تنشيطًا قويًا للمسارات المرتبطة بعرض المستضدات، والإشارات الالتهابية، وجزيئات التواصل التي تجذب وتنظم الخلايا المناعية. وفي الوقت نفسه، عرضت هذه الأورام سمات غزو وإجهاد، مثل تسارع دورة الخلية، وإعادة تشكيل النسيج، والتكيف مع نقص الأكسجة، ما يبرز دور IFI30 عند تقاطع الهجوم والدفاع داخل السرطان.
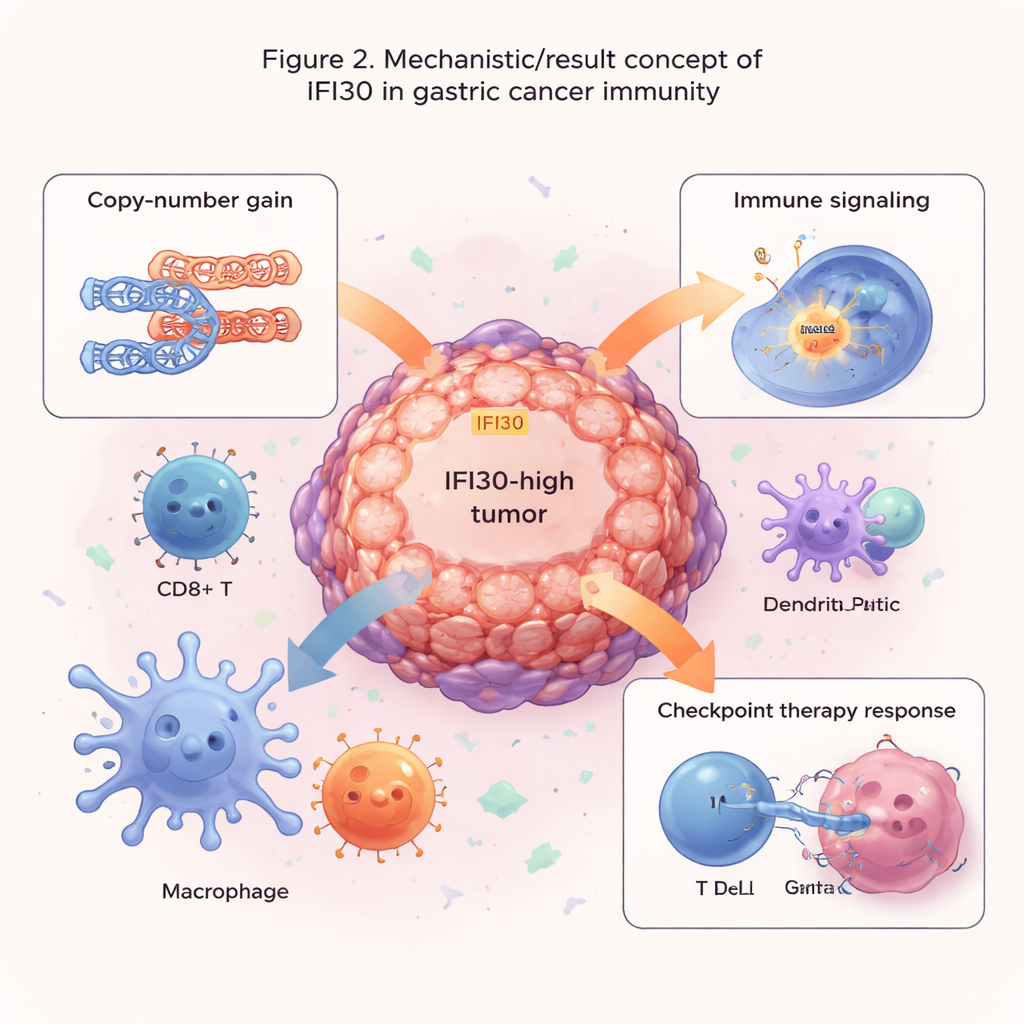
مؤشرات لاختيار الأدوية والعلاج المناعي
ثم تساءل المؤلفون عما إذا كان IFI30 يمكن أن يساعد في التنبؤ بكيفية استجابة الأورام للعلاج. بمزاوجة مستويات IFI30 مع مجموعات بيانات استجابة للأدوية واسعة، وجدوا أن الأورام ذات IFI30 العالي تميل إلى مقاومة بعض الأدوية التي تستهدف انقسام الخلايا أو مسار نمو شائع (MAPK)، لكنها تظهر حساسية أكبر للأدوية التي تحجب إشارات EGFR وPI3K/AKT. ومن اللافت أن مستويات IFI30 ارتبطت ارتباطًا وثيقًا بـ PD-L1، المكبح الرئيسي لخلايا T والذي تستهدفه مثبطات نقاط التفتيش الحالية. عبر عدة دراسات علاج مناعي، كان المرضى الذين تحمل أورامهم تعبيرًا أعلى عن IFI30 أكثر احتمالًا للاستجابة لحجب نقاط التفتيش مقارنةً بمن لديهم مستويات منخفضة. تفوق مقياس يستند إلى IFI30 على مقاييس راسخة مثل عبء الطفرات في الورم وPD-L1 بمفرده، وكان غنيًا بشكل خاص في الأورام ذات عدم الاستقرار الدقيق العالي (MSI)، وهي فئة معروفة بالفعل باستجابتها الأفضل للعلاج المناعي.
من المختبر إلى هدف محتمل جديد
لاختبار ما إذا كان IFI30 مجرد علامة أم يساهم أيضًا في نمو السرطان، خفض الفريق مستوياته في خطوط خلايا سرطان المعدة باستخدام أدوات جينية. عندما تم تقليل IFI30، نمت الخلايا السرطانية بشكل أبطأ، مشيرةً إلى دور مباشر في دعم تكاثر الورم. مجتمعة، تشير البيانات إلى أن IFI30 هو كل من مؤشر لنشاط المناعة ومساهم في السلوك الخبيث. وللمرضى، يعني هذا أن قياسًا بسيطًا لـ IFI30 قد يساعد يومًا ما الأطباء على اكتشاف سرطان المعدة بمزيد من الدقة، والتنبؤ بمن قد يستفيد من أدوية مستهدفة أو علاجات مناعية معينة، وربما توجيه علاجات جديدة تمنع مباشرة أو بشكل غير مباشر الأفعال المشجعة للورم التي يقوم بها IFI30.
الاستشهاد: Liu, Q., Yuan, W., Zhaowang, R. et al. Copy-number amplification drives IFI30 overexpression and coordinated immune activation, identifying a novel diagnostic and therapeutic target in gastric adenocarcinoma. Sci Rep 16, 6945 (2026). https://doi.org/10.1038/s41598-026-37574-z
الكلمات المفتاحية: سرطان المعدة, IFI30, مؤشر حيوي, مناعة الورم, العلاج المناعي