Clear Sky Science · ar
نهج إنزيم البيوتين المنقسم يكشف البروتينات المرتبطة بألفا-سينوكلين الأديكّ أثناء التجمع
لماذا تهم البروتينات المتكتلة في الدماغ
في داء باركنسون والحالات المرتبطة به، يمكن لبروتين دماغي مفيد عادة يسمى ألفا‑سينوكلين أن يتجمع إلى رواسب لزجة تُعرف بأجسام ليوي. تظهر هذه الرواسب قبل عقود من ظهور الأعراض وتُعد سمة مميزة تُرى عند التشريح بعد الوفاة، ومع ذلك لا نعرف بعد أي البروتينات الأخرى تساعد في دفع ألفا‑سينوكلين من حالة غير ضارة إلى تجمعات ضارة. تستخدم هذه الدراسة علامة جزيئية ذكية «للقرب» لرسم خرائط البروتينات التي تقطن بجوار ألفا‑سينوكلين أثناء تحوله من جزيئات مفردة إلى تكتلات صغيرة، مما يقدّم دلائل جديدة حول كيفية بدء المرض والمسارات التي قد تُستهدف لإبطاءه أو منعه.
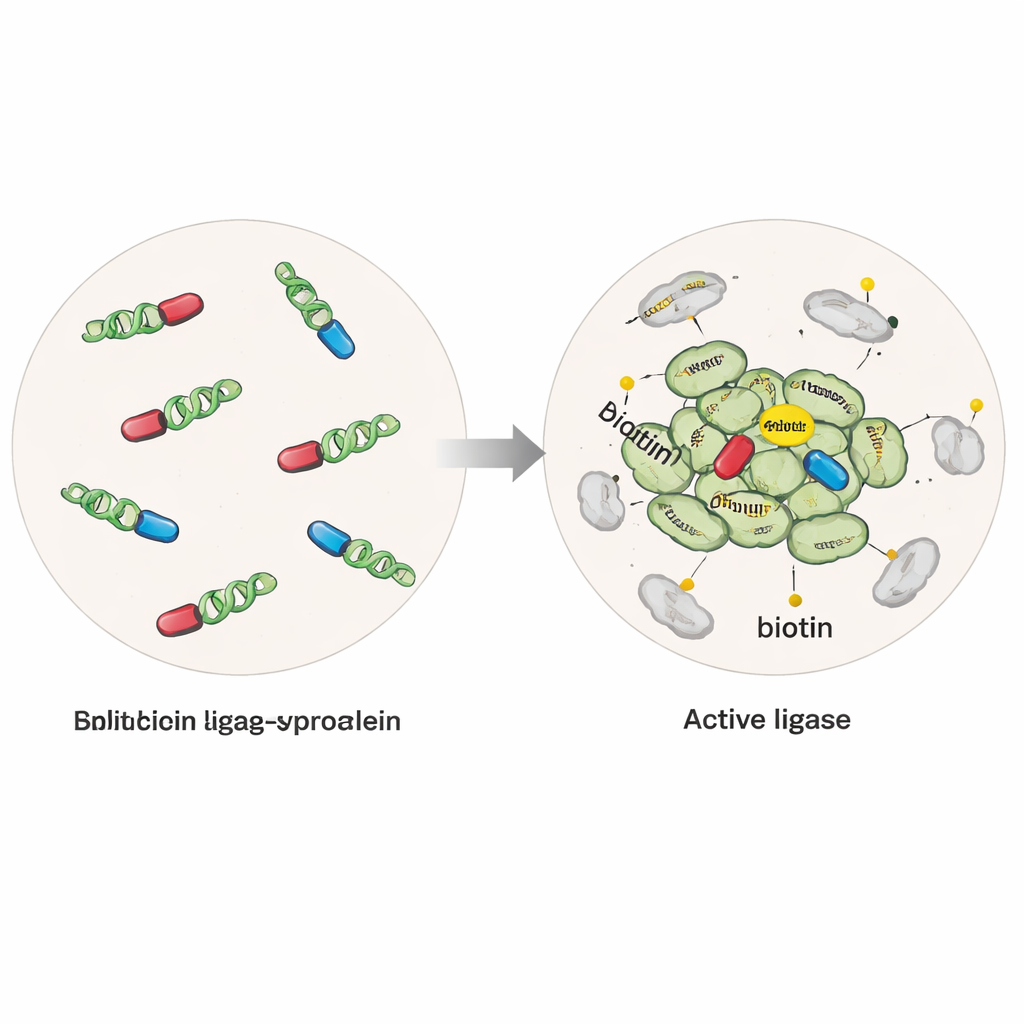
«علامة» جزيئية تُضيء الجيران
هندس الباحثون خلايا بشرية لتُنتج ألفا‑سينوكلين المُلتحمة بأنزيم معدل يمكنه ربط وسم صغير من البيوتين بأي بروتين يقع ضمن بضع مليارات من الأمتار. في أحد النسخ، كان الأنزيم سليمًا ونشطًا كلما وُجد ألفا‑سينوكلين، فالتقط البروتينات القريبة من الجزيئات المفردة وكذلك التكتلات. في نسخة ثانية أكثر انتقائية «منقسمة»، قُطع الأنزيم إلى نصفين غير نشطين، كل منهما مُلتحم بجزيء منفصل من ألفا‑سينوكلين. فقط عندما تجمعت جزيئات ألفا‑سينوكلين معًا إلى متعددات أو أوليغومرات أعيدت النِصْفَان لتكوين أنزيم نشط، فأُنشئت الوسم تحديدًا حول هذه التجمعات المبكرة. بإضافة خيوط ألفا‑سينوكلين المصفاة إلى الخلايا، تمكن الفريق أيضًا من دفع التجمع الشبيه بالمرض ومقارنة الحالات الطبيعية مقابل الحالات المرضية.
بناء خريطة للبروتينات القريبة
بعد منح وقت كافٍ لوضع الوسوم، سحب الفريق كل البروتينات الموسومة بالبيوتين وحددها باستخدام مطيافية الكتلة، وهي تقنية تزن وتعد البروتينات بدقة عالية. عبر كل الظروف وجدوا 1277 بروتينًا مميزًا، وبعد تصفية دقيقة ضيّقوا هذه القائمة إلى 581 احتمالًا لأن تكون فعلًا قريبة من ألفا‑سينوكلين. بمقارنة نظاميّ الأنزيم السليم والمنقسم، استطاعوا تمييز البروتينات التي ترتبط أساسًا بالجزيئات المفردة عن تلك التي تفضل متعددات الجزيئات. كما قارنوا خلايا بوجود وخلوّ خيوط مضافة لرؤية كيف يتغير محيط البروتين المحلي لألفا‑سينوكلين عند تحفيز التجمع.
مسارات خلوية رئيسية تُسحب إلى التكتلات
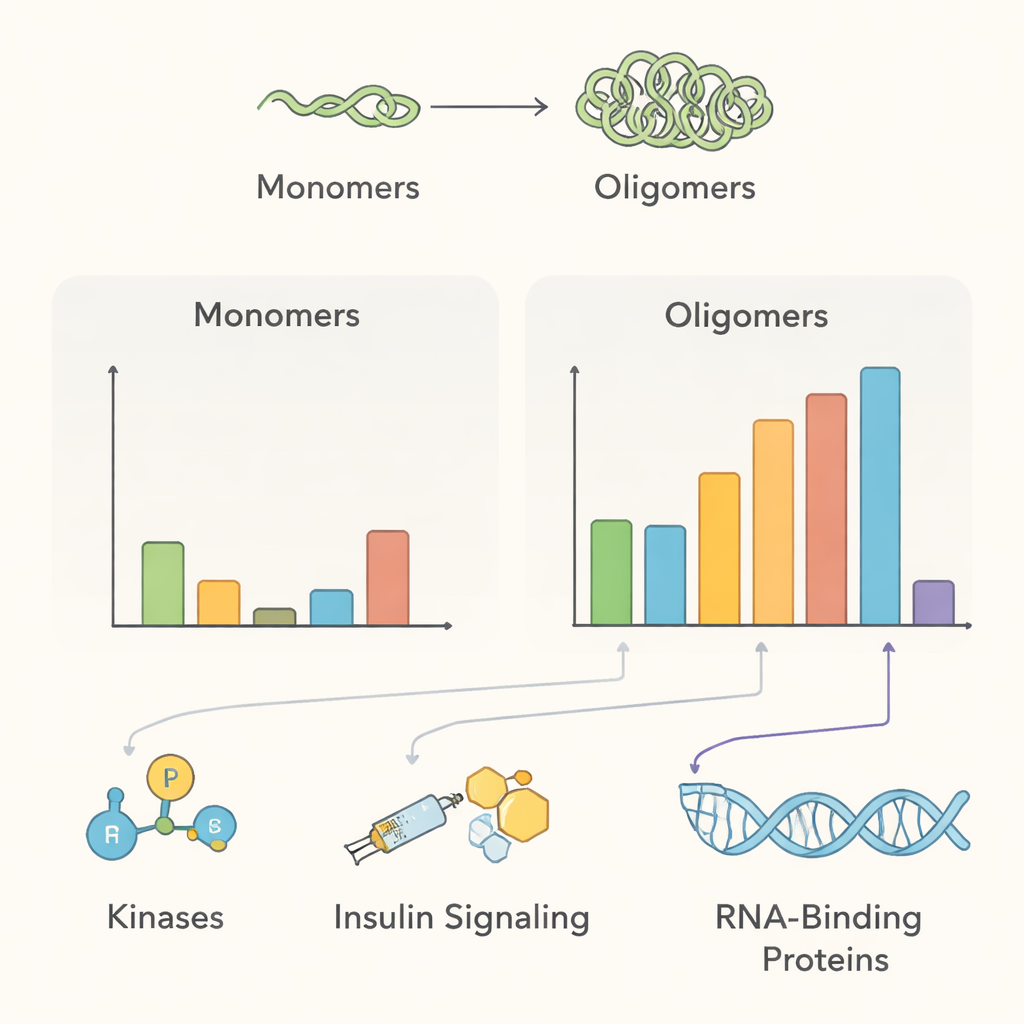
تشير خريطة التفاعلات الناتجة إلى عدة مواضيع بيولوجية رئيسية. في الظروف الطبيعية، كان ألفا‑سينوكلين متعدد التركيب قريبًا من العديد من بروتينات نقل الأغشية وإنزيمات تعديل البروتين — وهو ما يتوافق مع دوره المقترح في مساعدة الخلايا العصبية على إدارة الحويصلات المشبكية والحفاظ على مراقبة جودة البروتين. وُجدت العديد من الإنزيمات التي تضيف مجموعات الفوسفات، بما في ذلك الكينازات PAK4 وRIPK2 وMAP4K4، بكثرة بالقرب من متعددات صحية لكنها بدا أنها تفقد الاتصال بمجرد تكوّن التكتلات، مما يلمّح إلى أن تعطّل هذه العلاقات قد يُفضّل الأشكال المرتبطة بالمرض من البروتين. كما اكتشف الفريق بروتينات مرتبطة بإشارة عامل النمو الشبيهة بالإنسولين، داعمةً الروابط السريرية بين مقاومة الإنسولين ومرض باركنسون، ووجد أن التجمع يستقطب بروتينات مشاركة في التخلص من البروتينات التالفة، مثل عائلة الشابرون 14‑3‑3 ومكونات محددة من مسارات التحلل الخلوي.
جسور مفاجئة إلى اضطرابات دماغية أخرى
بعيدًا عن مرض باركنسون، تبرز البيانات ارتباطًا مفاجئًا بالتصلب الجانبي الضموري (ALS) والخرف الجبهي الصدغي (FTD). بدا بروتين ربط الرنا المسمى FUS، الذي يتحرّك للمواضع الخاطئة ويتجمع في تلك الحالات، قريبًا من ألفا‑سينوكلين متعدد التركيب في كل من الحالات الطبيعية وتحت ظروف تحفيز التجمع. كما تغيّرت قرب بروتينات مرتبطة بالرنا الأخرى مع تجمع ألفا‑سينوكلين. تثير هذه النتائج احتمال أن تجمعات صغيرة من ألفا‑سينوكلين قد تحاصر بروتينات معالجة الرنا في أماكن خاطئة داخل الخلايا، ما قد يربط بيولوجيا أمراض أجسام ليوي بتلك الخاصة بALS وFTD، رغم أن التفاعلات الفيزيائية المباشرة لا تزال بحاجة إلى التحقق.
ما الذي يعنيه هذا لفهم المرض
بالنسبة لغير المتخصصين، الخلاصة الرئيسية هي أن هذا العمل يقدّم «قائمة اتصالات» في مرحلة مبكرة للبروتينات التي ترافق ألفا‑سينوكلين أثناء تحوله من مساعد طبيعي إلى تكتل ضار. تشير الدراسة إلى أن فقدان علاقات حمائية معينة — مثل تلك مع كينازات محددة أو إنزيمات مراقبة الجودة — قد يكون مهمًا بقدر أهمية كسب شركاء سُمّيين جدد. وعلى الرغم من أن التجارب أُجريت في نموذج خلوي مبسط ولا تثبت بعد السبب والنتيجة، فإنها تبرز مرشحين ومسارات ملموسة للاختبار المستقبلي في الخلايا العصبية وأنسجة الدماغ. على المدى الطويل، قد توجه خرائط هذه الأحياء البروتينية المتغيرة استراتيجيات لاستعادة التفاعلات الوقائية، ودعم إشارات متعلقة بالإنسولين، أو منع احتجاز بروتينات ربط الرنا، بما قد يبطئ الانتقال من تغيّرات جزيئية طفيفة إلى أمراض أجسام ليوي كاملة التطور.
الاستشهاد: Fernandes, A.R., Owen, A.P., Faroqi, A.H. et al. A split biotin ligase approach reveals proteins associated with oligomeric alpha-synuclein during aggregation. Sci Rep 16, 7270 (2026). https://doi.org/10.1038/s41598-026-37551-6
الكلمات المفتاحية: ألفا-سينوكلين, مرض ليوي, تجمع البروتينات, بروتيوميات القرب, مرض باركنسون