Clear Sky Science · ar
تفاعل الحقل الكهرمغناطيسي النبضي منخفض التردد (PEMF) مع الميتوكوندريا
حقول لطيفة ومحطات طاقة الخلايا
يُستخدم علاج الحقل الكهرمغناطيسي النبضي (PEMF) حالياً في العيادات للمساعدة على رتق العظام المكسورة، وتخفيف آلام المفاصل، وتسريع التعافي بعد الجراحة. ومع ذلك ما زلنا لا نفهم تماماً كيف تؤثر هذه الحقول اللطيفة منخفضة التردد داخل أجسامنا. تطرح هذه الدراسة سؤالاً أساسياً لكنه مهم: هل تؤثر إشارات PEMF مباشرة على الميتوكوندريا، وهي محطات الطاقة الصغيرة داخل خلايانا التي تولّد معظم طاقتنا، وإذا كان الأمر كذلك فكيف؟
لماذا تهم الميتوكوندريا للصحة اليومية
تحول الميتوكوندريا الطعام والأكسجين إلى جزيء ATP، عملة الطاقة «العالمية» في الخلايا. عندما تتعطل الميتوكوندريا، يلتئم النسيج أبطأ، وتتعب العضلات بسرعة أكبر، وقد تتفاقم الأمراض المرتبطة بسوء الأيض. وبما أن أبحاثاً سابقة لمّحت إلى أن علاجات PEMF تحسّن التمثيل الغذائي للطاقة وتدعم إصلاح الأنسجة، ركّز الباحثون على ما إذا كان جهاز PEMF محدد يمكنه ضبط نشاط الميتوكوندريا. استعملوا إشارة مغناطيسية محددة جيداً: نبضات قصيرة بطول ميلي ثانية لموجة جيبية بتردد 30 كيلوهرتز وطاقة دخل منخفضة، طُبقت على خلايا عضلية مزروعة، وأنسجة من جرذان، وميتوكوندريا منقاة.
نظرة أقرب داخل الخلايا الحية
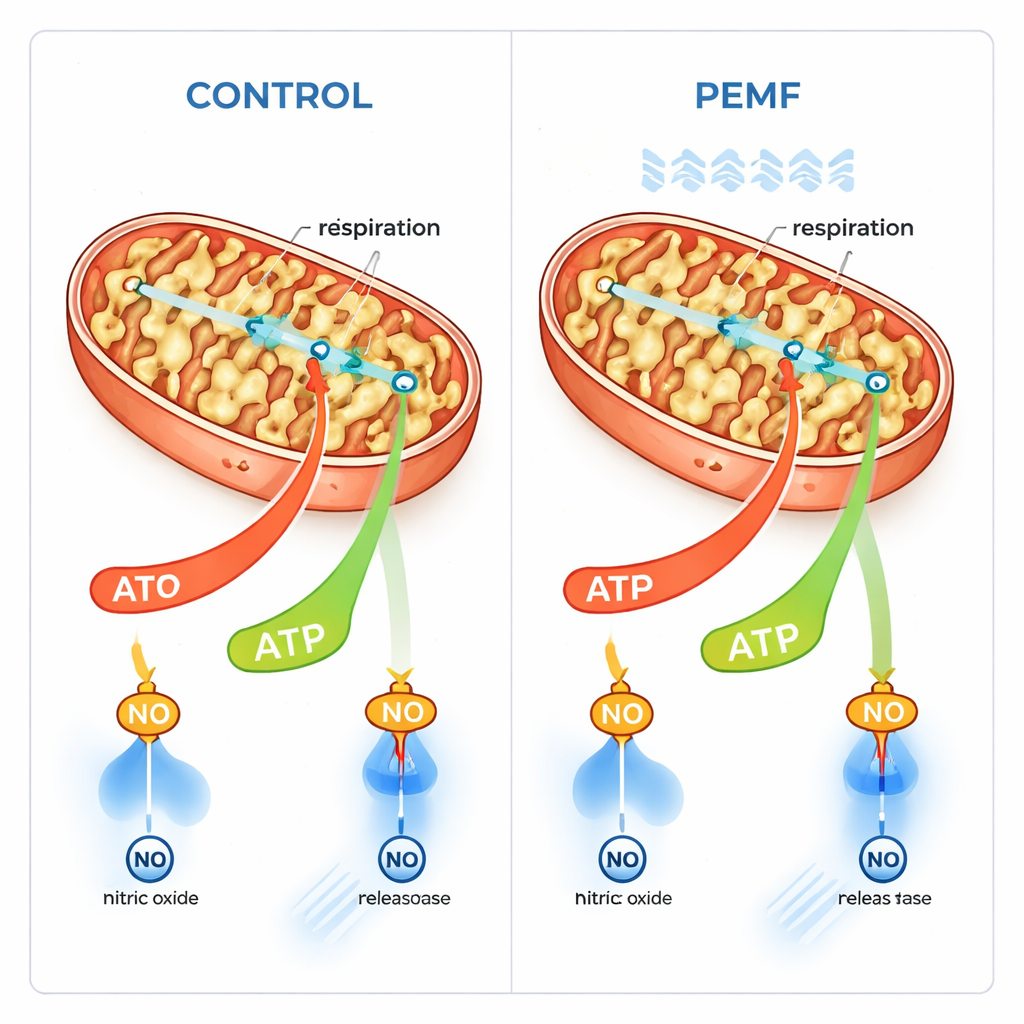
في خلايا عضلية بشرية نمت في المختبر، قاس الفريق ثلاثة مؤشرات رئيسية بعد التعرض لـ PEMF: الجهد الكهربائي عبر الغشاء الداخلي للميتوكندريا (نوع من البطارية الصغيرة)، ومستويات الأنواع التفاعلية للأكسجين (مستويات مرتفعة قد تكون ضارة)، وأكسيد النيتريك، الغاز الذي يمكن أن يعيق مؤقتاً تنفّس الميتوكوندريا. نحو 90 دقيقة بعد العلاج، كان الجهد الغشائي الميتوكوندري أقل بشكل طفيف، بينما انخفضت مستويات أكسيد النيتريك؛ أما الأنواع التفاعلية للأكسجين فلم تزداد. قد يشير الانخفاض الطفيف في الجهد الغشائي إما إلى تلف أو إلى إنتاج ATP بوتيرة أعلى. وبما أن الخلايا لم تُظهر علامات إجهاد، اشتبه المؤلفون بأن الميتوكوندريا كانت تعمل ببساطة بسرعة أكبر وتستهلك الفولتية المخزنة عبر غشائها الداخلي.
اختبار كيفية تنفّس الميتوكوندريا
لاختبار هذه الفكرة بصورة مباشرة أكثر، أحدث الباحثون ثقوباً لطيفة في الغشاء الخلوي الخارجي حتى يتمكنوا من تزويد الميتوكوندريا بوقودات مختلفة بدقة وقياس استخدام الأكسجين. لاحظوا اتجاهات ثابتة نحو تنفّس أعلى مرتبط بتوليد ATP بعد التعرض لـ PEMF، خاصة عند وجود الغلوتامات، وهو وقود شائع للميتوكندريا. وأشارت التحليلات الإحصائية عبر عينات كثيرة إلى أن تداخل التعرض لـ PEMF ونوع الوقود يشكلان بشكل ملحوظ سرعة استهلاك الميتوكوندريا للأكسجين. والأهم من ذلك أنه لم تكن هناك إشارة إلى أن PEMF أضرّ بالخلايا أو بالميتوكوندريا. بدل ذلك، بدا أن الحقول تحفّز انتقائياً وضعية التنفّس «المرتبطة» حيث يرتبط استخدام الأكسجين ارتباطاً وثيقاً بصنع ATP، دون زيادة الاحتراق غير المرتبط والمهدر للوقود.
الالتهاب، أكسيد النيتريك، ومفاجأة الضوء الأزرق
بما أن أكسيد النيتريك يمكن أن يتراكم أثناء الالتهاب ويعيق خطوة رئيسية في تنفّس الميتوكوندريا، تساءل الفريق عمّا إذا كان PEMF يمكن أن يساعد الميتوكوندريا على التعافي من مثل هذا التثبيط. أضافوا مادة مانحة لأكسيد النيتريك إلى معاجين أنسجة العضلات والكبد وميتوكوندريا كبد معزولة، مما أبطأ التنفّس بشكل كبير. في هذه الظروف، لم يستعد PEMF وظيفة الميتوكوندريا، حتى عندما كانت الميتوكوندريا مركزة بكثافة. ولمعرفة ما إذا كان الانسداد قابلاً للعكس على الإطلاق، سلطوا ضوءاً أزرق على الميتوكوندريا المثبطة بأكسيد النيتريك، مستخدمين طريقة معروفة بإزاحة أكسيد النيتريك من موقع ارتباطه. أتاح الضوء الأزرق تعافياً جزئياً للتنفس، مؤكداً أن النظام يمكن أن يعود، لكن PEMF لم يضف أي فائدة إضافية. بيّن هذا أن التأثيرات الإيجابية لـ PEMF لا تنبع من إزالة أكسيد النيتريك في ظروف شبيهة بالالتهاب.
بوابات الغشاء وتدفّق الطاقة
باستخدام تشبيه بين الخلايا والدارات الكهربائية، يقترح المؤلفون أن PEMF قد يعمل بصورة رئيسية على الأغشية البيولوجية. تَحيط بالميتوكوندريا غشاء خارجي يحتوي على بروتين بوابة رئيسي يُدعى VDAC، الذي يسمح لجزيئات مرتبطة بالطاقة بالمرور من وإلى الداخل. على عكس الجهد العالي جداً للغشاء الداخلي، يتمتع الغشاء الخارجي بجهد أصغر وأكثر عرضة للتأثر. يقترح المؤلفون أن PEMF يغيّر بشكل طفيف هذا الجهد الغشائي الخارجي، مؤثراً على تكرار فتح بوابات VDAC وبذلك يسهل تدفق الوقود وATP المستنفد عبر الغشاء. وهذا من شأنه أن يعزّز بطبيعة الحال نمط التنفّس المرتبط بصنع ATP دون تغيير القدرة القصوى لآلية نقل الإلكترون نفسها.
ما يعنيه هذا للعلاجات المستقبلية
بشكل عام، تجد الدراسة لا أدلة على أن هذا النوع من PEMF يضر بالميتوكوندريا. على العكس، يعزّز PEMF بهدوء الجزء من تنفّس الميتوكوندريا الذي يُنتج ATP، مع إبقاء القدرة التنفّسية القصوى والإجهاد التأكسدي دون تغيير. ومع ذلك، فهو لا يُنقذ الميتوكوندريا المحجوزة بفعل أكسيد النيتريك المرتفع، ما يشير إلى أن فوائده في الأنسجة الملتهبة يجب أن تنشأ عبر مسارات أخرى. بالنسبة للمرضى والأطباء، تدعم هذه النتائج فكرة أن المجالات الكهرومغناطيسية المصممة بعناية يمكن أن تدفع محطات طاقة الخلية نحو حالة أكثر كفاءة في إنتاج الطاقة — مما يقدّم تفسيراً آلياً معقولاً لبعض تأثيرات الشفاء المبلغ عنها في ترميم العظام، ورعاية الجروح، والتعافي بعد الجراحة.
الاستشهاد: Zavadskis, S., Gasser, A.S., Karas, M. et al. Interaction of pulsed low frequency electromagnetic field (PEMF) with mitochondria. Sci Rep 16, 6681 (2026). https://doi.org/10.1038/s41598-026-37527-6
الكلمات المفتاحية: علاج الحقل الكهرمغناطيسي النبضي, الميتوكوندريا, طاقة خلوية, أكسيد النيتريك, إنتاج ATP