Clear Sky Science · ar
نموذج تعلّم عميق قابل للتطبيق سريرياً وقابل للتعميم للأورام الأمامية للمنصف في صور الأشعة المقطعية عبر مؤسسات متعددة
لماذا يهم اكتشاف الأورام النادرة في الصدر
غالباً لن نسمع مصطلح «ورم المنصف الأمامي» في العيادة، لأن هذه الأورام—التي غالباً ما تشمل الغدة الزعترية أمام القلب—نادرة. ومع ذلك، عندما تظهر، يكون من الصعب التعرف عليها وقياسها بدقة على صور الأشعة المقطعية، وهي مهام تتطلب عادةً متخصصين في مراكز السرطان الكبرى. تبحث هذه الدراسة فيما إذا كان نظام ذكاء اصطناعي مدرّباً بعناية يمكن أن يساعد الأطباء في مستشفيات متعددة على اكتشاف هذه الأورام بدقة ورسم محيطها في صور الأشعة المقطعية الروتينية، مما قد يحسن التشخيص وتخطيط العلاج للمرضى الذين قد يُغفلون لولا ذلك.
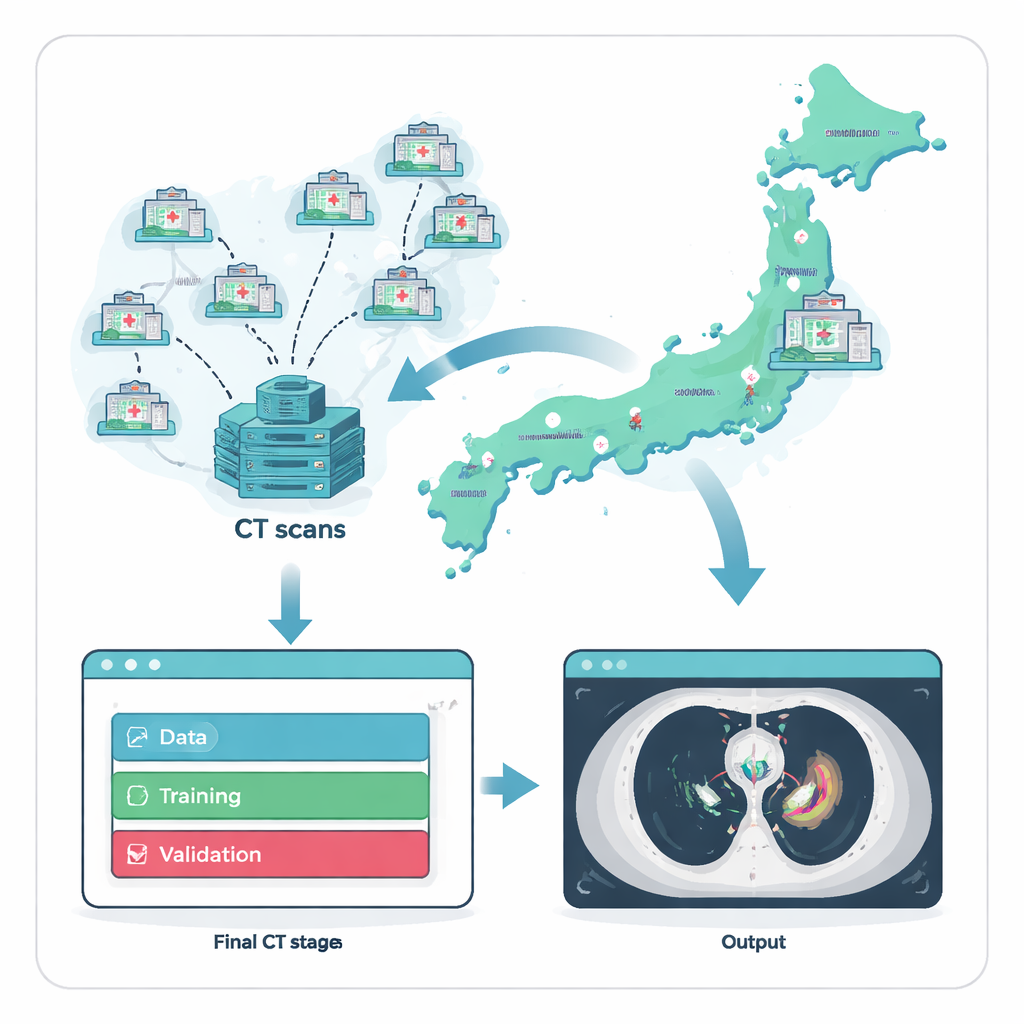
جمع حالات نادرة من أنحاء البلاد
بما أن أورام المنصف الأمامية غير شائعة، فإن العقبة الأولى كانت مجرد العثور على أمثلة كافية لتدريب نظام الذكاء الاصطناعي. تعامل الباحثون مع ذلك بالتعاون مع المستشفى الوطني لمكافحة السرطان في اليابان و135 مستشفى محالة على مستوى البلاد. على مدى عقدين، جمّعوا 711 صورة مقطعية للصدر، كل منها لمريض بالغ مختلف تم تأكيد تشخيص ورمه مجهرياً. ولضمان اختبار عادل وواقعي، قسّموا البيانات إلى ثلاث مجموعات: مجموعة كبيرة للتدريب، ومجموعة أصغر للتعديل الدقيق، ومجموعة اختبار خارجية منفصلة تماماً مكونة من 164 مسحاً مأخوذة من 121 مستشفى لم تساهم بأي صور تدريبية. هذا الفصل الصارم يحاكي أداء النظام عند إدخاله إلى مستشفيات جديدة لم يسبق له «رؤيتها» من قبل.
تحويل المسوحات إلى مادة تعليمية موثوقة
جودة نموذج الذكاء الاصطناعي تعتمد على جودة الأمثلة التي يتعلم منها، لذا استثمر الفريق كثيراً في وضع العلامات بتوقيع الخبراء. لكل صورة مقطعية، تتبّع المتخصصون حدود الأورام في الجزء الأمامي من الصدر بدقة. رسم جراح صدري أو فني أشعة الخطوط الأولية، ثم راقبتها اثنان من أخصائيي الأشعة التشخيصية ذوي الخبرة. وأُحلت أي خلافات للنقاش لحسمها، مما أفرز مرجعاً عال الجودة يعكس كيف يفسر الخبراء الصور في الممارسة. باستخدام منصة ذكاء اصطناعي تجارية بدون برمجة، بنى الأطباء نموذجاً ثلاثي الأبعاد ودربوه ليتبع هذه الرسومات الخبيرة، ما سمح للعاملين الطبيين بتوجيه عملية التطوير دون كتابة كود.
كيف يرى الذكاء الاصطناعي الأورام ثلاثية الأبعاد
جوهر النظام هو نسخة ثلاثية الأبعاد من بنية شبكة عصبية تعرف باسم U-Net، مصممة لتحليل مجلدات الأشعة المقطعية الكاملة بدلاً من الشرائح الفردية. تستقبل مكدساً من صور الصدر وتتنبأ، لكل عنصر حجمي صغير، ما إذا كان ينتمي إلى الورم أو إلى النسيج الطبيعي، فتقوم فعلياً برسم قناع ثلاثي الأبعاد فوق الورم. أثناء التدريب تعرّض النموذج لتناوبات عشوائية، وتغيير المقاييس، والقص، ليصبح أكثر متانة تجاه اختلافات وضع المريض وإعدادات الماسح. ثم قيَّم الباحثون مدى مطابقة مناطق الورم المتوقعة من النموذج لرسومات الخبراء، باستخدام مقاييس تداخل قياسية تكافئ كل من دقة وضع الحدود والتغطية الكاملة لحجم الورم.
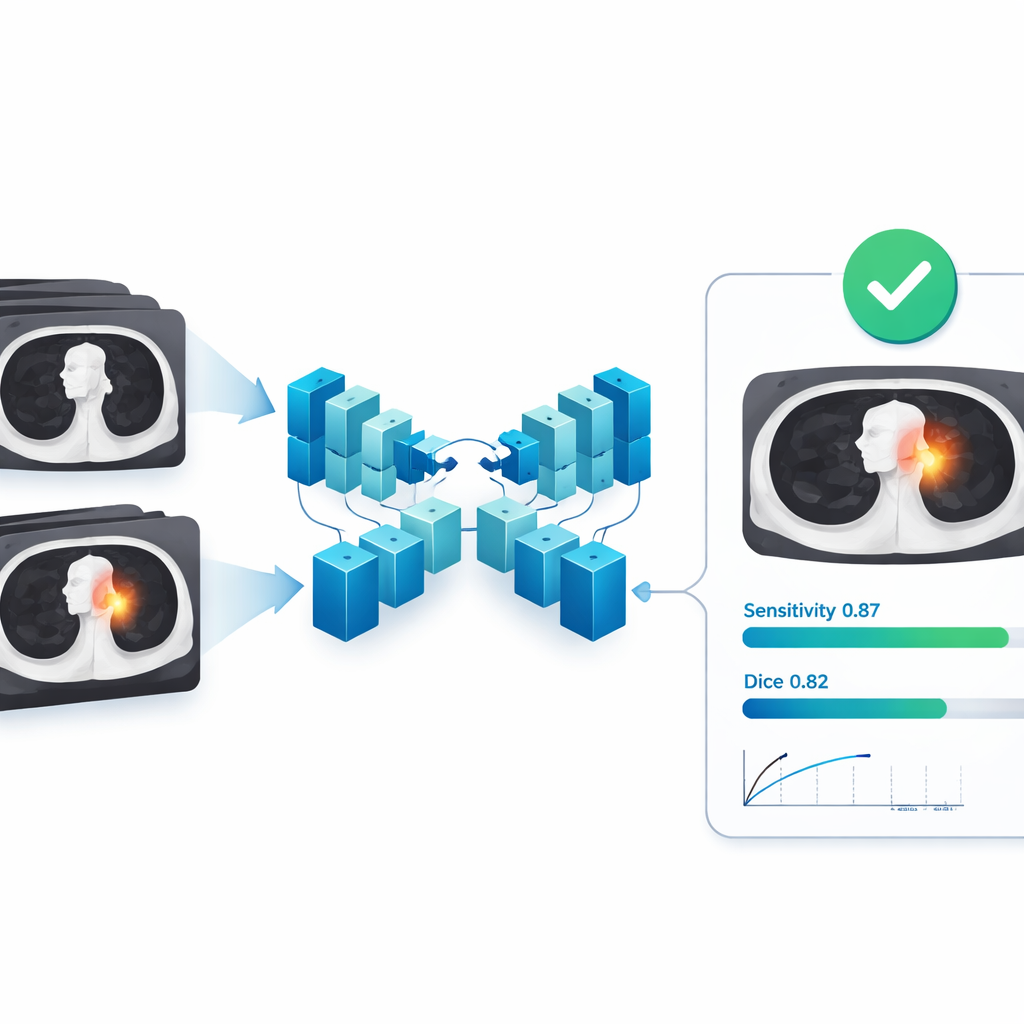
الأداء عبر مستشفيات وأنواع أورام متعددة
في مجموعة الاختبار الخارجية من 121 مستشفى مستقلة، أظهر نموذج الذكاء الاصطناعي اتفاقاً قوياً مع تقاسيم الخبراء. بمتوسط، كان مقياس التداخل (Dice) 0.82، مع مقياس مرتبط هو تقاطع على الاتحاد (IoU) عند 0.72؛ وكانت الدقة والاسترجاع حوالي 0.82–0.85، ما يعني أن النموذج نادراً ما صنّف نسيجاً طبيعياً خطأً كورم ونجح في التقاط معظم نسيج الورم. والأهم أن هذه النتائج ثبتت عبر مصنعي الماسحات المختلفين، وأحجام الأورام، وأنواع الأورام، ما يشير إلى أن النظام قادر على التعامل مع التنوع الموجود في العيادات الواقعية. وعند تقييمه ككاشف—بمعنى السؤال عما إذا كان يجد كل آفة على الإطلاق—بلغ النموذج حساسية تقارب 0.87 حتى بقاعدة مطابقة صارمة، مع أقل من إنذار كاذب واحد في المتوسط لكل مسح، وهو ملف أداء جذاب بشكل خاص لدعم فحوصات السرطان.
أين يساعد النظام وأين يبقى الدور البشري حاسماً
نظرة أقرب على النجاحات والإخفاقات كشفت نمطاً واضحاً: أداء الذكاء الاصطناعي كان أفضل على الأورام الأكبر وواجه صعوبة مع الآفات الصغيرة أو الخافتة جداً، حيث قد يفوتها جزئياً أو يخلط بينها وبين تراكيب طبيعية مجاورة مثل الأوعية الدموية أو تجمعات السوائل. وهذا يتماشى مع التجربة اليومية في الأشعة، حيث تكون النتائج الصغيرة أو منخفضة التباين الأسهل في التغافل عنها. يجادل المؤلفون بأن الأداة تُستخدم الأفضل في إعداد «الإنسان في الحلقة». يمكن أن تعمل كقارئ أول فعال يشير إلى الأورام المحتملة ويحدّد حدودها، موفّرة أحجاماً جاهزة لمهام مثل تخطيط العلاج والجراحة، بينما يركّز الأطباء على مراجعة المناطق الصغيرة أو الدقيقة أو الغامضة.
ما يعنيه هذا للمرضى والأدوات المستقبلية
بالنسبة للقارئ العام، الرسالة الأساسية هي أن نظام ذكاء اصطناعي مدرّب على مجموعة نادرة لكن خطيرة من أورام الصدر يمكن أن يساعد الأطباء بشكل موثوق في العثور على هذه السرطانات ورسم محيطها في صور الأشعة المقطعية، حتى في مستشفيات لم تساهم ببيانات في تدريبه. من خلال توفير خرائط ثلاثية الأبعاد دقيقة للأورام مع إبقاء الإنذارات الكاذبة منخفضة، قد يُسرّع النموذج التشخيص، ويدعم تخطيطاً شعاعياً وجرحياً أكثر دقة، ويشكّل شبكة أمان إضافية ضد الآفات المفقودة. في الوقت نفسه، تبرز الدراسة أن الذكاء الاصطناعي ليس بديلاً للحكم الخبير—خاصةً للأورام الأصغر والأكثر خفوتاً—بل مساعد واعد يصبح أقوى عندما يجتمع الأطباء وبيانات التصوير ومنصات الذكاء الاصطناعي سهلة الاستخدام.
الاستشهاد: Takemura, C., Miyake, M., Kobayashi, K. et al. A clinically applicable and generalizable deep learning model for anterior mediastinal tumors in CT images across multiple institutions. Sci Rep 16, 6774 (2026). https://doi.org/10.1038/s41598-026-37504-z
الكلمات المفتاحية: أورام المنصف الأمامية, التعلّم العميق في تصوير الأشعة المقطعية, تقسيم الصور الطبية, دعم تشخيص السرطان, الذكاء الاصطناعي في الأشعة