Clear Sky Science · ar
يعرض دواء التهاب الكبد الدهني المرتبط بخلل التمثيل الغذائي (MASH) ريسميتيْروم نشاطًا واسعًا على مستقبلات نووية مع تأثير وظيفي طفيف
لماذا يهم دواء كبدي جديد
يعيش ملايين الأشخاص حول العالم مع شكل خطير من مرض الكبد الدهني يُسمى الآن التهاب الكبد الدهني المرتبط بخلل التمثيل الغذائي، أو MASH. يمكن أن يتلف الكبد بصمت لسنوات ويؤدي في النهاية إلى تندب أو فشل كبدي أو سرطان. في عام 2024، أصبح دواء اسمه ريسميتيْروم أول علاج معتمد في الولايات المتحدة خصيصًا لـ MASH. تطرح هذه الدراسة سؤالًا حاسمًا للمرضى والأطباء: هل يعمل ريسميتيْروم بشكل دقيق على هدفه المقصود في الكبد، أم أنه يتداخل أيضًا مع مفاتيح جزيئية أخرى قد تقلل من فوائده أو تتسبب في آثار جانبية؟
طريقة مستهدفة لحرق دهن الكبد
صُمم ريسميتيْروم ليعمل كنسخة مركزة من هرمون الغدة الدرقية الطبيعي. تَتحكم هرمونات الغدة الدرقية في سرعة استخدام خلايانا للطاقة، مؤثرة على معدل ضربات القلب، ودرجة حرارة الجسم، وطريقة معالجة الدهون والسكريات. تعمل هذه الهرمونات عبر مستقبلين مرتبطين، يُسميان ألفا وبيتا. شكل بيتا هو الأكثر وفرة في الكبد، بينما يهيمن شكل ألفا في القلب والعظم. في الأشخاص المصابين بـ MASH، يكون إشارات هرمون الغدة الدرقية داخل الكبد غالبًا بطيئة حتى عندما تبدو تحاليل الدم طبيعية. يهدف ريسميتيْروم إلى «إيقاظ» مستقبل بيتا في خلايا الكبد لحرق المزيد من الدهن، وكسر الكوليسترول، وتقليل تراكم الدهون، مع تجنيب مستقبل ألفا لتفادي آثار جانبية على القلب والعظم. 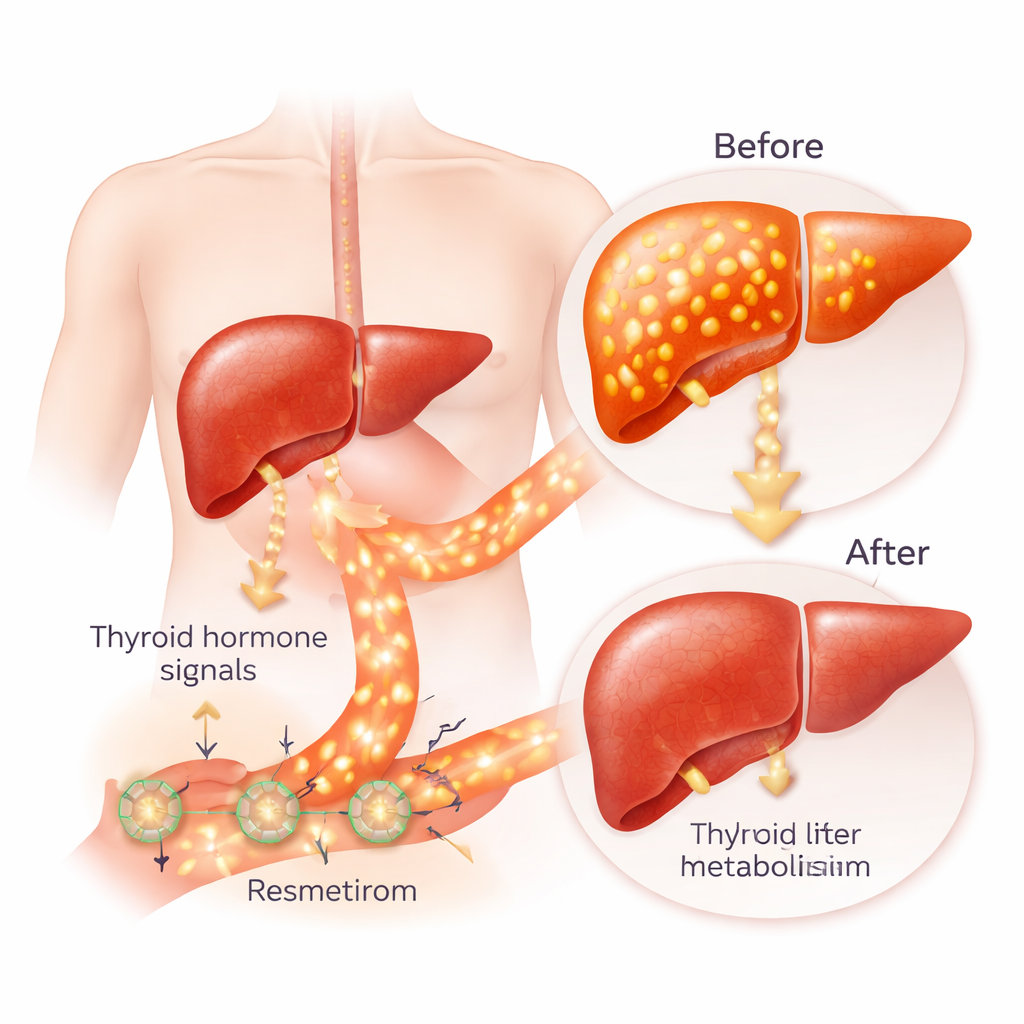
التحقق من الأهداف الجزيئية غير المرغوبة
نظرًا لأن ريسميتيْروم يجب أن يُعطى بجرعات مرتفعة نسبيًا ليقوم بعمله، تساءل الباحثون عما إذا كان قد يرتبط أيضًا بمستقبلات نووية أخرى—بروتينات في نواة الخلية تعمل كمفاتيح رئيسية للاستقلاب وإزالة السموم والإيقاعات اليومية للجسم. باستخدام النمذجة الحاسوبية وسلسلة من اختبارات المراسل الخلوية، تحققوا أولاً مما إذا كان ريسميتيْروم يتصرف مثل بعض نواتج تحلل هرمون الغدة الدرقية المعروفة بتنشيط مستقبل آخر يُسمى PPARγ. اقترحت النمذجة أنه، بالرغم من أشكالها المتشابهة، سيَوَقَع ريسميتيْروم بشكل ضعيف في جيب الارتباط الخاص بـ PPARγ، وأكدت اختبارات الخلايا أن ريسميتيْروم لم يشغّل هذا المستقبل.
ضربات خارج الهدف، لكن بتأثير مخفف
ثم فحص الباحثون ريسميتيْروم مقابل لوحة أوسع من المستقبلات النووية المشاركة في التحكم بالدهون والجلوكوز. كما كان متوقعًا، نشّط ريسميتيْروم مستقبل هرمون الغدة الدرقية بيتا بقوة أكبر من شكل ألفا. ومع ذلك، تفاعل أيضًا مع عدة مستقبلات أخرى: حجب مستقبلًا يُسمى CAR، وخفض النشاط الأساسي لثلاثة مستقبلات ROR، وقمع بشكل متواضع عاملًا محافظًا على الكبد يعرف بـ HNF4α. من الناحية النظرية، قد تكون هذه الأفعال خارج الهدف مقلقة، لأن كل هذه المفاتيح تساعد في تنظيم استقلاب الكبد وإزالة السموم. ومع ذلك، كانت قوة هذه التأثيرات معتدلة فقط، وغالبًا جزئية، مما يوحي أن ريسميتيْروم يدفع هذه المستقبلات بلطف بدلًا من قلبها بالكامل.
إدخال الدواء في خلايا كبدية أكثر واقعية
لرؤية ما إذا كانت هذه التفاعلات خارج الهدف مهمة في ظروف أقرب إلى الواقع الحيوي، تحول الفريق إلى خلايا سرطان الكبد البشرية الشائعة الاستخدام كبديل لأنسجة الكبد. قاسوا نشاط جينات رئيسية معروفة بالاستجابة لهرمون الغدة الدرقية وكذلك لمستقبلات CAR وRORs وHNF4α. عزز ريسميتيْروم الجينات المشاركة في إنتاج الجلوكوز وإزالة السموم بنمط يطابق عمل هرمون الغدة الدرقية، بالرغم من أن أفعاله خارج الهدف كان من المفترض أن تدفع بعض تلك الجينات في الاتجاه المعاكس. عندما حفّز العلماء إنتاج الدهون في هذه الخلايا، قلّل ريسميتيْروم والهرمون الدرقي الطبيعي بوضوح من تراكم الدهون، بينما كان للأدوية التي تستهدف ROR أو CAR أو HNF4α بمفردها تأثير ضئيل. 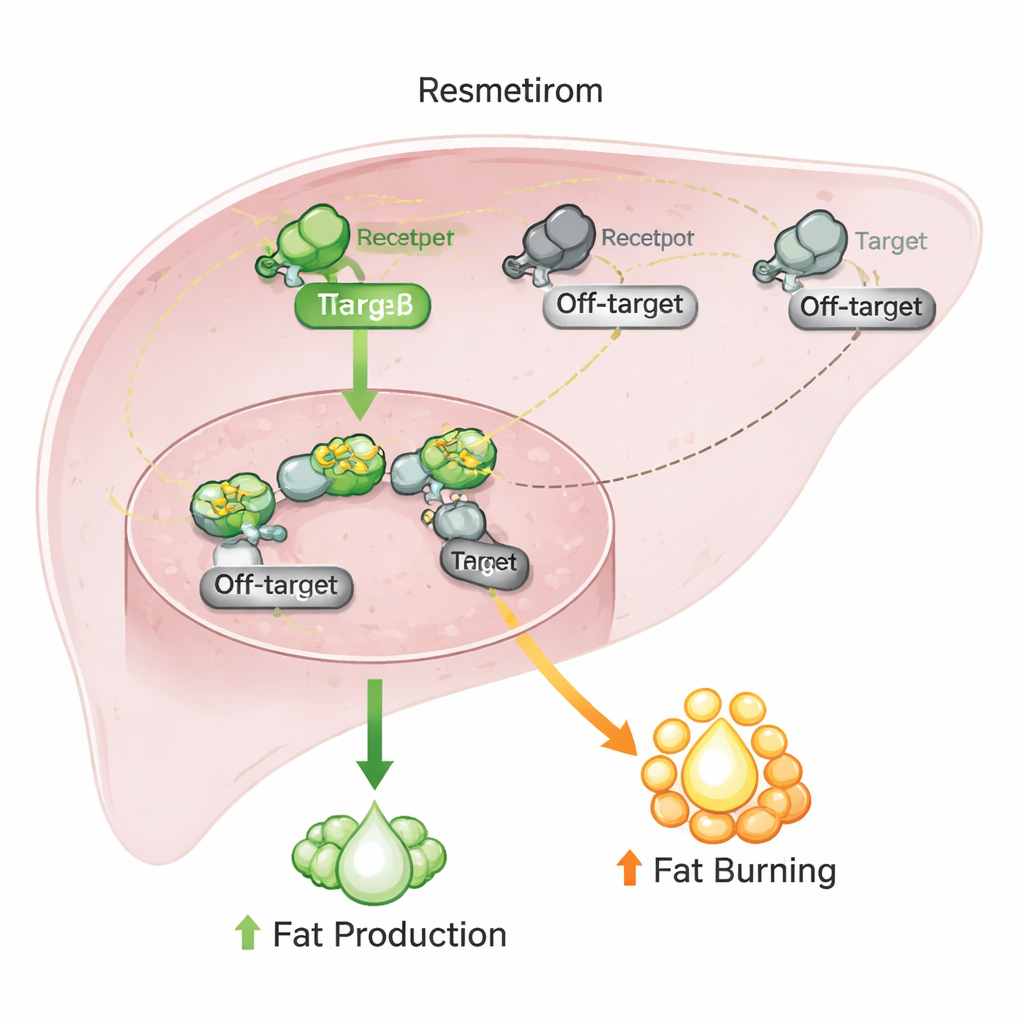
ماذا يعني هذا للمرضى والأدوية المستقبلية
تقترح النتائج مجتمعة أن ريسميتيْروم يتلامس بالفعل مع عدة مستقبلات نووية أخرى، لكن تأثيره الرئيسي في خلايا الكبد لا يزال مدفوعًا بمستقبل هرمون الغدة الدرقية بيتا المقصود. عمليًا، يعني ذلك أن قدرة الدواء على خفض دهن الكبد وتحسين صحته في MASH من غير المرجح أن تُقوّض بواسطة هذه الأنشطة الجانبية، على الأقل في الأنظمة التجريبية التي دُرست. وتُبرز الدراسة درسًا أوسع: لأن ريسميتيْروم معتدل الفعالية فقط، فإنه يحتاج تركيزات مرتفعة نسبيًا ليعمل، مما يزيد احتمال حدوث تأثيرات جانبية طفيفة خارج الهدف في أنحاء أخرى من الجسم. وهذا يجعل من الأهمّية بمكان تطوير أدوية مستقبلية مبنية على هرمون الغدة الدرقية تلتصق بمستقبل بيتا بقوة وبانتقائية أكبر، لتوفّر نفس فوائد الكبد أو أفضل بجرعات أقل وبمزيد من تقليل التداخلات الجزيئية غير المقصودة.
الاستشهاد: Kärcher, A., Isigkeit, L., Bandomir, N.C. et al. The metabolic dysfunction-associated steatohepatitis (MASH) drug resmetirom exhibits broad nuclear receptor activity with minimal functional impact. Sci Rep 16, 4083 (2026). https://doi.org/10.1038/s41598-026-37494-y
الكلمات المفتاحية: مرض الكبد الدهني, MASH, ريسميتيْروم, مستقبل هرمون الغدة الدرقية, استقلاب الكبد