Clear Sky Science · ar
حبس حساس الجهد استثنائي التحديد لقنوات NaV1.5 بواسطة ماغنيسيوم-بروتوبورفيرين يعيق هجرة الخلايا السرطانية
صبغة نباتية تشير إلى استراتيجية جديدة ضد السرطان
قد تشترك قلوبنا وأورامنا بضعف غير متوقع: نوع خاص من البوابات الكهربائية في غشاء الخلية يُدعى NaV1.5. تظهر هذه الدراسة أن نظيراً طبيعياً لبنى الكلوروفيل في النباتات، ماغنيسيوم‑بروتوبورفيرين IX (MgPpIX)، قادر على إغلاق هذه البوابة بدقة استثنائية. وبذلك يبطئ بشكل حاد حركة بعض الخلايا السرطانية — ما يوحي بأن جزيئاً مستوحى من كيمياء التمثيل الضوئي قد يساعد في كبح النقائل دون تعطيل كبير للدماغ أو العضلات.
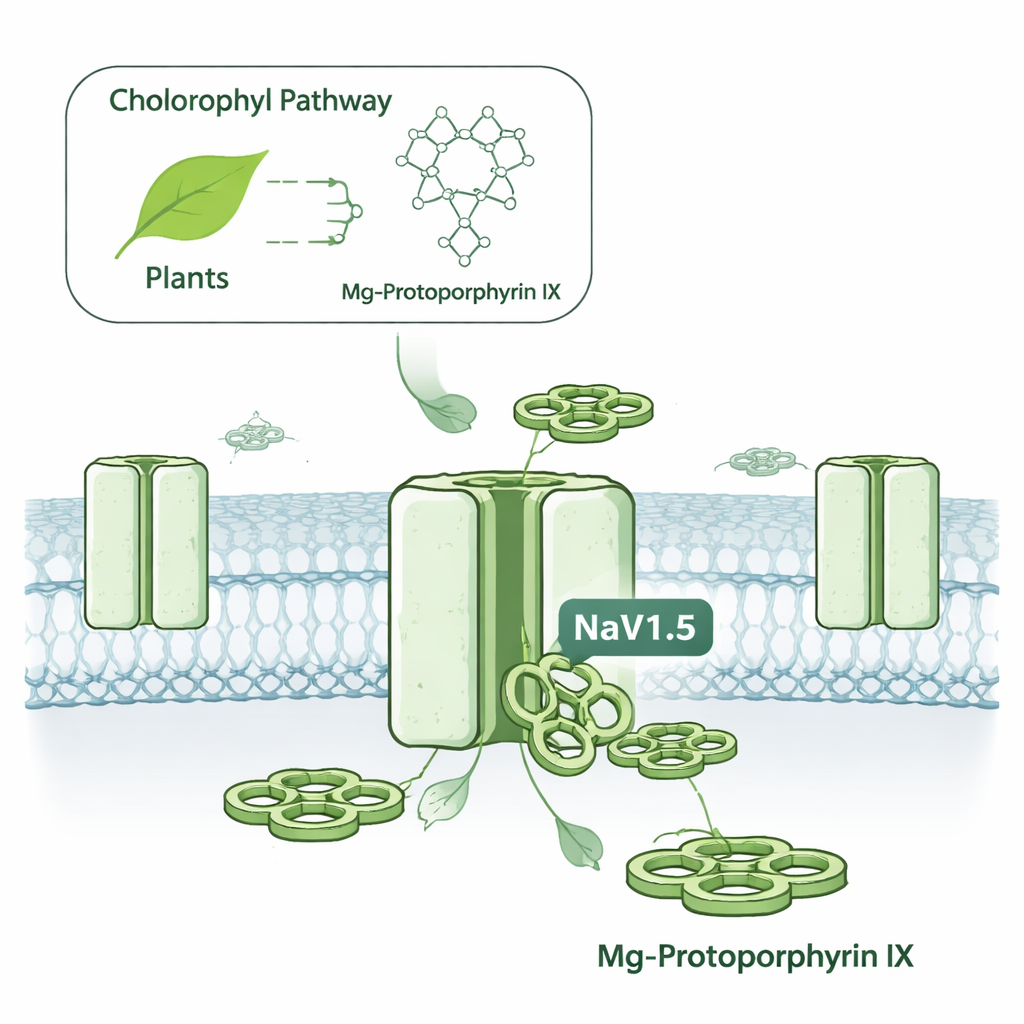
مفتاح كهربائي مخفي في الخلايا السرطانية
تستخدم الخلايا قنوات الصوديوم المعتمدة على الجهد كأبواب صغيرة تفتح وتغلق للسماح للأيونات المشحونة بالمرور، مولدة إشارات كهربائية. تُعرف NaV1.5 بدورها في ضربات القلب، حيث تساعد في تحفيز كل انقباضة. لكن نفس القناة توجد أيضاً في عدة سرطانات، بما في ذلك سرطانات الثدي والقولون، حيث تم ربط نشاطها بزيادة حركة الخلايا وغزوها. كان استهداف NaV1.5 صعباً لأن معظم أدوية قنوات الصوديوم تصيب أيضاً قنوات قريبة في الأعصاب والعضلات الهيكلية، مما يعرض لمخاطر آثار جانبية مثل النوبات أو الخدر أو ضعف العضلات. انطلق المؤلفون لاكتشاف ما إذا كانت هناك جزيئات صغيرة يمكنها تمييز NaV1.5 عن قريباتها بانتقائية أعلى بكثير.
مانع مستوحى من النبات بدقة قياسية
درس الفريق عائلة من الجزيئات الحلقية المسماة بروتوبورفيرينات معدنية، التي تشبه نوى الهيم في الدم والكلوروفيل في النباتات لكنها تحتوي على ذرات معدنية مركزية مختلفة. عندما طبقوا نسخاً مختلفة على قنوات NaV1.5 البشرية المعبّرة في خلايا مزروعة، برز مركب واحد: MgPpIX. خفض هذا المركب التيار الكهربائي عبر NaV1.5 بنحو 99% عند تراكيز نانومولارية، أي أقوى بحوالي 100 مرة من نظير قائم على الحديد (الهيمين). كانت النسخ المعدنية الأخرى، مثل تلك المحتوية على النيكل أو النحاس، عملياً غير فعالة. ومن اللافت أن MgPpIX لم يؤثر على عدة أنواع أخرى من قنوات الصوديوم البشرية (المستخدمة في الدماغ، والأعصاب المحيطية، والعضلات الهيكلية) بنفس الجرعات، مما يجعل انتقائيته من بين الأكثر حدة المُبلغ عنها لهذه العائلة القنوية.
كيف تعطل الجزيء ذراع الجهد الصغيرة
لفهم هذه الدقة الغريبة، جمع الباحثون بين التلاعب الجيني والمحاكاة الحاسوبية. تحتوي قنوات الصوديوم على أربعة أجزاء متكررة، كل منها يضم «حساس جهد» يتحرك عندما يتغير فرق الجهد عبر الغشاء. عن طريق تبديل أحماض أمينية فردية بين NaV1.5 وقنوات غير حساسة، حدد الفريق تأثير MgPpIX في حساس الجهد في الميدان الثاني، لا سيما بقايا اثنين مكشوفين إلى خارج الخلية. أشارت محاكاة الديناميكا الجزيئية في بيئة غشائية واقعية إلى أن MgPpIX يستقر بجانب هذا الحساس عندما يكون في وضع الراحة «المنخفض». يجذب المركز المعدني الموجب الشحنة في MgPpIX سلسلة جانبية سالبة الشحنة على القناة، في حين تتفاعل الحلقة المسطحة مع الليبيدات المحيطة. يبدو أن هذا الارتباط يثبت حساس الجهد في مكانه، مانعاً حركته إلى الحالة الفعّالة «المرتفعة» وبالتالي إبقاء القناة مغلقة. ومن المثير للاهتمام أن الاستقطابات القوية — مثل تلك أثناء نبضة القلب — يمكن أن تزيح الجزيء مؤقتاً، سلوك يصفه المؤلفون بأنه «اعتماد عكسي على الاستخدام».
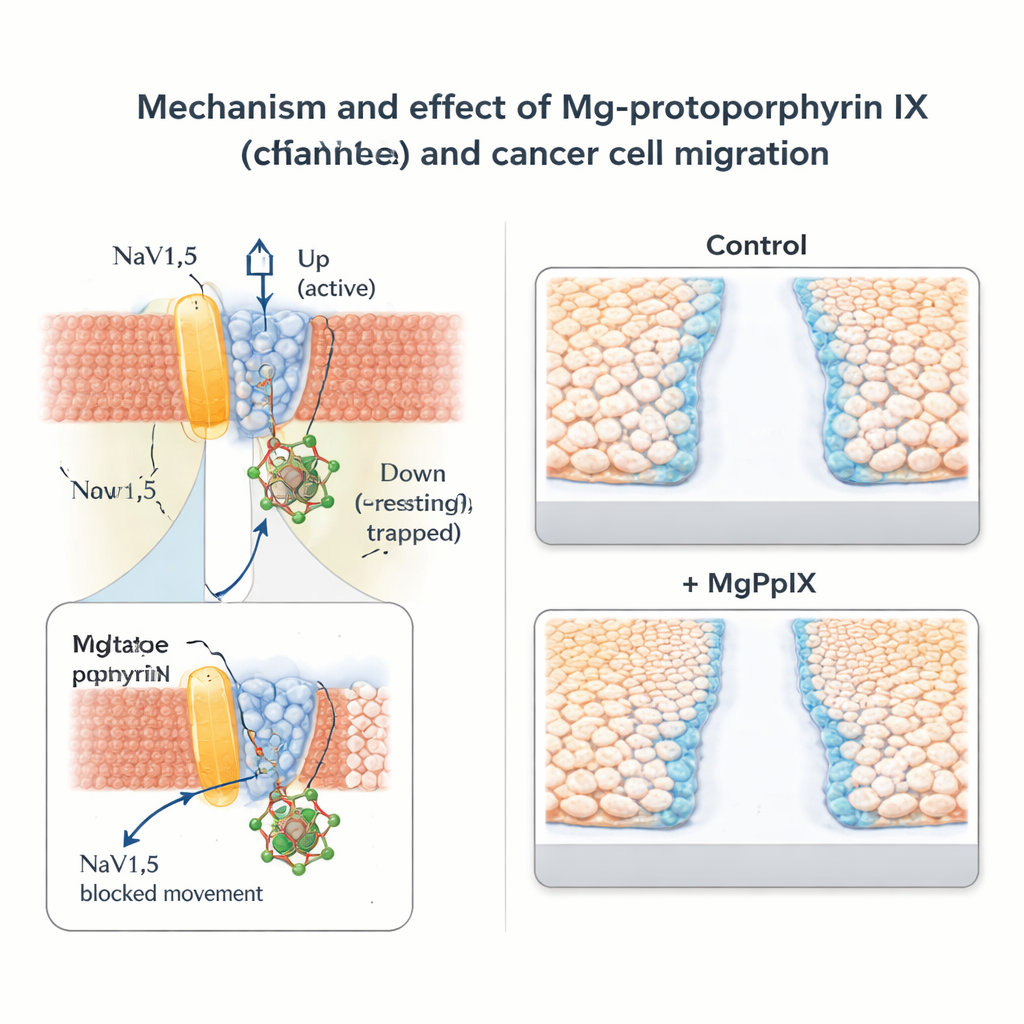
إبطاء حركة الخلايا السرطانية دون حجب عصبي واسع
استكشف الفريق بعد ذلك ما يعنيه هذا المكبح الجزيئي لسلوك السرطان. في خطوط خلايا سرطان الثدي (MDA-MB-231) وسرطان القولون (SW-480) التي تُعبّر بشكل طبيعي عن NaV1.5، قلّل MgPpIX التيارات الصودية بشكل درامي وأبطأ هجرة الخلايا في اختبارات «الخدش» وعبور الغشاء التقليدية. كلما كانت بروتوبورفيرين معدنية معينة أكثر فعالية في حجب NaV1.5، زاد تأثيرها في إعاقة حركة الخلايا، مما يعزز العلاقة بين نشاط القناة والحركية. على النقيض من ذلك، لم تُظهر خطوط خلايا سرطانية تفتقر إلى NaV1.5 أي استجابة لـ MgPpIX لا كهربائياً ولا في اختبارات الهجرة، مما يدعم فكرة أن التأثير انتقائي بدرجة كبيرة وليس ساماً بصفة عامة. وبالمقارنة مع السم الكلاسيكي لقنوات الصوديوم تيتروتوكسين، حقق MgPpIX قمعاً أقوى للهجرة عند تراكيز أقل بكثير.
وعد وتحفظات لأدوية مضادة للنقائل في المستقبل
لغير المتخصصين، الرسالة المركزية هي أن الباحثين وجدوا جزيئاً ذا صلة بالنبات يعمل كمشبك دقيق دقيق على بوابة كهربائية من نوع قلبي استغلتها بعض السرطانات. عن طريق حبسه لذراع الجهد في وضع الراحة، يمكن لـ MgPpIX أن يحد بشدة من حركة الخلايا السرطانية في المختبر مع الحفاظ على قنوات صوديوم أخرى حاسمة للإحساس والحركة. وبما أن النشاط الكهربائي السريع للقلب يمكن أن يخفف هذا الحظر جزئياً، فقد يكون هناك حتى نافذة أمان حيث تتأثر الخلايا الورمية أكثر من الخلايا القلبية. على الرغم من أن MgPpIX نفسه قد لا يكون جاهزاً كدواء، فإن موقعه وآلية ارتباطه الفريدة يقدمان نموذجاً قوياً لتصميم أدوية مستقبلية تهدف إلى إيقاف انتشار السرطان عن طريق استهداف NaV1.5 بانتقائية غير مسبوقة.
الاستشهاد: Jamili, M., Ahmed, M., Bernert, A. et al. Exceptionally selective voltage-sensor trapping of NaV1.5 channels by Mg-protoporphyrin impairs cancer cell migration. Sci Rep 16, 4085 (2026). https://doi.org/10.1038/s41598-026-37492-0
الكلمات المفتاحية: قنوات الصوديوم, Nav1.5, هجرة الخلايا السرطانية, جزيئات مشتقة من الكلوروفيل, أدوية قنوات الأيونات المستهدفة