Clear Sky Science · ar
المُحفزات المصغرة Ple384 (TH) وPle388 (PITX3) لاستهداف خلايا الدوبامين في الدماغ المتوسط لدى الفئران والقرود
لماذا تهم هذه الدراسة لصحة الدماغ
خلايا الدماغ المصنعة للدوبامين تساعدنا على الحركة والتعلم من المكافآت والحفاظ على الدافع. وهي أيضاً الخلايا التي تموت في مرض باركنسون. يرغب العلماء والأطباء في توصيل جينات مفيدة أو أدوات جزيئية بشكل موجه إلى هذه الخلايا الضعيفة، سواء في حيوانات المختبر أو، في المستقبل، لدى البشر. لكن توجيه العلاج الجيني بحيث ينشط فقط في الخلايا الصحيحة وليس في جميع أنحاء الدماغ كان عقبة كبيرة. تصف هذه الدراسة مفاتيح DNA صغيرة جديدة يمكنها تشغيل الجينات بشكل موثوق تقريباً فقط في خلايا الدوبامين بالدماغ المتوسط لدى الفئران والقرود، فاتحةً طريقاً لعلاجات أكثر دقة وربما أكثر أماناً.
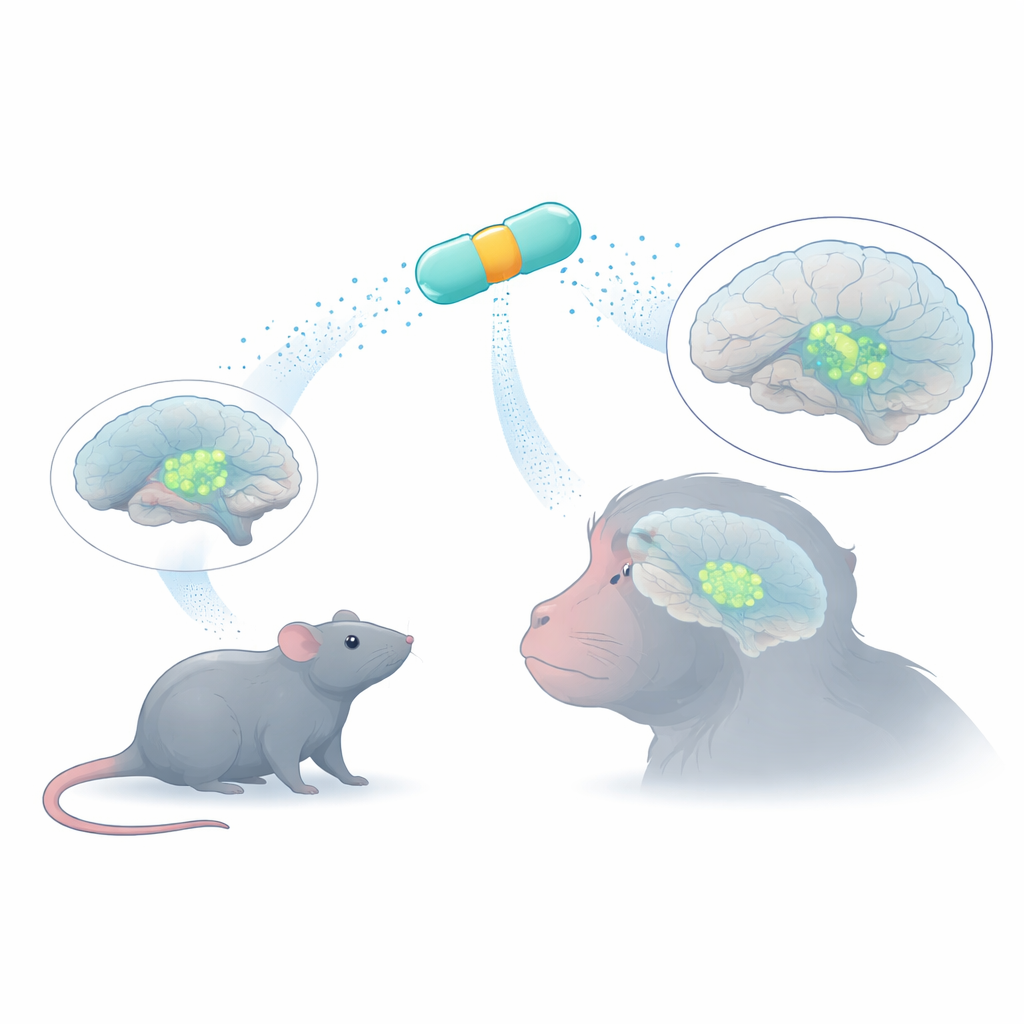
مفاتيح جينية صغيرة لوظيفة كبيرة
لإدخال جين علاجي إلى خلايا الدماغ، يستخدم الباحثون غالباً فيروسات معبِّرة عن نفسها من نوع adeno-associated viruses (AAV)، وهي ناقلات آمنة تحمل كمية محدودة من الحمض النووي. داخل كل فيروس، تعمل سلسلة مُحفز قصيرة كزر تشغيل/إيقاف، تحدد أين سيكون الجين نشطاً. العديد من المُحفزات الطبيعية تكون كبيرة جداً أو غير متخصصة، فتُشغِّل الجينات في أنواع خلايا كثيرة. استخدم الفريق أدوات المعلوماتية الحيوية لتصميم ثمانية «مُحفزات مصغرة» Compact MiniPromoters من الحمض النووي البشري—مجموعات قصيرة من عناصر التحكم مأخوذة من جينات معروفة بوضع علامة على الخلايا المصنعة للدوبامين. كان الهدف مجموعة من المفاتيح التي تتسع داخل ناقلات AAV ومع ذلك تحفز تعبيراً قوياً ومركزاً على نوع الخلية.
العثور على الأهداف الصحيحة في دماغ الفأر
اختبروا المُحفزات المصغرة الثمانية أولاً في الفئران. وضع كل مُحفز داخل ناقل AAV يحمل بروتيناً فلوريسنياً أخضراً، مما سمح للعلماء برؤية أين كان المفتاح نشطاً. أدخلوا الفيروسات إما عبر مجرى الدم أو مباشرة في الفراغات المملوءة بالسائل داخل الدماغ. فشلت معظم المُحفزات المصغرة في أن تكون انتقائية: أضاء بعضها العديد من الخلايا غير المنتجة للدوبامين، وبعضها بالكاد عمل على الإطلاق. برزا اثنان. الأول، المسمى Ple384، بُني من مناطق تحكم في جين التيروزين هيدروكسيلاز، الإنزيم الرئيسي المستخدم من قبل جميع الخلايا المنتجة للكاتيكولامين. الآخر، Ple388، أتى من PITX3، جين حاسم لشق من خلايا الدوبامين في الدماغ المتوسط. أنتجا كلٌ من Ple384 وPle388 إشارات قوية ومحدودة بشدة في المنطقة السوداء المركبة (substantia nigra compacta) ومنطقة السقيف البطني (ventral tegmental area)—مراكز خلايا الدوبامين في الدماغ المتوسط—مع أكثر من 90% من الخلايا المعلّمة تحمل أيضاً جزيء علامة الدوبامين.
من الفئران إلى القرود دون حفر عميق في الدماغ
أي علاج جيني موجه للأمراض البشرية يجب أن ينجح في نهاية المطاف في الرئيسيات، التي أدمغتها أكبر وأكثر تعقيداً. الحقن المباشر في المنطقة السوداء إجراء تقنياً صعباً وقد يتلف هذه البنية الصغيرة والعميقة. بدلاً من ذلك، اختبر الباحثون ما إذا كان بالإمكان توصيل نفس المُحفزات المصغرة إلى السائل الدماغي الشوكي في قرود الريسوس عبر حقنة واحدة في البطين الجانبي. باستخدام غلاف AAV متغير معروف بقدرته على الانتشار من الفراغات السائلة، وجدوا أن كل من Ple384 وPle388 حفّزا تعبيراً قوياً في خلايا الدوبامين في المنطقة السوداء ومنطقة السقيف البطني لدى الريسوس، بينما تجنبت إلى حد كبير مناطق غنية بالدوبامين الأخرى مثل الوطاء والعقدة الزرقاء (locus coeruleus). كانت غالبية الخلايا المعلّمة في المنطقة المستهدفة خلايا دوبامينية، مؤكدة أن المفاتيح حافظت على انتقائيتها عبر الأنواع.
أداتان بقوتين مختلفتين
مع أن كلا المُحفزين المصغرين وصلا إلى أهدافهما، إلا أنهما فعلا ذلك بأنماط مختلفة. أضاء Ple384، المستند إلى جين التيروزين هيدروكسيلاز ذو الانتشار الأوسع، عدداً أكبر من الخلايا بشكل عام وغطى كل من الطبقات البطنية والظهرية للمنطقة السوداء بالإضافة إلى جزء أكبر من منطقة السقيف البطني. أما Ple388، المعكس لتعبير PITX3 الأكثر تقييداً، فوسّم أساساً مجموعة فرعية من خلايا الطبقة البطنية ونتج عنه فلورسنس أضعف. رصد التعبير خارج الهدف كان في المقام الأول بالقرب من مواقع الحقن وفي بعض الأعضاء المحيطية بعد توصيل عبر مجرى الدم، لكن الضوابط الدقيقة أظهرت أن الناقلات الفيروسية كانت قادرة على الوصول إلى مناطق دماغية كثيرة؛ وكان المُحفزان المصغران نفسهما هما من قيدا التعبير ليقتصر في الغالب على خلايا الدوبامين في الدماغ المتوسط. هذه القوة القابلة للضبط—أحدهما أقوى وأوسع، والآخر أكثر انتقائية ومعتدل—تعني أن الباحثين يمكنهم اختيار المفتاح الأنسب لاحتياجاتهم، من تعديل لطيف إلى تدخل واسع النطاق.
ما يعنيه هذا للعلاجات المستقبلية
لغير المتخصص، الرسالة الأساسية هي أن المؤلفين ابتكروا مفتاحين جينيين مصغرين يعملان كمفاتيح ضوئية دقيقة وقابلة للبرمجة لخلايا الدوبامين في الفئران والقرود. يقدم Ple384 وصولاً قوياً وواسع النطاق إلى هذه الخلايا، بينما يركّز Ple388 على مجموعة أضيق وأكثر عرضة للخطر. وبما أن هذه المفاتيح صغيرة بما يكفي لتتناسب بسهولة داخل الناقلات الفيروسية المستخدمة شائعاً، فهي تترك مساحة للجينات العلاجية وقد تساعد في تقليل الآثار الجانبية بتجنّب المناطق الدماغية غير المرغوبة. مع تقدم العلاج الجيني لمرض باركنسون والحالات المرتبطة به، ستكون عناصر التحكم المستهدفة هذه مكونات أساسية لعلاجات قوية ودقيقة في آن واحد.
الاستشهاد: Galvan, A., Choi, D., Korecki, A.J. et al. MiniPromoters Ple384 (TH) and Ple388 (PITX3) for targeting midbrain dopaminergic neurons in mice and monkeys. Sci Rep 16, 9277 (2026). https://doi.org/10.1038/s41598-026-37466-2
الكلمات المفتاحية: خلايا الدوبامين, العلاج الجيني, مرض باركنسون, نواقل AAV, المُحفزات الخاصة بالخلايا