Clear Sky Science · ar
التأثيرات العلاجية لـ IGF-2 على الطيف السريري للاعتلال العصبي البصري النخاعي من خلال تثبيط موت الخلايا النجمية عبر تعديل مسار الإشارة IGF-1R/PI3K/AKT
حماية الدماغ في مرض مناعي ذاتي قليل المعرفة
طيف اضطراب التهاب العصب البصري والنخاع المناعي، المعروف بـ NMOSD، هو مرض مناعي ذاتي نادر لكنه مدمر يهاجم الأعصاب البصرية والحبل الشوكي، مما يترك المرضى غالبًا أعمى أو مشلولين أو يعانون من مشاكل إدراكية خطيرة. الأدوية الحالية تركز أساسًا على تهدئة الجهاز المناعي، وتكون مكلفة، ولا تحمي خلايا الدماغ مباشرة من الضرر. تستكشف هذه الدراسة ما إذا كانت جزيء طبيعي مرتبط بالنمو في الدم يُدعى IGF‑2 قد يساعد في حماية خلايا الدماغ من الإصابة في NMOSD ويوفر نهجًا جديدًا لعلاج المرض.
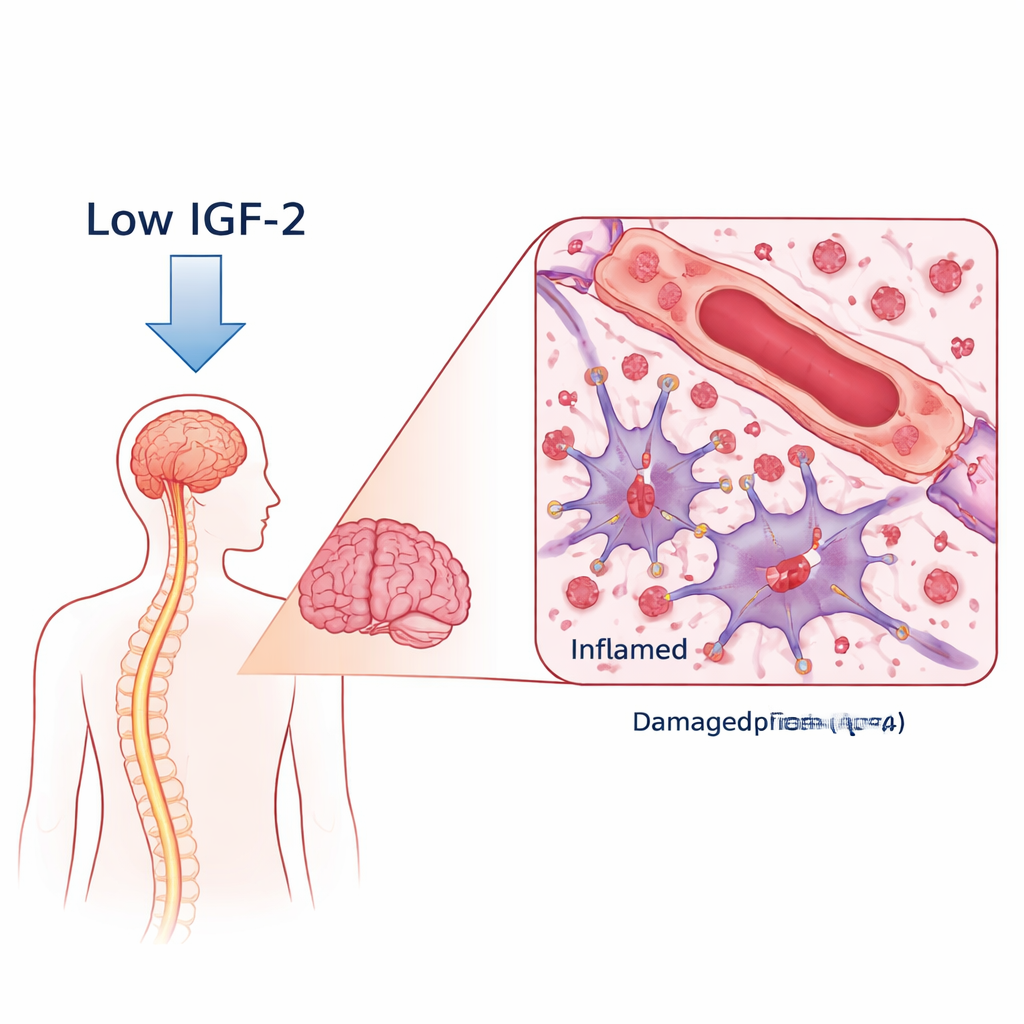
جسم مضاد ضار وحامي مفقود
في NMOSD، يصنع الجسم أجسامًا مضادة تستهدف بروتين قناتي للماء يسمى AQP4، الموجود على خلايا داعمة على شكل نجمي في الدماغ تُعرف بالخلايا النجمية. عندما ترتبط هذه الأجسام المضادة، فإنها تطلق هجمات مناعية تُلحق الضرر بالخلايا النجمية، وتزيل الميالين (الغطاء العازل حول الأعصاب)، وقد تضر الخلايا العصبية. قارن الباحثون دمًا من نساء مصابات بـ NMOSD موجبة لأجسام AQP4 مع متطوعات أصحاء. باستخدام مسح واسع للبروتينات، وجدوا أن مستويات IGF‑2 كانت أقل بكثير لدى مرضى NMOSD، بينما كانت اثنان من بروتينات ربط IGF التي يمكنها احتجاز IGF‑2 أعلى. والأهم من ذلك، أن المرضى ذوي أقل مستويات IGF‑2 كانوا يميلون إلى أن يكون لديهم إعاقات أسوأ ودرجات أضعف في اختبارات التفكير والذاكرة، مما يربط هذا الجزيء بشدة المرض والصحة الإدراكية.
العلاج القياسي يساعد على استعادة IGF-2
يتلقى العديد من مرضى NMOSD الريتوكسيماب، دواء يزيل خلايا B المنتجة للأجسام المضادة. قاس الفريق البروتينات في الدم قبل وبعد علاج الريتوكسيماب. بعد العلاج، ارتفعت مستويات IGF‑2 وانخفضت بروتينات الربط، لتقترب من النمط المرصود لدى الأشخاص الأصحاء. وهذا يوحي بأن تهدئة الجهاز المناعي قد تتيح للجسم استعادة بعض عوامله الحامية. وعلى الرغم من أن الريتوكسيماب ليس مُصممًا للعمل على IGF‑2 مباشرة، فإن التغير في هذا الجزيء يشير إلى أنه قد يكون جزءًا من استجابة التعافي في الجسم، وأن رصد IGF‑2 قد يساعد في تتبع وضع المرضى مع مرور الوقت.
اختبار IGF-2 في نموذج فأري للمرض
لرؤية ما إذا كان IGF‑2 يمكن أن يفعل أكثر من كونه علامة لشدة المرض، لجأ العلماء إلى نموذج فأري. حقنوا أجسامًا مضادة بشرية لـ AQP4 ومتمم بشري في أدمغة الفئران، ما أعاد خصائص رئيسية لـ NMOSD: فقدان AQP4 على الخلايا النجمية، والالتهاب، وتلف الميالين، وضعف الأطراف. مجموعة أخرى من الفئران تلقت أولًا فيروسًا غير ضار جعل خلايا أدمغتها تنتج IGF‑2 بكمية زائدة. فقدت هذه الفئران المعززة بـ IGF‑2 وزنًا أقل، وواجهت مشكلات حركية أخف، وأظهرت فقدانًا أقل للميالين والتهابًا أقل في أنسجة الدماغ والحبل الشوكي. ساعد العلاج القياسي بالريتوكسيماب أيضًا، لكن الإفراط في التعبير عن IGF‑2 بدا أنه يحمي نسيج الدماغ بشكل أكثر مباشرة، مما يشير إلى دور وقائي عصبي بدلاً من كونه مجرد مثبط للمناعة.
كيف يهدئ IGF-2 موت الخلايا والالتهاب
ثم فحص الفريق الخلايا النجمية في أطباق مخبرية تعرضت لأجسام NMOSD المضادة. عادةً، خفضت هذه الأجسام المضادة مستويات مستقبل رئيسي يُدعى IGF‑1R وكبّلت مسار أمان سفلي معروف باسم PI3K/AKT، بينما شغّلت بروتينات «تدمير ذاتي» وإشارات التهابية. عندما أجبر الباحثون الخلايا النجمية على إنتاج المزيد من IGF‑2، عاد نشاط هذا المسار الوقائي، وانخفضت مؤشرات موت الخلايا، وقل إطلاق الخلايا لمولات التهابية مثل IL‑1β وIL‑6 وTNF‑α. وإغلاق مستقبل IGF‑1R محا جزئيًا هذه الفوائد، مما يظهر أن IGF‑2 يعمل أساسًا بتفعيل سلسلة IGF‑1R/PI3K/AKT داخل الخلايا النجمية. وفي الفئران الحية، قلل تعزيز IGF‑2 أيضًا من تنشيط الخلايا البلعمية الصغيرة (الميكروغليا)، وخفض إشارات التهابية في مجرى الدم.
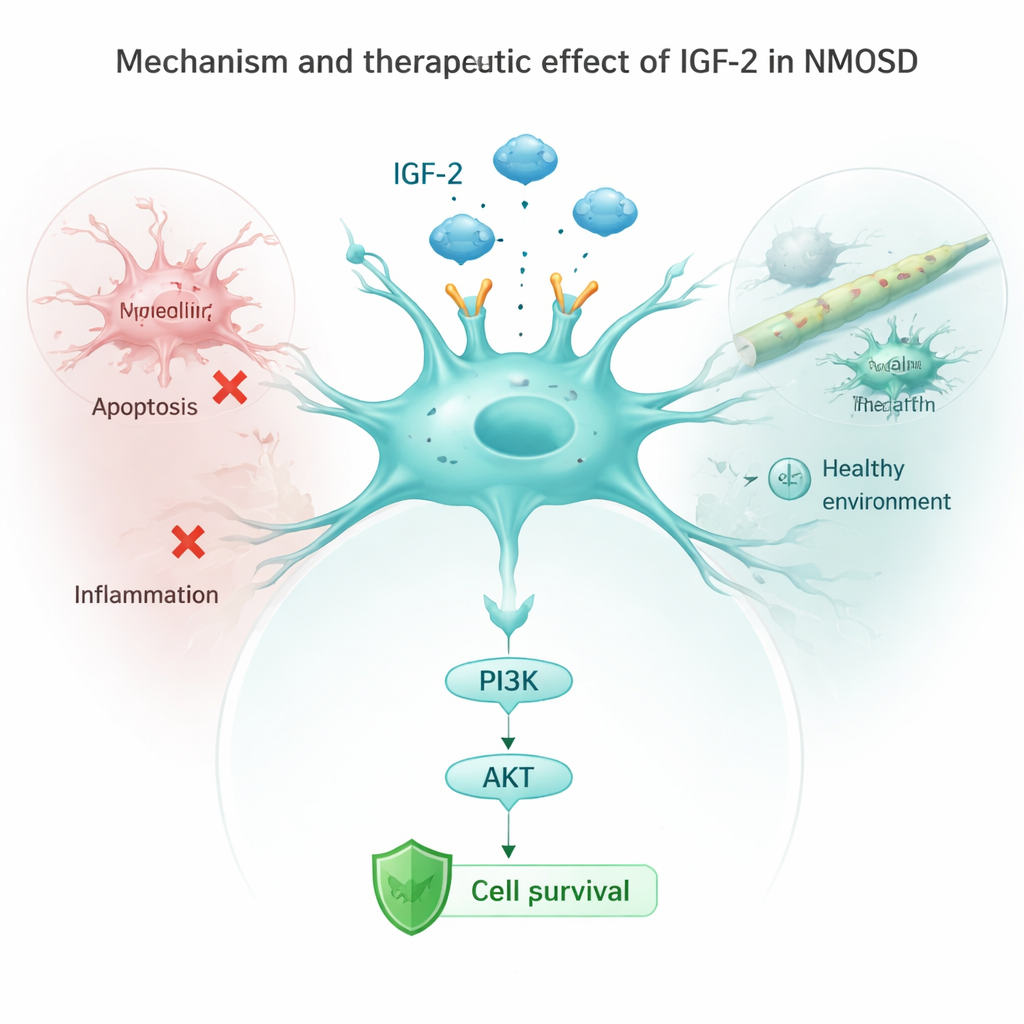
ماذا قد يعني هذا للمرضى
تجتمع هذه النتائج لتقترح أن انخفاض IGF‑2 هو علامة تحذيرية وفرصة ضائعة في NMOSD. المرضى الذين لديهم IGF‑2 أقل يميلون إلى أن يكونوا أكثر إعاقة ولديهم وظائف إدراكية أضعف، بينما استعادة أو تعزيز IGF‑2 في النماذج التجريبية يساعد الخلايا النجمية على النجاة، ويقلل من التهاب الدماغ، ويخفف تلف الأعصاب. ورغم أن هذا العمل مبكر وهو قائم على أعداد صغيرة من المرضى ودراسات حيوانية، إلا أنه يشير إلى IGF‑2 كهدف واعد لعلاجات مستقبلية قد لا تقتصر على تهدئة الهجوم المناعي فحسب، بل تحمي أيضًا خلايا الدماغ الضعيفة بشكل مباشر.
الاستشهاد: Zhang, Y., Xu, N., Yu, K. et al. Therapeutic effects of IGF-2 on NMOSD by inhibiting astrocyte apoptosis through modulation of the IGF-1R/PI3K/AKT signaling pathway. Sci Rep 16, 6312 (2026). https://doi.org/10.1038/s41598-026-37456-4
الكلمات المفتاحية: التهاب العصب البصري والنخاع المناعي, الخلايا النجمية, IGF-2, الالتهاب العصبي, الحماية العصبية