Clear Sky Science · ar
طفرة GJB2 c.109G > A التي تُفعّل مسار الاستماتة الميتوكوندرية بوساطة IFI27 المؤدية إلى فقدان السمع الوراثي غير المتلازم
لماذا تهم خلايا الأذن الصغيرة مستقبل الأطفال
يف影 فقدان السمع الموجود عند الولادة ملايين الأطفال حول العالم، وغالبًا ما يشكل طريقة تعلمهم الكلام والنجاح في المدرسة وقدرتهم على التواصل مع الآخرين. أحد الأسباب الوراثية الشائعة هو جين يُسمى GJB2، لكن الأطباء لم يفهموا تمامًا كيف تؤدي التغيرات في هذا الجين إلى تلف الأذن الداخلية. تستخدم هذه الدراسة سمك الزِرْد وخلايا بشرية لتتبّع سلسلة الأحداث من تغيير واحد في الحمض النووي لـGJB2 إلى موت خلايا الحسّاس الصوتية الرقيقة، وتشير إلى جزيء جديد، IFI27، كهدف محتمل للعلاجات المستقبلية.
تغير جيني شائع خلف الصمت الطفولي
بدأ الباحثون بفحص عينات دم من 1,199 طفلاً مشتبهاً بإصابتهم بفقدان سمع وراثي في محافظة فوجيان بالصين. ركزوا على عدة جينات معروفة للصمم ووجدوا أن التغيرات في GJB2 هي السائدة، حيث شكّلت 85% من كل الطفرات المكتشفة. من بين هذه الطفرات، كان التغير المحدد المسمى c.109G>A (المعروف أيضًا باسم p.Val37Ile) هو الأكثر تكرارًا. هذا المتغير شائع نسبيًا في عامة السكان ومع ذلك يوجد متكاثرًا بقوة لدى الأشخاص المصابين بمشاكل السمع، مما يشير إلى دوره الكبير في فقدان السمع غير المتلازم—أي فقدان السمع الذي يحدث دون مشاكل طبية مصاحبة.
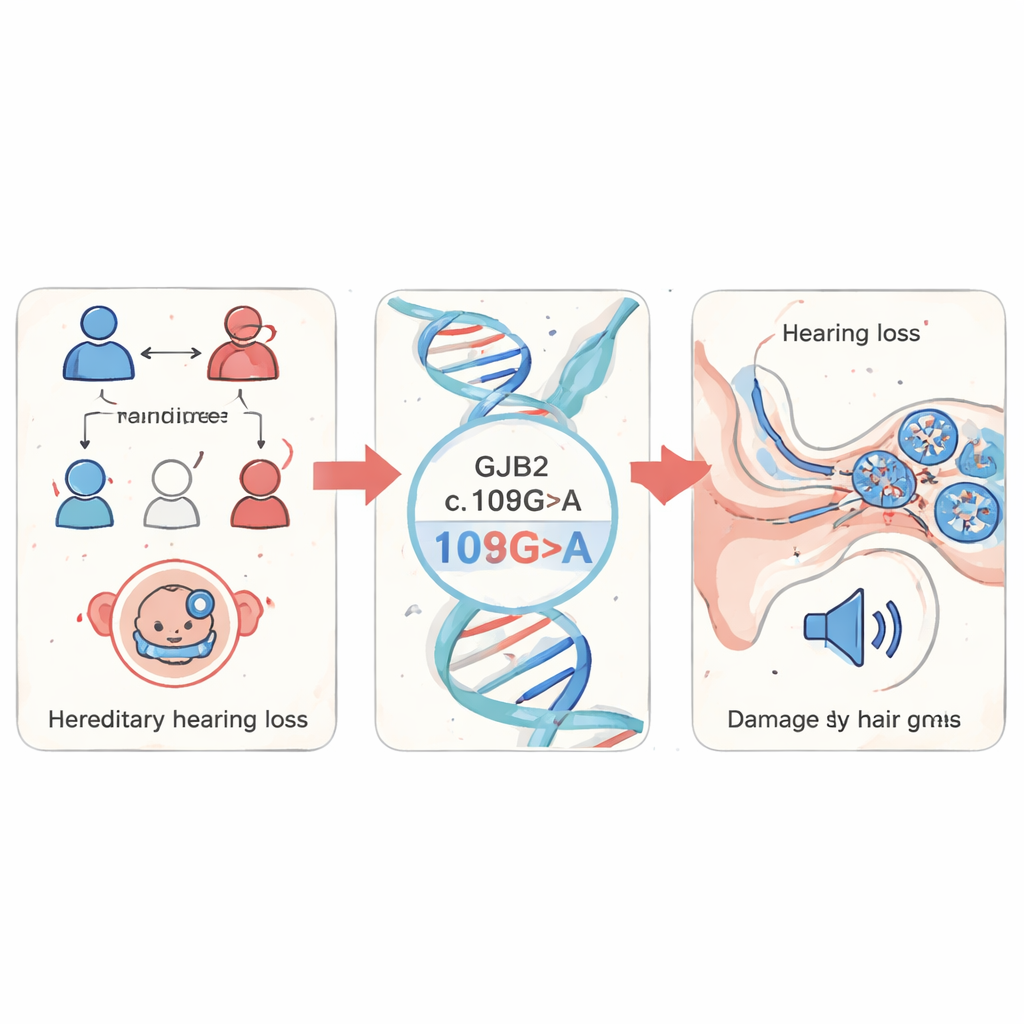
تتبّع التلف في سمكة شفافة
لمعرفة ما تفعله هذه الطفرة في كائن حي، لجأ الفريق إلى سمك الزِرْد، وهو سمك مياه عذبة أجنةه شفافة ويشارك العديد من الجينات وبُنى الأذن مع البشر. مهندَس الباحثون أجنة سمك الزِرْد لإنتاج إما GJB2 البشرية الطبيعي أو نسخة الطفرة c.109G>A، واستخدموا أيضًا نهج «خفض التعبير» لتقليل جين gjb2 الخاص بالسمكة. أظهرت الأجنة التي تحمل الجين الطافر أو المخفض تباطؤًا في النمو، وذيولًا منحنية، وتورمًا حول القلب، وهي علامات على تعطل التطور. والأهم من ذلك أن آذانها الداخلية كانت شاذة بوضوح: هياكل رئيسية تسمى الحصيات (otoliths) كانت أصغر وأكثر تباعدًا، ومنطقة القوقعة المملوءة بالسائل كانت مصغّرة. عندما أعاد العلماء إضافة GJB2 الطبيعي إلى جانب الطفرة، تحسنت العديد من هذه المشكلات البنيوية، مما يدل على أن الطفرة نفسها كانت سبب العيوب.
من آذان معطوبة إلى سلوك سمعي أضعف
بما أن السمع يعتمد على خلايا «الشعيرات» الصغيرة التي تحول اهتزازات الصوت إلى إشارات عصبية، صبغ الفريق هذه الخلايا في سمك الزِرْد. كان لدى الأسماك الحاملة لطفرات GJB2 أو خفض التعبير عدد أقل بكثير من خلايا الشعيرات في كل من الأذن الداخلية وعلى سطح الجسم، حيث تشعر أسماك الزرد أيضًا بحركة الماء. ثم اختبر الباحثون مدى استجابة الأسماك للصوت. باستخدام نظام تتبّع آلي، قاسوا المسافة والسرعة التي سبح بها اليرقات في اليوم الخامس عند تعرضها لانفجارات قصيرة من الصوت. استجابت الأسماك الطبيعية وتلك الحاملة لـGJB2 البري بالسباحة أكثر وبسرعة أكبر، بينما الأسماك الحاملة للطفرة والمخفضة بالكاد غيرت سلوكها، مما يدل على ضعف السمع. ومرة أخرى، أدت إضافة GJB2 الطبيعي جزئيًا إلى استعادة أعداد خلايا الشعيرات والحركة المحفزة بالصوت.
مسار قاتل داخل مصانع طاقة الخلية
لفهم ما يحدث داخل الخلايا، استخدم العلماء تسلسل الرنا للمقارنة بين نشاط الجينات في سمك الزِرْد الطبيعي وتلك التي لديها انخفاض في gjb2. تم تفعيل مجموعة من الجينات المرتبطة بـ«مسار الاستماتة الميتوكوندرية»—مسار الانتحار الخلوي المتمركز في مصانع طاقة الخلية—بشكل قوي. برزت بشكل خاص عدة أعضاء من عائلة IFI27، إلى جانب لاعبين معروفين في موت الخلية مثل Bax وcytochrome c وApaf1 والكاسبيزات. أكدت تجارب لاحقة في خلايا HEK293 البشرية النمط نفسه: الخلايا الحاملة لـGJB2 الطافر أنتجت المزيد من الجذور الحرة التفاعلية (ROS، شكل من أشكال الإجهاد التأكسدي)، وأطلقت المزيد من السيتوكروم c من الميتوكوندريا، وقامت بتشغيل بروتينات الاستماتة، مما أدى إلى زيادة موت الخلايا. عندما كتم الباحثون IFI27 في الخلايا الحاملة للجين الطافر، انخفضت مستويات ROS، وخفت إشارات الموت، وقَلَّت نسبة الخلايا التي دخلت في الاستماتة.
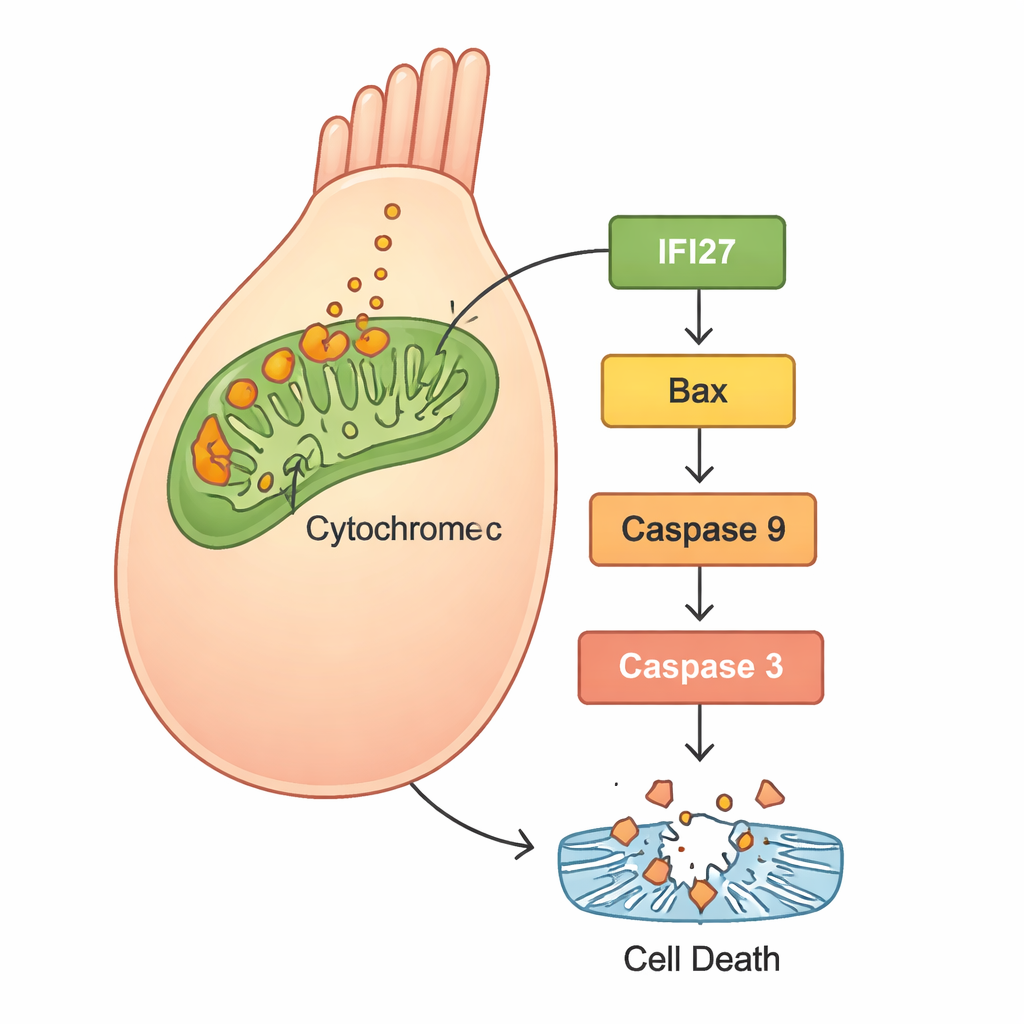
ماذا يعني هذا للعلاجات المستقبلية
تُشير النتائج مجتمعة إلى قصة واضحة: طفرة GJB2 c.109G>A تعطل التطور والوظيفة الطبيعية للأذن الداخلية، ليس فقط بتغيير التواصل الخلوي، بل أيضًا بتحفيز الإجهاد داخل الميتوكوندريا. هذا الإجهاد يرفع مستوى IFI27 والجينات المرتبطة به، ويطلق السيتوكروم c، ويفعّل سلسلة من البروتينات التي تدفع خلايا الشعيرات نحو الموت المبرمج. ونظرًا لأن خلايا الشعيرات لا تنمو بسهولة مرة أخرى في الإنسان، فإن فقدانها يؤدي إلى عجز سمعي دائم. من خلال إظهار أن خفض IFI27 يمكن أن يخفف هذه الشلالة المدمرة في الخلايا البشرية، تبرز الدراسة IFI27 كهدف واعد للأدوية أو العلاجات الجينية. ومع أن مثل هذه العلاجات ما تزال بعيدة في المستقبل—ومن المحتمل أن تحتاج إلى إعطاء مبكرًا جدًا في الحياة—فإن هذا العمل يقدم خارطة جزيئية واضحة لتحويل طفرة جينية كانت غامضة إلى سبب محتمل للوقاية من صمم الطفولة.
الاستشهاد: Chen, Y., Zhao, P., Lin, Q. et al. GJB2 c.109G > A mutation activating IFI27-mediated mitochondrial apoptosis pathway leading to hereditary non-syndromic hearing loss. Sci Rep 16, 6240 (2026). https://doi.org/10.1038/s41598-026-37393-2
الكلمات المفتاحية: فقدان السمع الوراثي, طفرة GJB2, نموذج سمك الزرد, الاستماتة الميتوكوندرية, IFI27