Clear Sky Science · ar
استماتة فعّالة عبر انكسارات مزدوجة لسلسلة الحمض النووي في الخلايا الظهارية البشرية يحفزها تأثير غير حراري لموجات تيراهرتز عريضة النطاق ذات حقل عالٍ
ضوء جديد على قتل الخلايا السرطانية
غالباً ما تمثل علاجات السرطان توازناً دقيقاً: عليها تدمير الخلايا السرطانية دون الإضرار الشديد بالأنسجة السليمة أو بالجهاز المناعي. تستكشف هذه الدراسة أداة غير مألوفة لهذه المهمة — موجات تيراهرتز (THz) مكثفة، وهي نوع من الضوء غير المرئي بين الموجات الدقيقة وتحت الحمراء. يظهر الباحثون أن نبضات THz عريضة النطاق ومُعدَّلة بعناية وذات حقل عالٍ يمكن أن تحفز الخلايا السرطانية على «الانتحار» بشكل منضبط، دون طهو النسيج أو التسبب بموت خلوي فوضوي يؤدي إلى الالتهاب.
لماذا يهم الموت الخلوي الهادئ
تدفع العديد من علاجات السرطان الشائعة الخلايا نحو الموت، لكنها غالباً ما تفعل ذلك بتكاليف جانبية. قد تفقد الأدوية والمواد البيولوجية فعاليتها مع تطور المقاومة في الأورام، وقد تُضعف الجهاز المناعي. يمكن أن تُصيب الطرق الفيزيائية مثل الأشعة السينية أو الإشعاع أو الاستئصال بالحرارة الأنسجة السليمة المحيطة، مما يسبب في كثير من الأحيان نخر الخلايا — وهو شكل عنيف من الموت الخلوي يثير الالتهاب والألم. قد يوفر أسلوب يدفع بدل ذلك نحو الاستماتة (apoptosis)، عملية تفكك ذاتي منظم ومرتب للخلايا، وسيلة أقل إيلاماً بكثير لتقليص الأورام، لا سيما تلك القريبة من الجلد.
موجات تيراهرتز تلتقي خلايا سرطان الثدي
ركز الفريق على خلايا سرطان الثدي البشرية (MCF‑7)، وهي نوع من الخلايا الظهارية يُستخدم كثيراً في الدراسات المعملية. عرّضوا هذه الخلايا لنبضات THz عريضة النطاق وقوية جداً لمدة تصل إلى أربع ساعات أثناء الحفاظ على درجة حرارتها ضمن النطاق الطبيعي للجسم. وصلت شدات الحقل إلى عدة ملايين فولت لكل سنتيمتر، أعلى بكثير من الأجهزة اليومية. في ظل هذه الظروف، ارتفعت نسبة الخلايا التي تدخل الاستماتة تدريجياً مع زمن التعرض. مع أعلى شدة THz جُربت، دخلت ما يقرب من 99% من الخلايا السرطانية في الاستماتة، بينما مات أقل من 1% بالنخر. تشير هذه الموجة الضخمة والنظيفة من الموت المبرمج إلى أن نبضات THz تفعل أكثر من مجرد تسخين الخلايا.
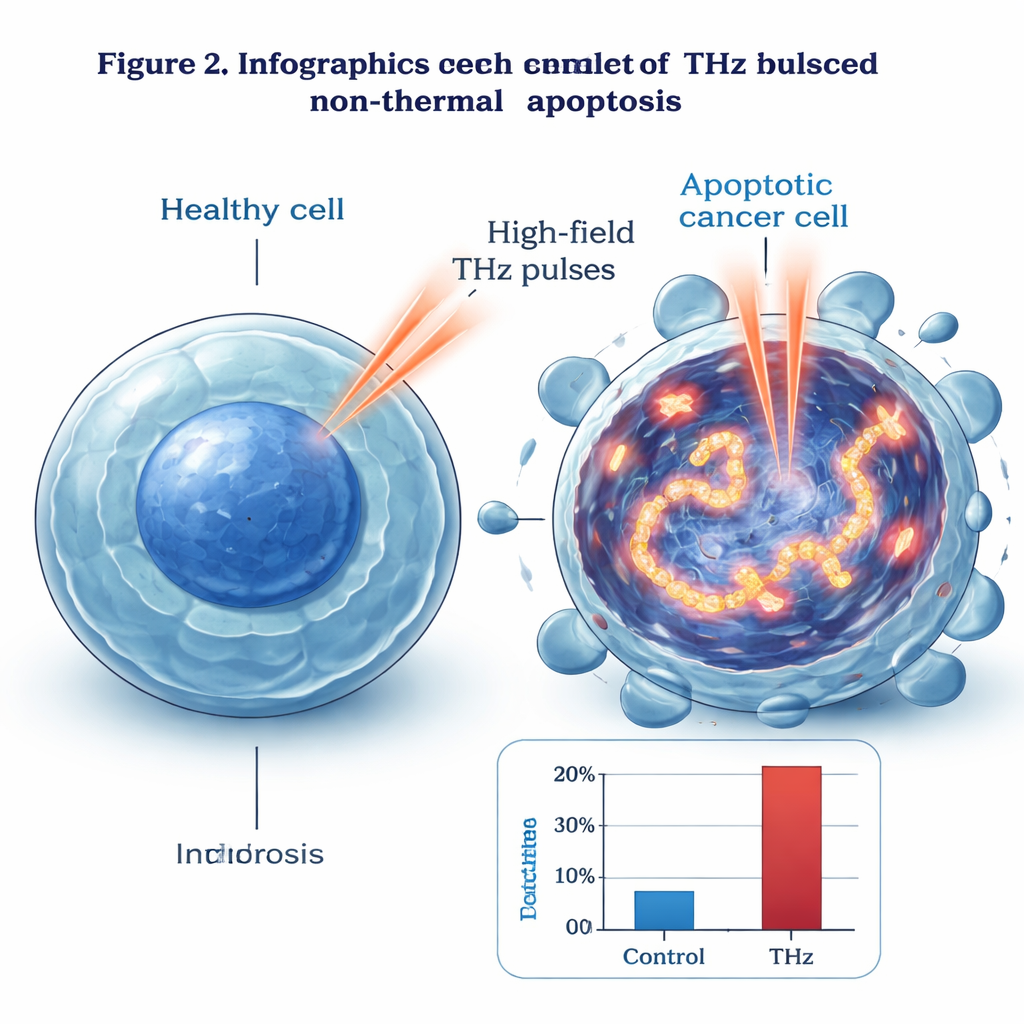
تأثيرات غير حرارية وحدود الحرارة الآمنة
بما أن الماء يمتص إشعاع THz بقوة، فالقلق الواضح هو التسخين العرضي. استخدم العلماء تصويراً حرارياً لتتبع تغيرات الحرارة أثناء الإشعاع. حتى بعد أربع ساعات عند شدة متوسطة، ارتفعت حرارة الخلايا السرطانية بنحو 3 °C فقط، وبقيت نسبة النخر أقل من 4%. أظهرت تجارب ضابطة منفصلة عرّضت الخلايا للحرارة فقط لأربع ساعات أن درجات الحرارة دون 41 °C أنتجت موتاً ضئيلاً، بينما حدث ارتفاع حاد في النخر فوق 43 °C. حتى عند أقوى إعدادات THz لديهم، حافظ الباحثون على درجات الحرارة عند أو دون عتبة 43 °C ولا يزالون يرون استماتة شبه كاملة مع نخر ضئيل. من خلال خفض معدل تكرار النبضات، أظهروا أنه يمكن ضبط الحرارة مع الحفاظ على تأثير مضاد للأورام قوي، مما يؤكد أن آلية غير حرارية تعمل هنا.
هز الحمض النووي وتشغيل جينات الموت
للبحث عن تلك الآلية، فحصت المجموعة داخل الخلايا. تحت المجهر الإلكتروني، أظهرت الخلايا المعالجة بـTHz علامات مبكرة كلاسيكية للاستماتة: تكثف المادة الوراثية، تغير النوى، وغشاء خارجي سليم. باستخدام علامة فلورية تُسمى γ‑H2AX، كشفوا عن انكسارات مزدوجة واسعة في الحمض النووي — أضرار أكثر تواتراً بكثير في الخلايا المعرضة بالمقارنة مع الضوابط غير المعالجة أو المعالجة بحرارة خفيفة. تبع نمط الضرر ملف كثافة حزمة THz، إذ ازداد نحو مركزها. كشفت تحليلات الجينات والبروتينات أن مجموعة من الجزيئات المستجيبة للإجهاد والضرر، مثل GADD45B و c‑Jun، نُشطت بقوة، بينما لم تتغير عناصر معروفة في مسارات الموت التقليدية، بما في ذلك p53 والعديد من الكاسبيز، كثيراً. يقترح المؤلفون أن الحقول الشديدة لـTHz قد تُحدث «رنينات» اهتزازية عنيفة في الحمض النووي، تشد وتكسر اللولب المزدوج بشكل فيزيائي ثم تُفعّل مسار استماتة مميز مستقل عن p53 والكاسبيز.
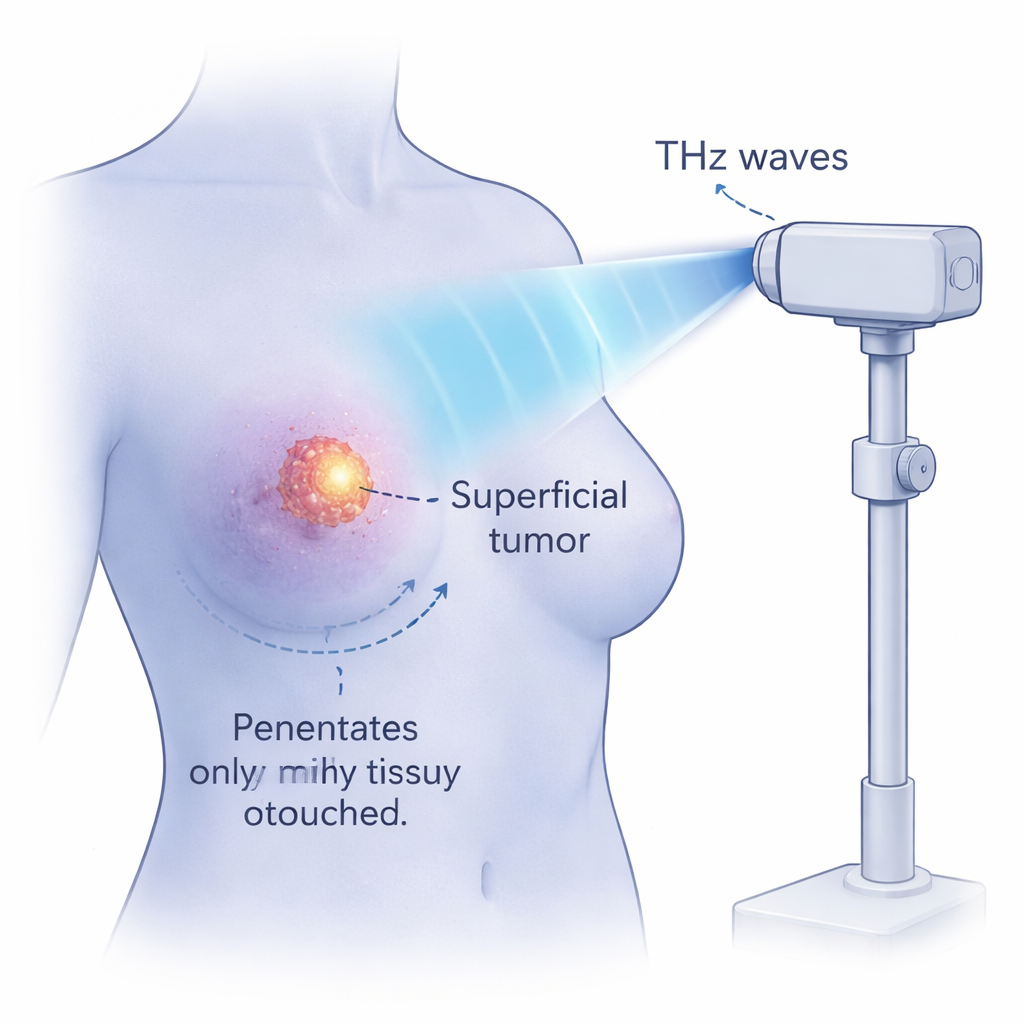
من طبق المختبر إلى علاجات مستقبلية
بينما أُجريت هذه التجارب في مزروعات خلوية، فهي تلمح إلى أسلوب جديد من العلاج الفيزيائي للسرطان. تبدو موجات THz ذات الحقل العالي قادرة على اختراق عدة مليّمتريات في الأنسجة الرطبة — بما يكفي للوصول إلى الأورام السطحية — ومع ذلك تفقد شدتها بسرعة، ما قد يوفر حماية للأعضاء الأعمق. وبما أن التأثير أساساً غير حراري، فقد يكون من الممكن، من الناحية النظرية، قتل الخلايا السرطانية طبقة بطبقة دون حرق الأنسجة المحيطة أو إثارة التهاب قوي. يبقى الكثير من العمل: يجب تأكيد آلية «الرنين» المقترحة للحمض النووي، وتحتاج السلامة للخلايا الطبيعية إلى اختبارات دقيقة، كما أن الدراسات الحيوانية والسريرية مطلوبة. ومع ذلك، تفتح هذه الأبحاث باب الفكرة القائلة إن نبضات ضوئية مصممة بعناية، مضبوطة على حركات الجزيئات البيولوجية الطبيعية، قد توفر مستقبلاً طريقة دقيقة وأكثر لطفاً لاستئصال أنواع معينة من السرطان.
الاستشهاد: Zhou, H., Wei, X., Peng, XY. et al. Efficient apoptosis via double-strand breaks of DNA in human epithelial cells induced by non-thermal effect of high-field broadband terahertz waves. Sci Rep 16, 6163 (2026). https://doi.org/10.1038/s41598-026-37373-6
الكلمات المفتاحية: علاج السرطان بتيراهرتز, استماتة غير حرارية, انكسارات مزدوجة لسلاسل الحمض النووي, خلايا سرطان الثدي, استئصال الأورام الفيزيائي