Clear Sky Science · ar
إطار ثلاثي الأوميكس وتعلم آلي يحدد علامات تنبؤية وبصمات أيضية في الإنتان
لماذا يهم هذا للأشخاص المصابين بعدوى شديدة
الإنتان هو استجابة مهددة للحياة للعدوى يمكن أن تدفع الجهاز المناعي إلى فرط نشاط وتتسبب في فشل الأعضاء. يعرف الأطباء أن الكشف المبكر عن الإنتان وتفصيل العلاج لكل مريض يمكن أن ينقذ الأرواح، لكن اختبارات الدم الحالية أدوات محدودة: في الغالب لا تُظهر من سيتحسّن ومن يواجه أعلى مخاطر. تستخدم هذه الدراسة مزيجاً قوياً من ثلاثة أنواع من القياسات الجزيئية والتعلم الآلي الحديث للبحث عن إشارات تحذيرية أدق في دم مرضى الإنتان.
النظر إلى الدم عبر ثلاثة منظورات مختلفة
بدلاً من التركيز على نوع واحد من الجزيئات، قام الباحثون بتحليل نفس المرضى بثلاث طرق في آن واحد. قاسوا أي الجينات كانت مفعّلة أو مطفأة (النسخ–أوميكس)، وأي البروتينات كانت حاضرة وفعالة فعلاً (البروتيومكس)، وأي الجزيئات الأيضية الصغيرة كانت دارة في الدم (الميتابولومكس). جمعوا دماء من 21 مريضاً بالإنتان و10 متطوعين أصحاء واستخدموا إحصاءات متقدمة لرصد كيفية تغير هذه الطبقات الثلاث معاً في المرض. تساعد هذه النظرة "ثلاثية الأوميكس" على التغلب على مشكلة رئيسية: في الإنتان، قد ينفصل نشاط الجينات عن مستويات البروتين، لذا فإن النظر إلى طبقة واحدة فقط قد يكون مضللاً.
تدريب الخوارزميات لرصد أنماط عالية المخاطر
من بين آلاف الجينات والبروتينات، استخدم الفريق أولاً طريقة شبكية لإيجاد مجموعات تتحرك معاً في الإنتان. ثم تحققوا من تلك المجموعات عبر البروتينات التي اختلفت بوضوح بين المرضى والمراجعين الأصحّاء، ووصلوا إلى 32 مرشحاً قوياً. لتضييق هذه القائمة أكثر، لجأوا إلى التعلم الآلي، مستخدمين خوارزميتين مكملتين لاقتلاع الإشارات الأضعف والاحتفاظ بالأكثر معلوماتية. عندما اختبروا كيف ترتبط هذه الجينات المتبقية بالبقاء على قيد الحياة في مجموعة بيانات إنتان عامة وكبيرة، برز اثنان: TPR وERN1. أميل المرضى ذوو المستويات الأعلى من TPR إلى البقاء لفترة أطول، بينما ارتبطت المستويات الأعلى من ERN1 بنتائج أسوأ.
ربط خلايا المناعة والاضطراب الأيضي
لم تتوقف الدراسة عند الجينات والبروتينات. بمسح آلاف المستقلبات في دم المرضى، وجد الباحثون 136 جزيئاً صغيراً تتبعوا عن كثب TPR وERN1. الكثير منها كان ضمن مسارات تتعامل مع دهون أغشية الخلايا والأحماض الدهنية، وهي أساسية لكيفية إشارة خلايا المناعة وانتشار الالتهاب. في الوقت نفسه، أظهر تحليل الخلية الواحدة — الذي يفحص خلايا المناعة في الدم على مستوى كل خلية بدلاً من دمجها — أن TPR وERN1 نشطان خصوصاً في البلعميات الوحيدة، والبالعات، وخلايا القاتل الطبيعي. مجتمعة، تشير هذه النتائج إلى أن العلامتين تقعان عند مفترق طرق بين خلايا مكافحة العدوى في الجسم والطريقة التي تستخدمها تلك الخلايا وتعيد تشكيل الدهون والطاقة أثناء الإنتان.
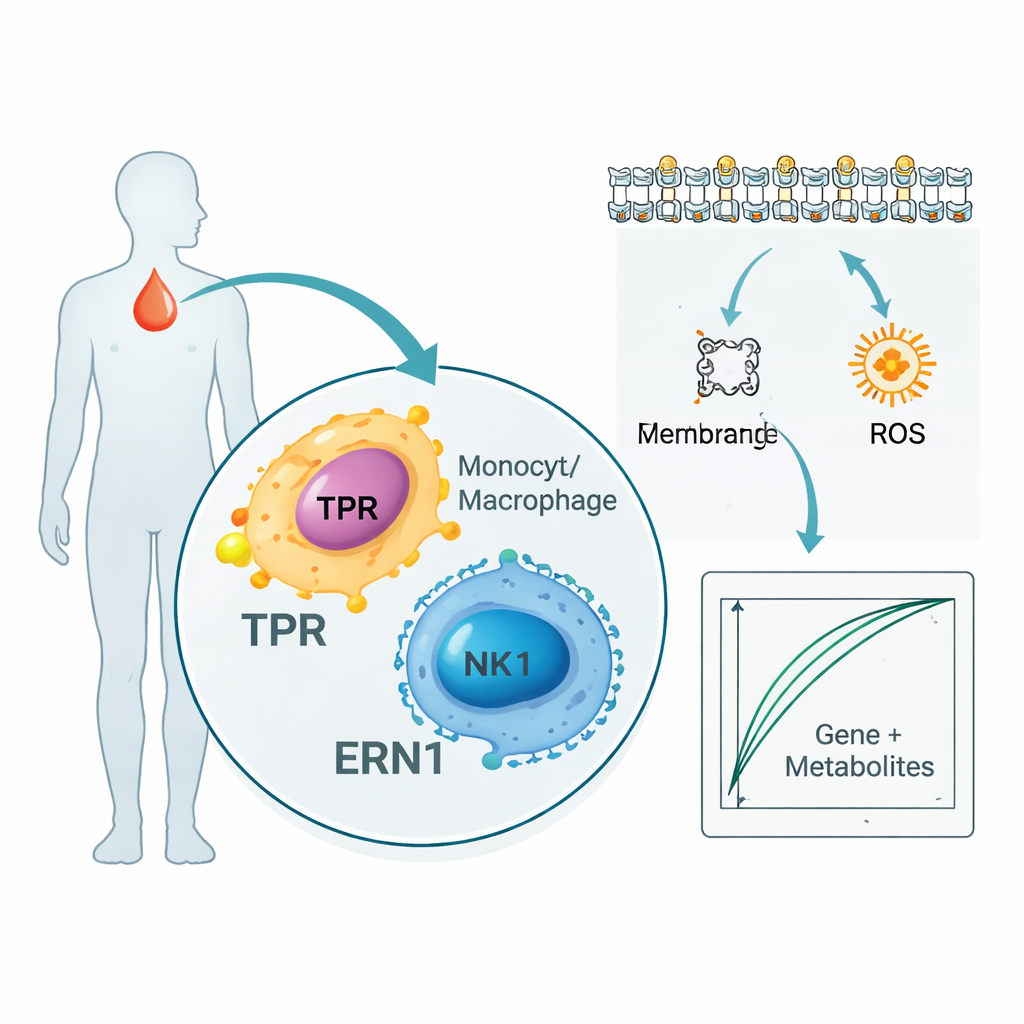
بناء اختبار دم نموذجي إثباتي للمفهوم
لاستكشاف كيف قد تُترجم هذه الاكتشافات إلى تطبيق عملي، جمع المؤلفون الجينين مع خمسة من أكثر المستقلبات إفادة لتدريب نماذج حاسوبية بسيطة تفرّق بين مرضى الإنتان والأشخاص الأصحّاء. في مجموعة البيانات الداخلية الصغيرة لديهم، تمكنت هذه البصمات المجمعة "جين + مستقلب" من التمييز تقريباً بشكل كامل بين المصابين بالإنتان وغيرهم. كما تحقّق الباحثون من قواعد بيانات عامة كبيرة تربط بروتينات الدم بمخاطر الأمراض لعشرات الآلاف من الأشخاص ووجدوا أن مستويات بروتينات TPR وERN1 كانت مرتبطة باستمرار بحالات متعلقة بالإنتان، مضيفة طبقة دعم أخرى. ومع ذلك، يؤكد المؤلفون أن هذه النماذج أدوات في مرحلة مبكرة مصممة لتوليد فرضيات، وليست اختبارات جاهزة للاستخدام بجانب السرير.
مركبات نباتية كمقدمات مبكرة لا كعلاجات
في خطوة أخيرة، تساءل الفريق عما إذا كانت هناك جزيئات طبيعية قد تؤثر على TPR أو ERN1. بحثوا في قاعدة بيانات متخصصة تضم نحو 500 مركب منقّح من الأدوية التقليدية الصينية، لكل منها ملف نشاط جيني. بدا أن عدة مركبات تدفع هذين الجينين بقوة نحو الأعلى أو الأسفل في خلايا مزروعة مختبرياً، مما يوحي بأنها قد تساعد يوماً ما الباحثين على استكشاف بيولوجيا الإنتان أو تصميم أدوية جديدة. مع ذلك، تأتي هذه النتائج من مطابقة حاسوبية فقط: فهي لا تثبت أن أيّاً من هذه المواد آمنة أو فعالة للبشر المصابين بالإنتان.
ما الذي تقوله هذه الدراسة فعلاً
تقدّم هذه الدراسة خريطة مفصّلة بدلاً من حل نهائي. من خلال نسج ثلاث طبقات جزيئية، وبيانات الخلية الواحدة، والتعلم الآلي، يبرز المؤلفون TPR وERN1 — والتغيرات الأيضية المتصلة بهما — كنقاط إرشادية واعدة لكيفية اختلال توازن الجهاز المناعي والأيض في الإنتان. للقراء غير المتخصصين، الرسالة الأساسية أن الإنتان ليس مرضاً واحداً موحّداً بل نمط متغيّر من حالات مناعية وأيضية، وأن اختبارات دم أكثر ذكاءً قد تساعد الأطباء في المستقبل على رؤية الحالة التي يكون فيها المريض وتكييف العلاج وفقاً لذلك. قبل أن يحدث ذلك، لا بد من اختبار هذه الإشارات المبكرة وتأكيدها في مجموعات مرضى أكبر وأكثر تنوعاً وفي تجارب مخبرية يمكنها إثبات السببية.
الاستشهاد: Li, X., Ke, G., Hu, Y. et al. A tri-omics and machine learning framework identifies prognostic biomarkers and metabolic signatures in sepsis. Sci Rep 16, 6648 (2026). https://doi.org/10.1038/s41598-026-37342-z
الكلمات المفتاحية: مؤشرات حيوية للإنتان, تعدد الأوميكس, التعلم الآلي في الطب, أيض الجهاز المناعي, تشخيص دقيق