Clear Sky Science · ar
استهداف محور Akt–EphA2 والتلاصق بين الخلايا يعزز الحساسية للأنويكيس في خلايا السرطان
لماذا تهم الخلايا السرطانية الطافية
عندما تنفصل خلايا السرطان عن الورم وتنتقل عبر مجرى الدم، يفترض أن تموت عادة لأنها تفقد تماسها مع الأنسجة المحيطة. هذا البرنامج الوقائي المدمج، المسمى موت الخلايا الناجم عن الانفصال، يساعد على منع نمو خلايا في أماكن غير مناسبة. لكن الخلايا السرطانية النّقيلية غالبًا ما تتعلّم تجاهل هذا الإشارة وتظل حية أثناء الطفو، مما يسهل عليها تكوين أورام جديدة. تطرح هذه الدراسة سؤالًا بسيطًا في ظاهره: إذا أعدنا حسًا ميكانيكيًا رئيسيًا لـِ خلايا سرطان الثدي العدوانية، هل يمكننا إجبار هذه الخلايا المتجولة على الموت، وإن لم يحدث ذلك، ما الحيل الاحتياطية التي تستخدمها للبقاء؟
إيقاظ حاسة فقدتْها الخلايا
تختبر الخلايا باستمرار مدى صلابة محيطها عن طريق سحبها للهياكل التي تثبتها. في الأنسجة السليمة، يؤدي فقدان التماس أو الهبوط على سطحٍ رخو جدًا إلى تحفيز الانتحار الذاتي. البروتين تروبوميوسين 2.1 (Tpm2.1) هو جزء مهم من آلة الشد الداخلية هذه وغالبًا ما يكون ناقصًا أو منخفضًا في الخلايا السرطانية. استخدم الباحثون سلالة خلايا سرطان الثدي النّقيلية المدروسة على نطاق واسع وهندسوها لإنتاج المزيد من Tpm2.1، مستعيدين جزءًا كبيرًا من استشعار الصلابة هذا. عندما أُجبرت هذه الخلايا المعدلة على النمو في أطباق خاصة غير لاصقة تحول دون التصاقها، شهدت بالفعل مزيدًا من موت الخلايا، ونمت بمعدل أبطأ، وتحركت أقل مقارنة بالخلايا السرطانية غير المعدلة. ومع ذلك، حتى بعد عدة أيام في حالة تعليق، بقي نحو 70% من الخلايا المعبرة عن Tpm2.1 على قيد الحياة، ما يوحي بأن إحياء حاسة اللمس وحده لا يحل المشكلة تمامًا.
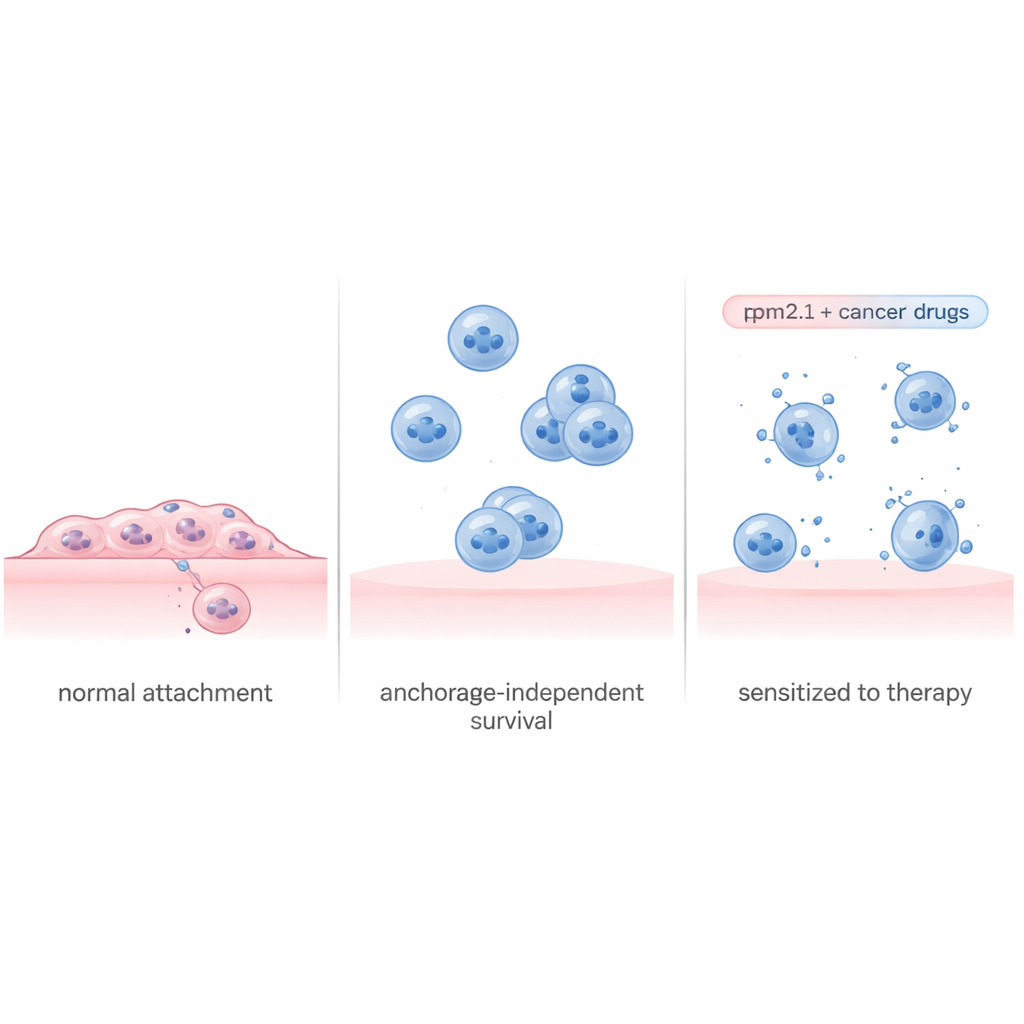
قراءة كتاب بقاء الخلايا السرطانية
لفهم سبب وفاة بعض الخلايا وبقاء غيرها، قسم الفريق الخلايا الطافية المعبرة عن Tpm2.1 إلى مجموعتين: تلك التي أظهرت علامات مبكرة للموت وتلك التي بدت سليمة. ثم قاسوا أي الجينات كانت مفعلة أو مطفأة في كل مجموعة على مدى أربعة أيام. أظهرت الخلايا المحتضرة توقّفًا واسعًا للبرامج المعنية بانقسام الخلايا وإصلاح الحمض النووي والالتصاق، إلى جانب إشارات إجهاد بدت كطريقٍ بلا عودة نحو الانتحار الخلوي. بالمقابل، نشّطت الخلايا الناجية خطة بقاء منسقة. في وقتٍ مبكر بعد الانفصال، شغّلت مسارات التهابية ومناعية ولاحقًا رفعت دُفعات ضخمة من دوائر النمو والبقاء، بما في ذلك مسار معروف يتمحور حول البروتين Akt. في الوقت نفسه، زادت بشكل كبير من التعبير عن جينات تساعد الخلايا على الالتصاق ببعضها البعض، مما أتاح لها تشكيل تجمعات واقية حتى دون التمسك بالمصفوفة المحيطة.
القوة في الأعداد: كيف تقاوم تجمعات الخلايا الموت
بما أن بيانات الجينات أشارت إلى زيادة الالتصاق بين الخلايا، اختبر الباحثون ما إذا كان الاكتظاظ البسيط يمكن أن يساعد الخلايا على البقاء في حالة تعليق. عندما نمت الخلايا المعبرة عن Tpm2.1 بكثافة عالية، حيث كان تكوّن التجمعات سهلاً، مات عدد أقل بكثير من الخلايا مقارنةً عندما كانت متناثرة. برز جزيء لاصق واحد، ICAM1، كمُرتفع بشكل واضح في الخلايا الناجية وهو معروف بالفعل بمساعدته على تشكيل تجمعات الخلايا الورمية الدائرة واستقرارها في أنسجة بعيدة. أدى حجب ICAM1 بمثبط صغير الجزيئات إلى موت عدد أكبر من الخلايا المعبرة عن Tpm2.1 في التعليق، بينما لم يؤثر بشكل كبير على الثقافات المعيارية الملتصقة. تدعم هذه النتائج فكرة أنه، بمجرد استعادة ميكانيكا الخلايا جزئيًا، يمكن للخلايا السرطانية أن تتجنب الموت ببساطة عبر التمسك ببعضها البعض بدلًا من الالتصاق ببيئتها.
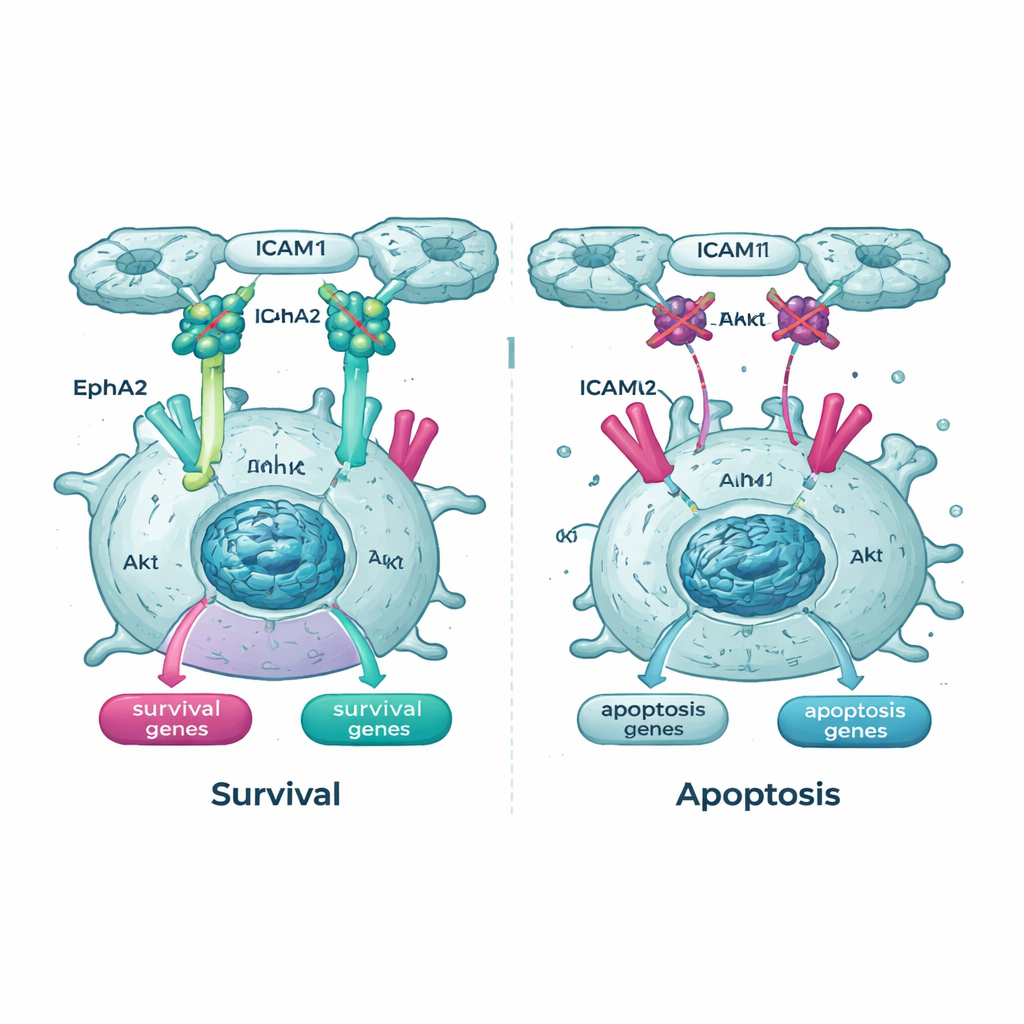
قطع خطوط الحياة الرئيسية داخل الخلية
أبرزت الدراسات الجينية أيضًا مسار Akt وأحد شركائه، مستقبل يُدعى EphA2، كخطّ حياة مهم للخلايا السرطانية المعلقة. في الخلايا المعبرة عن Tpm2.1، كان الشكل النشط للفوسفوريلات من Akt أقل في التعليق مقارنة بالخلايا الضابطة، كما انخفضت مستويات EphA2 ونشاطه كذلك. عندما عالج الفريق الخلايا بأدوية تحجب Akt أو EphA2، أصبحت كل من الخلايا السرطانية العادية والمعبرة عن Tpm2.1 أكثر عرضة للموت في التعليق. ومن اللافت أن الخلايا التي أعيد لها استشعار الصلابة كانت حسّاسة بشكل خاص لهذه الأدوية بمرور الوقت، مما يوحي بأنه بمجرد إعادة تشغيل فحوصات السلامة الميكانيكية جزئيًا، تصبح هذه الخلايا معتمدة أكثر على إشارات البقاء المتبقية.
تحويل حالة متهيئة إلى نقطة ضعف قاتلة
لغير المتخصص، الرسالة الأساسية هي أن إصلاح مفتاح أمان واحد معطّل في الخلايا السرطانية — قدرتها على الشعور والاستجابة لفقدان التماس — ضروري لكنه غير كافٍ لإجبارها على الانتحار الخلوي. الخلايا التي تبقى تفعل ذلك من خلال التجمع وإعادة توجيه دوائرها الداخلية عبر مسارات نمو وبقاء بديلة. تُظهر هذه الدراسة أن استعادة استشعار الصلابة بواسطة Tpm2.1 يضع خلايا سرطان الثدي النّقيلية في حالة «تهيؤ» تجعلها أقرب إلى الموت لكنها ليست مصممة عليه بعد. ومن ثم، عن طريق حجب محور Akt–EphA2 وتعطيل التلاصق بين الخلايا عبر ICAM1، يمكن للباحثين دفع هذه الخلايا المتهيئة إلى حافة الانهيار وزيادة موت الخلايا الناجم عن الانفصال بشكل كبير. عمليًا، تصف الدراسة استراتيجية للعلاجات المركبة المستقبلية تهدف إلى القضاء على الخلايا الورمية الطافية قبل أن تتمكن من زرع نقائل جديدة.
الاستشهاد: Vivante, A.G., Dwivedi, N., Sheetz, M.P. et al. Targeting the Akt–EphA2 axis and cell–cell adhesion enhances anoikis sensitivity in cancer cells. Sci Rep 16, 6197 (2026). https://doi.org/10.1038/s41598-026-37327-y
الكلمات المفتاحية: انبثاث سرطان الثدي, تماسك الخلايا, الأنويكيس, إشارات Akt, استشعار الصلابة