Clear Sky Science · ar
تصوير الجزيئات البيولوجية بين الخلايا باستخدام مؤشرات البروتين الفلوري ذات مراسي ليفية-PEG
مراقبة تواصل الخلايا في الزمن الحقيقي
تعتمد أدمغتنا وأجسامنا على حوار كيميائي مستمر بين الخلايا. تنتقل الأيونات والناقلات العصبية عبر فراغات صغيرة لنقل الرسائل، لكن هذه الإشارات السريعة والعابرة يصعب رؤيتها دون أن يتم إزعاجها. تعرض هذه الدراسة طريقة بسيطة «لطلاء» الخلايا الحية بمؤشرات متوهجة تلتصق بسطحها الخارجي، مما يتيح للعلماء مشاهدة هذه الرسائل — لا سيما أيونات البوتاسيوم والناقل العصبي الغلوتامات — مباشرة وبتفصيل. 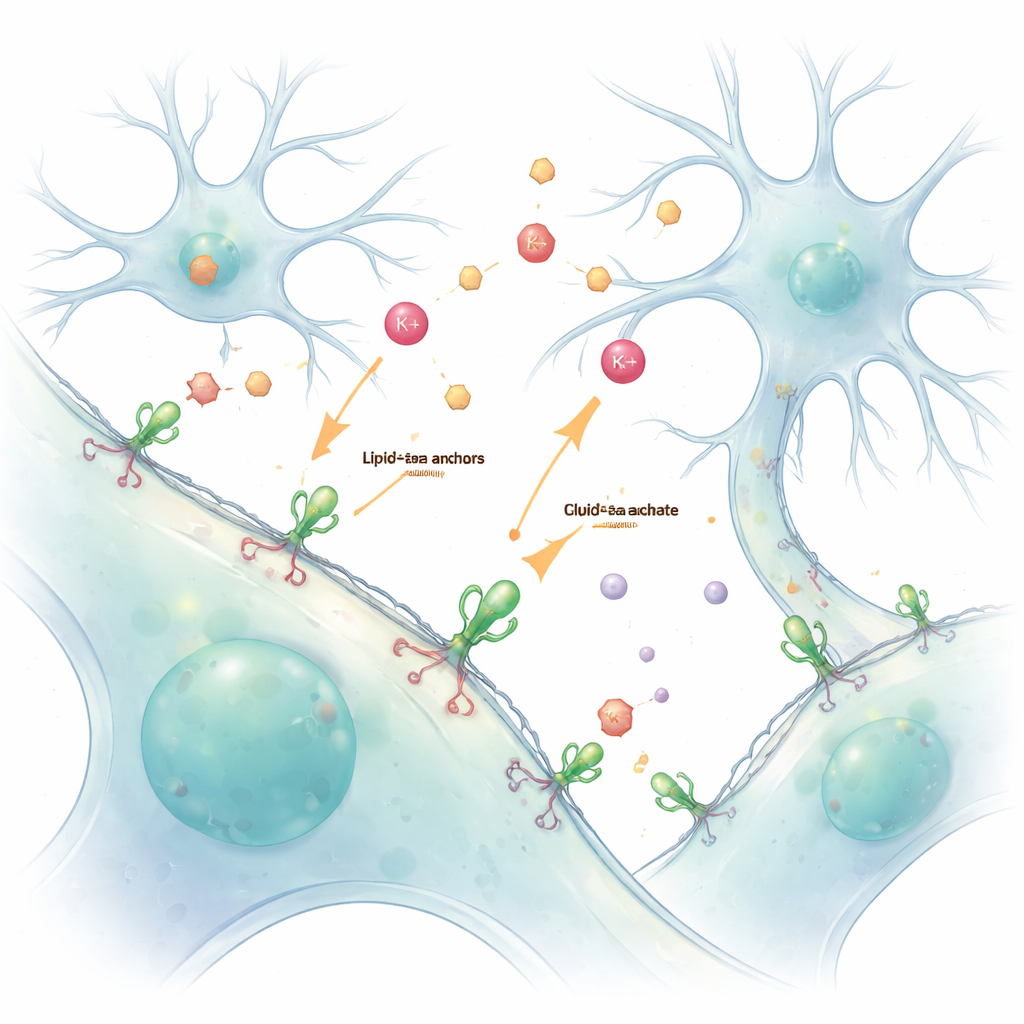
طريقة جديدة لوضع علامة على سطح الخلية
تقليديًا، يقوم الباحثون ببرمجة الخلايا لإنتاج مؤشرات بروتينية فلورية من حمضها النووي. وعلى الرغم من قوة هذه المقاربة الجينية، فإنها غالبًا ما تضع المؤشرات داخل الخلية، ما يصعّب فصل ما يحدث داخل الخلية عما يحدث خارجها. حل المؤلفون هذه المشكلة باستخدام مقبض كيميائي يسمى مرساة ليفية–PEG. يندمج أحد طرفي هذا الجزيء في الغشاء الخارجي، بينما يرتبط الطرف الآخر كيميائيًا بمؤشر بروتيني فلوري. عند إضافة هذه المؤشرات المحضرة إلى الخلايا الحية، فإنها تغطي السطح الخارجي تلقائيًا، مشكلة طبقة مضيئة ومستقرة تبلغ عما يحدث في السائل المحيط.
تحويل البوتاسيوم والغلوتامات إلى ضوء
كيّف الفريق مؤشرين فلوريين موجودين بالفعل: GINKO2، الذي يستجيب لأيونات البوتاسيوم، وR-iGluSnFR1، الذي يستجيب للغلوتامات. نقّوا هذه البروتينات من بكتيريا ثم ربطوها بمراسي ليفية–PEG. في خلايا بشرية مزروعة، شكّل مستشعر البوتاسيوم المرتبط خطًا ناعمًا على طول سطح الخلية وتوهّج كلما زاد تركيز البوتاسيوم خارج الخلايا، ثم خفت ضوؤه عند هبوط المستويات. والأهم أن خواصه الضوئية وحساسيته طابقت إلى حد كبير المؤشر الأصلي غير المعدّل في تجارب الأنبوب، مما يدل على أن الربط لم يقلل من أدائه. كان الأمر ذاته صحيحًا بالنسبة لمستشعر الغلوتامات، الذي بقي مستجيبًا بعد الربط وأبرز بوضوح الغلوتامات في الفراغ خارج الخلايا مباشرة.
الاستماع إلى الخلايا العصبية في المزارع والشرائح
انتقل الباحثون بعد ذلك إلى خلايا عصبية من قرن آمون للفأر، وهي منطقة دماغية مهمة للتعلّم والذاكرة. قاموا بتغطية هذه الخلايا العصبية بمستشعر الغلوتامات المرتبط بالليف–PEG وحَمّلوا داخل نفس الخلايا بصبغة كالسيوم منفصلة تبلغ عن النشاط الكهربائي. باستخدام مجهر الانعكاس الكلي الداخلي، تمكنوا من مشاهدة ومضات حمراء من الغلوتامات على سطح الخلية بينما أبلغت الإشارات الخضراء داخل الخلايا عن إطلاق النبضات. أظهر هذا العرض ثنائي اللون أن المستشعرات المرتبطة يمكنها تتبع الإطلاق العفوي للناقل العصبي دون أي تعديل وراثي للخلايا العصبية نفسها.
رسم خرائط الأمواج الكيميائية عبر نسيج الدماغ
بعد ذلك، اختبر الفريق الطريقة في شرائح دماغية حادة تحافظ على التوصيلات الطبيعية لقرن آمون. وضعوا مستشعر البوتاسيوم المرتبط على الشرائح ونبّهوا الألياف العصبية كهربائيًا. أنتج المستشعر المرتبط زيادات واضحة وقابلة للتكرار في الفلورة بعد كل منبه، بينما تسرّبت المستشعرات غير المرتبطة بسرعة ووفرت إشارات ضعيفة وغير مستقرة. عن طريق غمر الشرائح في محاليل ذات مستويات معروفة من البوتاسيوم، وتصحيح الوميض الذاتي للنسيج، بنى المؤلفون منحنى معايرة وقدّروا تراكيز البوتاسيوم خارج الخلايا الفعلية. كانت المستويات القاعدية حوالي 2.5 ملي مولار وارتفعت إلى نحو 3.4 ملي مولار مع تحفيز معتدل، بما يتوافق مع قياسات الأقطاب التقليدية. كشفت المستشعرات المرتبطة لكل من البوتاسيوم والغلوتامات كيف تنتشر هذه الإشارات بشكل مختلف: بقيت تغيّرات الغلوتامات قريبة من المشابك النشطة، بينما امتدت زيادات البوتاسيوم لمئات الميكرومترات، مما يلمح إلى تأثيرات أوسع على قابليّة الإثارة في الشبكة. 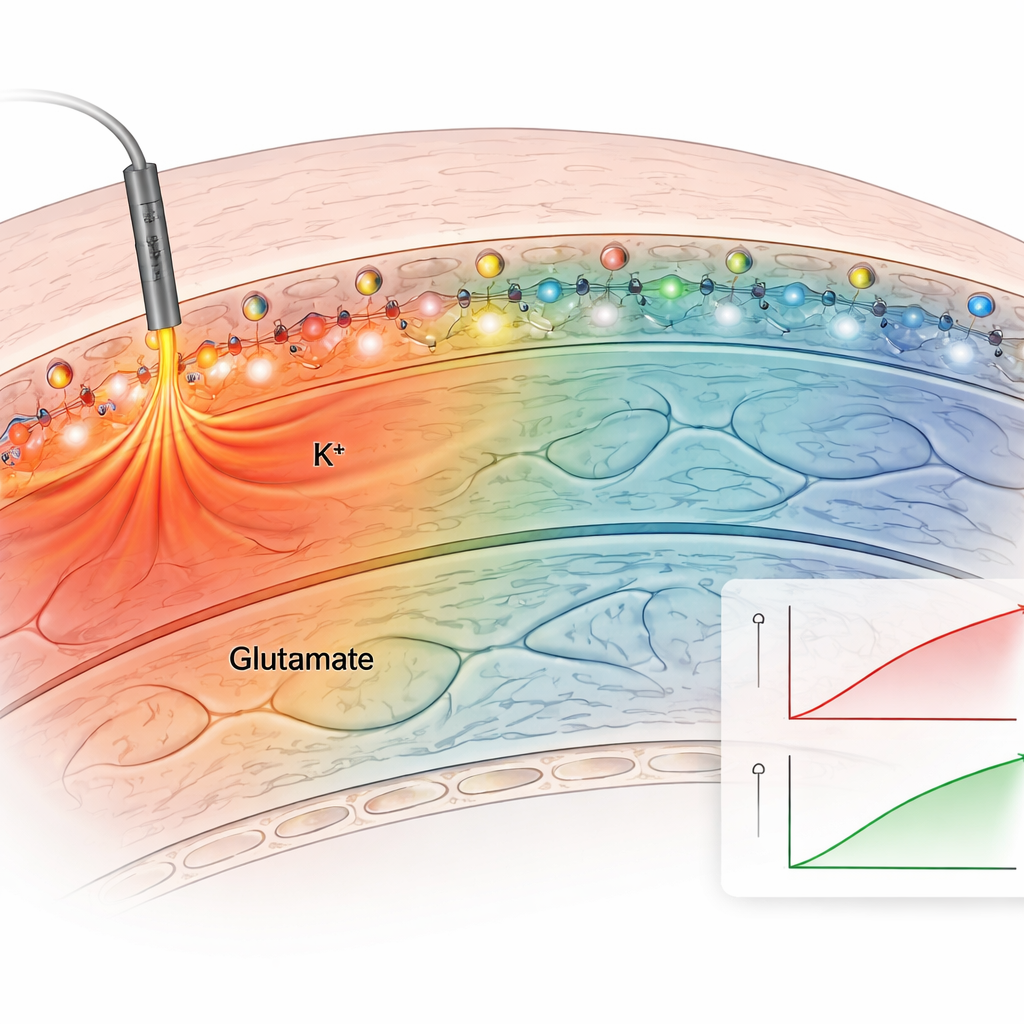
استقصاء كيفية تنظيف الدماغ وتوليد الإشارات
لأن المستشعرات مثبتة على سطح الخلية، تمكن المؤلفون من تفكيك العمليات التي تشكّل هذه الأمواج خارج الخلايا. أدى حجب ناقلات الغلوتامات، التي تمتص الغلوتامات عادةً، إلى أن يظهر مستشعر الغلوتامات المرتبط إشارات أكبر وأطول دوامًا، مؤكّدًا أن الامتصاص المحلي يحدّ من انتشار الغلوتامات. قلّل حجب مستقبلات الغلوتامات من نوع AMPA كلًا من الاستجابات الكهربائية وإشارات البوتاسيوم، مشيرًا إلى أن معظم ارتفاع البوتاسيوم ينشأ من الخلايا التالية للمشابك المنشطّة بواسطة الإدخال المشبكي. أمّا حجب قنوات الصوديوم بالتتروتوكسين فقلّص تغيّرات البوتاسيوم تقريبًا، رابطًا إياها مباشرةً بجهد الفعل. توضح هذه التجارب مجتمعة كيف يمكن للمستشعرات المرتبطة تحويل كيمياء معقدة وموزعة إلى أفلام وخرائط بديهية.
لماذا يهم هذا لبحوث الدماغ المستقبلية
لغير المتخصصين، الرسالة الأساسية هي أن هذا العمل يقدم طريقة سريعة وغير جينية لتغطية الخلايا والأنسجة الحية بمؤشرات جزيئية حسّاسة للغاية. بدلًا من إعادة هندسة كل نوع خلية، يمكن للعلماء إضافة بروتينات المؤشر الجاهزة من الخارج ومباشرةً تصور كيف تتغير الأيونات والناقلات العصبية في الزمن الحقيقي على سطح الخلية. تحسّن هذه المقاربة التحكم والقدرة على التكرار والدقة المكانية مع تجنّب تحديات توصيل الجينات، خصوصًا في تحضيرات حساسة مثل الشرائح الدماغية الحادة. مع تطوير المزيد من المؤشرات الفلورية لمواد كيميائية مختلفة، قد تصبح استراتيجية الربط بالليف–PEG مجموعة أدوات واسعة الاستخدام لمشاهدة اللغة الكيميائية للخلايا في أنحاء الجسم.
الاستشهاد: Mita, M., Kiyosue, K. & Tani, T. Imaging intercellular biomolecules by using fluorescent protein indicators with lipid-PEG anchors. Sci Rep 16, 6964 (2026). https://doi.org/10.1038/s41598-026-37240-4
الكلمات المفتاحية: الإشارات خارج الخلوية, المستشعرات الحيوية الفلورية, تصوير الغلوتامات, ديناميكيات البوتاسيوم, خلايا قرن آمون العصبية