Clear Sky Science · ar
الوصْف البنيوي لارتباط المعادن في إنزيم السلفوترانسفيراز البروتيني التيروسيني البشري، TPST2
لماذا تهم أيونات المعادن الصغيرة في إشارات الخلايا
داخل خلايانا، تعيد آلات جزيئية لا تحصى ضبط كيفية نمو الأنسجة، عمل الهرمونات، وتواصل خلايا المناعة بهدوء. إحدى هذه الآلات، إنزيم يُدعى TPST2، يضيف علامة كبريتات صغيرة إلى بروتينات معينة أثناء مرورها عبر مركز شحن الخلية، جهاز جولجي. تكشف هذه الدراسة كيف تساعد أيونات معادن بسيطة مثل الصوديوم والمنجنيز TPST2 على العمل بكفاءة أكبر عن طريق تقوية أجزاء من بنيته بشكل طفيف — وهو تصور قد يربط توازن المعادن داخل الخلايا بالسرطان والأمراض المرتبطة بالهرمونات. 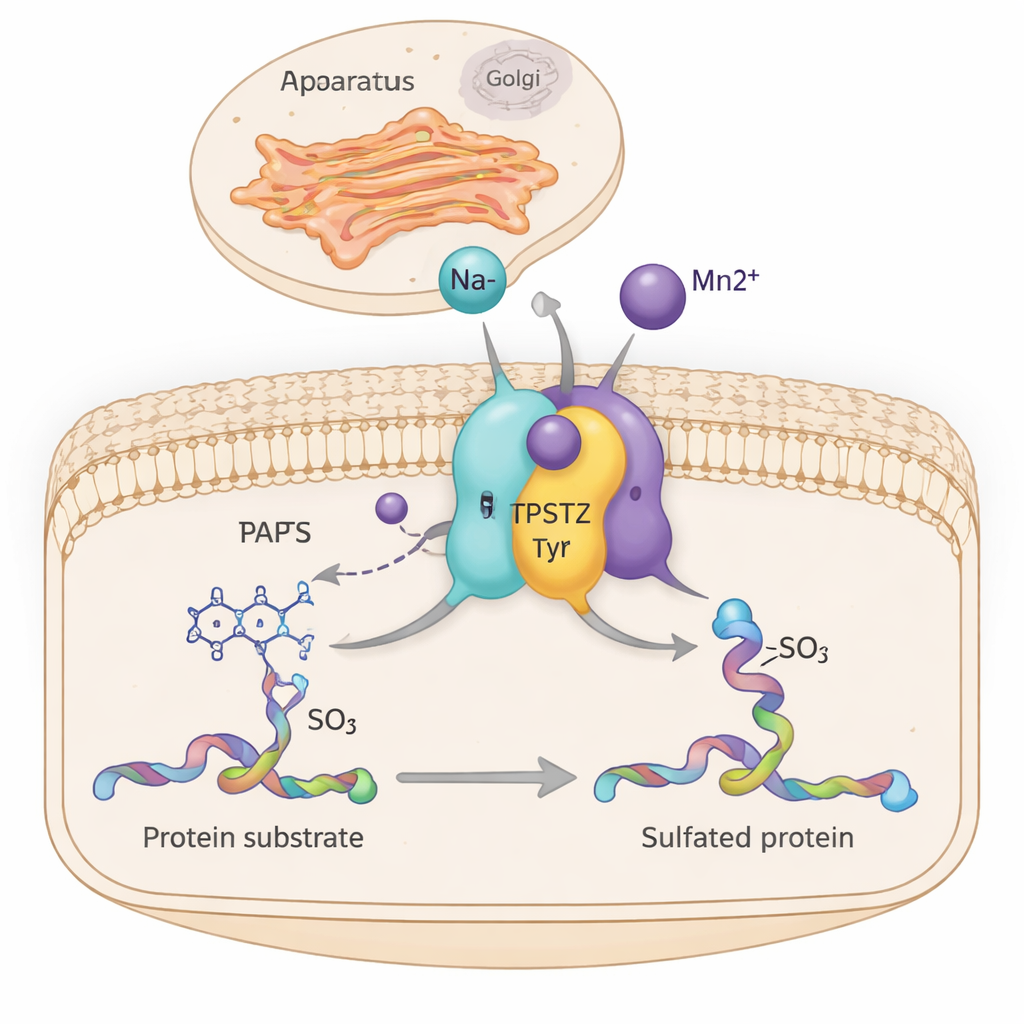
بروتين يزيّن بروتينات أخرى
ينتمي TPST2 إلى عائلة من الإنزيمات التي تنفذ «كبريتنة التيروسين»، وهو تعديل كيميائي يضاف إلى وحدات تيروسين محددة في البروتينات. تلعب البروتينات المكبَّرَت دوراً محورياً خارج الخلايا، فتؤثر في تجلط الدم، وحركة كريات الدم البيضاء، وربط الهرمونات بمستقبلاتها، وحتى في كيفية دخول الفيروسات إلى الخلايا. لدى البشر إنزيمان رئيسيان للكبريتنة، TPST1 وTPST2، اللذان يستقران في غشاء جهاز جولجي ويعدِّلان البروتينات أثناء تجهيزها للتصدير. تُظهر دراسات على الفئران أن فقدان TPST2 يعطل إنتاج هرمون الغدة الدرقية، ويعيق النمو، ويسبب العقم لدى الذكور، مما يبرز أهميته للفسيولوجيا الطبيعية.
روابط بالسرطان وتجنب المناعة
ربطت أبحاث حديثة TPST2 مباشرة بالمرض. في الميلانوما، يعدل TPST2 مكوّناً من مستقبل الإنترفيرون بطريقة تُضعف الإشارات المناعية، ومنع TPST2 يعزز فعالية علاجات نقاط التفتيش المناعية التي تستهدف PD-1. في سرطان البنكرياس، يساعد مسار يعتمد على TPST2 في تثبيت بروتين (integrin β4) يعزز نمو الورم وانتشاره. يبطئ تثبيط TPST2 في هذه النماذج انقسام الخلايا السرطانية وغزوها. ونظراً لأن TPST2 يعمل على بروتينات سطح الخلية، فإنه يعيد برمجة كيفية استشعار الخلايا لبيئتها واستجابتها لها، مما يجعله هدفاً جذاباً لعلاجات جديدة.
اكتشاف مفاتيح التشغيل المعدنية
عرف الكيميائيون الحيويون منذ زمن أن نشاط TPST2 يزداد كثيراً عندما تكون المعادن ثنائية التكافؤ مثل المنجنيز (Mn²⁺) حاضرة، لكن السبب البنيوي كان مفقوداً. في هذه الدراسة، أنتج المؤلفون النواة التحفيزية لـTPST2 البشري وكريستلوها مع ناتج تفاعل وكلٍ من الصوديوم (Na⁺) أو المنجنيز. باستخدام حيود الأشعة السينية عالي الدقة، اكتشفوا جيبين صغيرين لارتباط المعادن داخل الإنزيم، كل منهما محاط بترتيب من الذرات يشبه الشكل السداسي (ثماني السطوح). من خلال ضبط طول موجة الأشعة السينية لالتقاط البصمات المميزة للمعادن المختلفة، أكدوا أن Mn²⁺ يشغل هذه المواقع بشكل انتقائي، بينما ترتبط معادن مثل الزنك والنحاس إما بشكل ضعيف في مواقع أخرى أو لا ترتبط إطلاقاً.
تقوية الأجزاء المتحركة الأساسية بدلاً من إعادة تشكيل الكل
على نحو مفاجئ، بدا TPST2 مع الصوديوم وTPST2 مع المنجنيز متطابقين تقريباً بشكل عام؛ لم يحدث فتح أو غلق دراماتيكي للبنية. بدلاً من ذلك، أثرت المعادن بشكل رئيسي على منطقتين مرنتين بالقرب من مدخل الموقع النشِط: لولب يُدعى α3 وحلقة قريبة تُعرف بحلقة α12–α13. في الحالات الخالية من المعادن أو ذات الارتباط الفضفاض كانت هاتان المقطعتان تتحركان وتكونان جزئياً غير منظمتين. عندما يرتبط Na⁺ تصبحا أكثر انتظاماً؛ أما Mn²⁺ فيشدّهما أكثر، كما يتضح من انخفاض الحركة الحرارية في بيانات الأشعة السينية ومن تحليلات المرونة المعتمدة على الحاسوب. تزيد هذه الصلابة الإضافية بدرجة معتدلة من درجة انصهار الإنزيم ويُعتقد أنها تقلل التكلفة «الانتروبية» لتنظيم الموقع النشط — مما يجعل توجيه الركائز إلى الوضع الصحيح للكبريتنة أسهل وأسرع لِـTPST2. 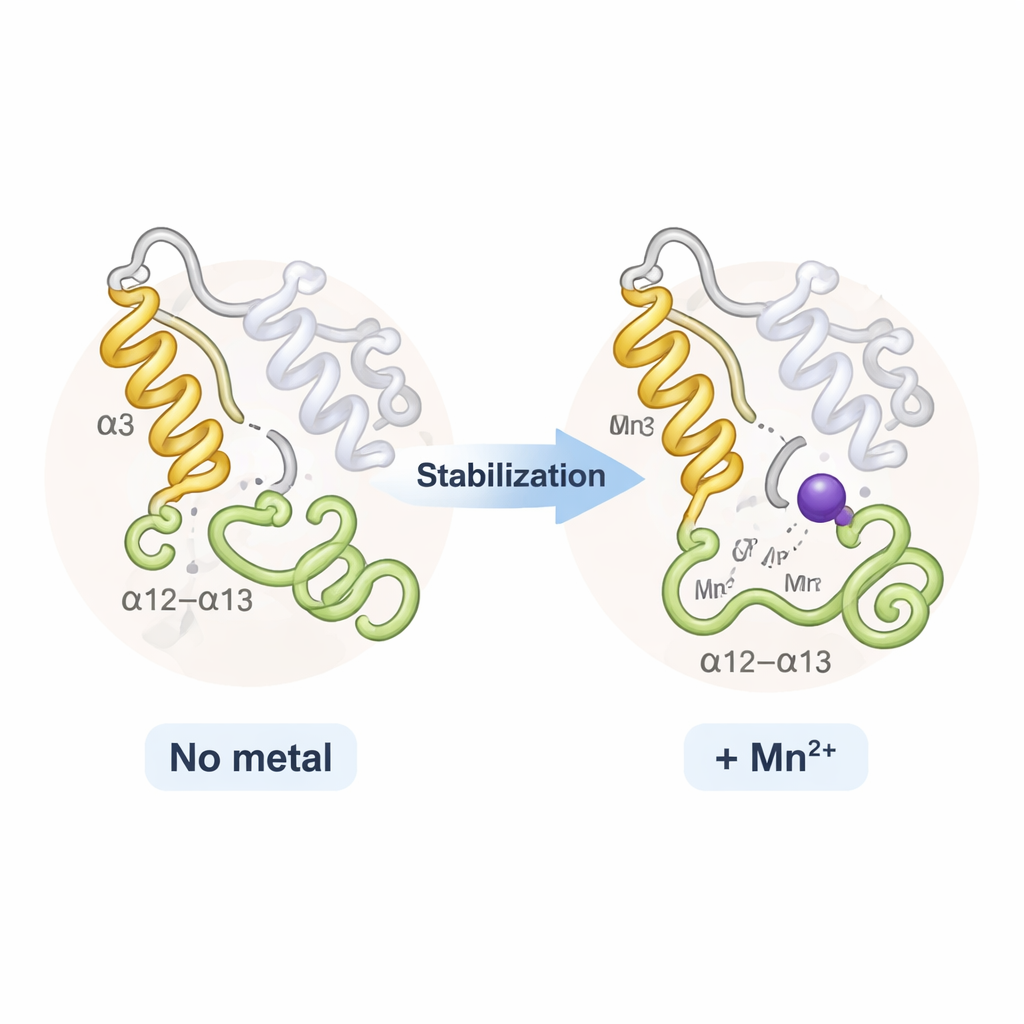
من معادن الخلية إلى ضبط الإشارات
يقترح المؤلفون نموذج «التنشيط عبر الترتيب». في غياب معدن مرتبط، يكون TPST2 مترهلاً حول مدخل الموقع النشط ويعمل بكفاءة منخفضة. يمكن للصوديوم، الشائع داخل الخلايا، أن يرتبط بنفس المواقع ويخلق حالة شبه منظمة ونشطة بشكل معتدل. أما المنجنيز، الموجود بكميات ميكرومولية مضبوطة بعناية داخل جهاز جولجي، فيرتبط بقوة أكبر ويقفل المناطق الأساسية في حالة منظمة على النحو الأمثل، مما يعظم الكفاءة التحفيزية. يشير هذا إلى أن تغييرات طفيفة في مستويات المنجنيز بالجولجي قد تضبط مدى تعديل TPST2 لأهدافه. وبما أن TPST2 يؤثر على إنتاج الهرمونات وإشارات السرطان، تبرز هذه الدراسة رابطاً محتملاً بين توازن أيونات المعادن، و"زخارف" البروتينات، والمرض — كما توفر إطاراً بنيوياً لتصميم أدوية تعدل نشاط TPST2 بمحاكاة أو تعطيل ارتباط المعادن.
الاستشهاد: Jin, M., Noh, C., Yang, J. et al. Structural characterization of metal binding in human tyrosylprotein sulfotransferase 2, TPST2. Sci Rep 16, 6066 (2026). https://doi.org/10.1038/s41598-026-37189-4
الكلمات المفتاحية: كبريتنة التيروسين, TPST2, المنجنيز, جهاز جولجي, تعديل البروتينات