Clear Sky Science · ar
شاشات على مستوى الجينوم تحدد المنظمات الأساسية لتعبير بروتين بريون على سطح الخلية
لماذا هذا مهم لصحة الدماغ
أمراض البريونات، مثل مرض كروتزفيلد-ياكوب لدى البشر و«داء جنون البقر» لدى الأبقار، نادرة لكنها دائماً مميتة وتؤثر على الدماغ. المتهم المركزي هو بروتين دماغي طبيعي يُسمى بروتين البريون، والذي يمكنه الطي بشكل خاطئ ونشر التلف من خلية إلى أخرى. كلما زاد مقدار هذا البروتين على سطح الخلايا العصبية، كان سهلاً على المرض أن ينتشر. هدفت هذه الدراسة إلى رسم خريطة، على مستوى الجينوم بأكمله، لأي الجينات تتحكم في كمية بروتين البريون التي تظهر على خارج الخلايا الشبيهة بالعصبونات. قد تساعد هذه الخريطة العلماء على تصميم طرق جديدة لخفض هذا البروتين وربما إبطاء مجموعة من الأمراض التنكسية العصبية.
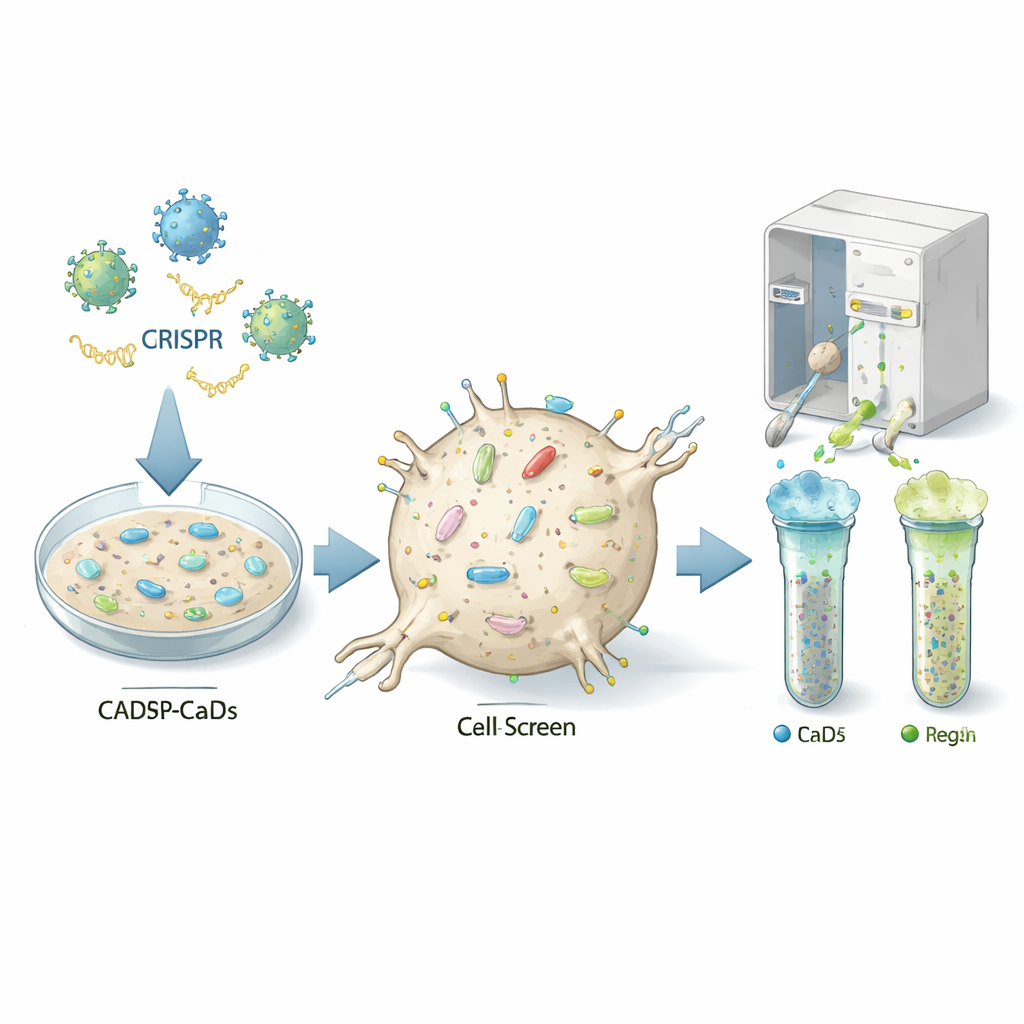
إيجاد مقابض التحكم في الخلية
استخدم المؤلفون طريقة قوية لتحرير الجينات تُسمى CRISPR لإيقاف عمل كل جين تقريباً، واحداً تلو الآخر، في سلالة خلوية فأرية شبيهة بالعصبونات يمكن أن تُصاب بالبريونات (تُدعى خلايا CAD5). تلقت كل خلية «ضربة» جينية مختلفة، فاحتوت المجموعة الناتجة على ملايين المتغيرات، كل منها يفتقد جيناً محدداً. بعدها صبغ الفريق الخلايا بأجسام مضادة متوهجة تتعرف على بروتين البريون الطبيعي على سطح الخلية، واستخدموا جهاز فرز خلوي لفصل الخلايا ذات المستويات غير العادية المنخفضة أو المرتفعة من هذا البروتين. من خلال تسلسل أدلة RNA الدليلية التي تراكمت في المجموعات المنخفضة أو المرتفعة، استطاعوا استنتاج أي الجينات المعطلة كانت تعمل عادة كمفاتيح تشغيل أو إيقاف لبروتين البريون على سطح الخلية.
حالتان خلويتان، نتائج متداخلة
الخلايا العصبية لا تبدو أو تتصرف جميعها بنفس الشكل عبر فترة حياتها، لذا تساءل الباحثون عما إذا كانت نفس الجينات تتحكم في بروتين البريون في حالات خلوية مختلفة. يمكن الحفاظ على خلايا CAD5 في حالة سريعة النمو وأقل تخصصاً، أو دفعها، عبر إزالة المصل من وسط الزرع، لتأخذ شكلاً أكثر نضجاً وشبهاً بالعصبونات. نفذ الفريق نفس فحص CRISPR على مستوى الجينوم في كلتا الحالتين. في الخلايا غير المتمايزة (الأقل نضجاً) تحققوا من صحة 46 جيناً تزيد، و21 جيناً تقلل، من بروتين البريون على السطح عند وجودها. في الخلايا المتمايزة (الأكثر شبهاً بالعصبونات) أكدوا وجود 41 منظمات إيجابية و13 منظمات سلبية. كانت 23 جينة — معظمها تلك التي تساعد على إلحاق «مرساة» دهنية بالبروتين — مشتركة بين الحالتين، مما يبرز آلية تنظيمية أساسية تعمل بغض النظر عن مستوى النضج.
خطوط التجميع الرئيسية الأكثر أهمية
كشفت مزيد من التحليلات أن العديد من الجينات المكتشفة حديثاً تنتمي إلى «خطوط تجميع» خلوية معروفة تعدل البروتينات أثناء انتقالها إلى سطح الخلية. أحد المسارات الرئيسية يبني مرساة GPI، وهي بنية صغيرة غنية بالدهون تربط بروتين البريون بالوجه الخارجي لغشاء الخلية. تعطيل أي خطوة تقريباً في هذا المسار قلل من كمية بروتين البريون التي تصل إلى السطح، في كل من الخلايا غير الناضجة والناضجة. المسار الثاني يتعلق بالجليكوزلة المرتبطة بـ N، حيث تُضاف سلاسل سكرية معقدة إلى البروتينات أثناء مرورها عبر الأغشية الداخلية للخلية. برزت جينات هذا المسار المضاف للسكر بشكل رئيسي كمهمة في الخلايا الأقل نضجاً. عندما عالج الباحثون الخلايا بجزيئات صغيرة تحجب خطوات محددة في الجليكوزلة، انخفضت مستويات بروتين البريون السطحي بنحو ثلث دون قتل الخلايا، مؤكدة النتائج الجينية.
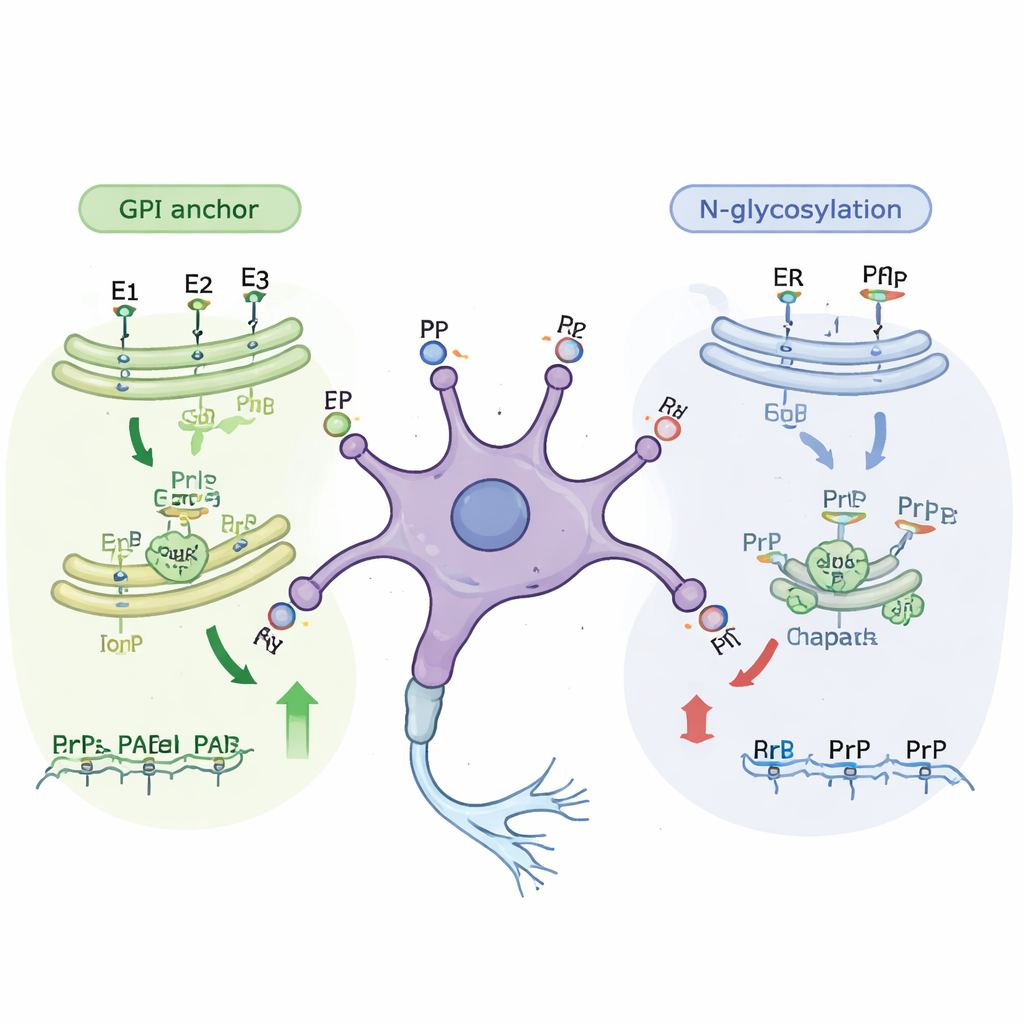
بروتينات المساعدة واستجابات الإجهاد
أبرزت الشاشات أيضاً الشيبيرونات الجزيئية — بروتينات تساعد البروتينات الأخرى على الطي بشكل صحيح — كمنظمات مهمة للبريون. على نحو خاص، برز Hspa5 (المعروف أيضاً باسم BiP)، وهو شيبيرون مركزي في حجرة طي البروتينات داخل الخلية، كمنظم إيجابي في الخلايا الأكثر شبهاً بالعصبونات. عندما استخدم الباحثون دواءً لكبح Hspa5، انخفضت مستويات بروتين البريون السطحي في كلتا الحالتين الخلوية، مرة أخرى دون أذى واضح للخلايا. شملت النتائج الأخرى جينات متعلقة بنقل البروتينات عبر الخلية، والتحكم في تشغيل الجينات أو إيقافها، وعدة بروتينات مرتبطة بوظيفة المشابك وأمراض دماغية أخرى مثل مرض ألزهايمر وALS. معاً، تُظهر هذه النتائج أن مستويات بروتين البريون على سطح الخلية تتشكل عبر شبكة من المسارات تمتد من إنتاج البروتين وتعديله إلى نقله وضبط جودته.
ما يعنيه هذا للعلاجات المستقبلية
يوفر هذا العمل أول فهرس شامل للجينات التي تتحكم في كمية بروتين البريون التي تظهر على سطح الخلايا الشبيهة بالعصبونات المعرضة للإصابة بالبريونات. بعض هذه الجينات، وخصوصاً تلك المنتمية إلى مسارات مرساة GPI وN-جليكوزلة ونظام الشيبيرون Hspa5، تبرز كنقاط انطلاق واعدة لاكتشاف الأدوية: خفض نشاطها ينبغي أن يقلل من مقدار بروتين البريون المتاح للطي الخاطئ، والدراسات السابقة تُظهر أن حتى التخفيض الجزئي يمكن أن يؤخر المرض بشكل ملحوظ في الحيوانات. في الوقت نفسه، تؤكد الاختلافات الواضحة بين الخلايا غير الناضجة والناضجة أن حالة خلية الدماغ مهمة عند اختيار الأهداف. وبينما لا يزال هناك حاجة لمزيد من العمل لاختبار كيف يؤثر التلاعب بهذه الجينات على العدوى البريونية الفعلية وحالات التنكس العصبي الأخرى في الأدمغة الحية، تقدم هذه الدراسة خريطة لمقابض خلوية يمكن للباحثين استكشافها لإبطاء أو منع هذه الأمراض المدمرة.
الاستشهاد: Beauchemin, K.S., Supattapone, S. Genome-wide screens identify core regulators of cell surface prion protein expression. Sci Rep 16, 5895 (2026). https://doi.org/10.1038/s41598-026-37137-2
الكلمات المفتاحية: بروتين بريون, فحص CRISPR, الضمور العصبي, جليكوزلة البروتين, مَرْساة GPI