Clear Sky Science · ar
دراسة مقارنة حول التنبؤ بالانبثاث البعيد بعد جراحة سرطان الرئة استنادًا إلى نماذج تعلم الآلة
لماذا يهم التنبؤ بانتشار السرطان
لا يزال سرطان الرئة واحدًا من أكثر السرطانات فتكًا، حتى عندما يزيل الجراحون كل الأورام المرئية. يصاب كثير من المرضى لاحقًا بترسبات سرطانية خفية تظهر في الدماغ أو العظام أو الكبد أو أعضاء أخرى. يرغب الأطباء في معرفة، بعد الجراحة بوقت قصير، أي المرضى أكثر عرضة لهذا النوع من الانتشار البعيد حتى يتمكنوا من تكييف زيارات المتابعة والعلاجات. تستكشف هذه الدراسة ما إذا كانت برامج الحاسوب الحديثة، المعروفة بنماذج تعلم الآلة، قادرة على التنبؤ بمن هم في خطر أعلى، باستخدام معلومات تجمعها المستشفيات بالفعل في الرعاية الروتينية.
فحص دقيق لعدد كبير من المرضى
راجع الباحثون سجلات 3,120 شخصًا مصابًا بسرطان الرئة في المراحل I إلى III والذين أُزيلت أورامهم في مركز سرطاني واحد في الصين. خضع جميعهم لمتابعة لا تقل عن عامين. جمع الفريق لكل مريض 52 نوعًا من المعلومات، بما في ذلك العمر والجنس والوزن وتاريخ التدخين ونتائج الفحوصات والتفاصيل الجراحية والاختبارات المختبرية، وما إذا تلقوا علاجات إضافية مثل الكيمياء أو الإشعاع بعد الجراحة. مع مرور الوقت، طور 596 من هؤلاء المرضى انبثاثًا بعيدًا، بينما لم يتطور الانبثاث لدى 2,524 منهم. سمح هذا الخليط الواقعي للفريق برؤية الميزات المرتبطة بالانتشار المستقبلي.
تعليم الحواسيب على التعرف على أنماط الخطر
بدلًا من الاعتماد على صيغة واحدة، قارن العلماء تسع طرق مختلفة لتعلم الآلة، بدءًا من أشجار القرار البسيطة وصولًا إلى تقنيات متقدمة تجمع بين نماذج صغيرة متعددة. استخدموا أولًا مرشحًا رياضيًا لتقليص العوامل الأصلية الـ52 إلى مجموعة أصغر وأكثر معلوماتية. ثم، في جولات متكررة، دربوا كل نموذج على جزء من البيانات واختبروه على مرضى لم «يرهم» من قبل. وبما أن حوالي واحدًا من كل خمسة مرضى فقط طور انبثاثًا، قاموا بتعديل التدريب حتى لا يتنبأ الحاسوب ببساطة بـ"خطر منخفض" للجميع. قيموا الأداء باستخدام مقاييس متعددة، بما في ذلك مدى قدرة النماذج على تمييز المرضى ذوي المخاطر العالية عن ذوي المخاطر المنخفضة ومدى تطابق المخاطر المتوقعة مع ما حدث فعليًا.
إيجاد النموذج الأكثر موثوقية
من بين الطرق التسع، برز نموذج يسمى شجرة تعزيز التدرج (Gradient Boosting Decision Tree - GBDT). على بيانات الاختبار، صنف المرضى بدقة إجمالية تقارب 77%، وكانت قيمة قياس التمييز المُلخصة (المساحة تحت منحنى ROC) 0.81، وهي قيمة تُعتبر قوية لأدوات التنبؤ الطبية. كان النموذج جيدًا بشكل خاص في تحديد المرضى الذين سيبقون بلا انبثاث (قيمة تنبؤية سلبية عالية)، مما يعني أن نتيجة منخفضة المخاطر كانت مطمئنة في الغالب. عندما فحص الفريق سلوك النموذج عبر تقسيمات عشوائية متعددة للبيانات، ظل أداؤه ثابتًا، مما يوحي بأنه لم يكتف بتذكر خصائص مجموعة فرعية واحدة فقط.
ما الذي يوجه قرارات النموذج
أحد الانتقادات الشائعة لتعلم الآلة أنه قد يكون "صندوقًا أسود". للتعامل مع هذا، استخدم المؤلفون طريقة تفسير تسمى SHAP، التي تُنسب لكل عامل مساهمة في تقدير الخطر النهائي لكل مريض. أظهر هذا التحليل أن أقوى الإشارات كانت ما إذا كان المريض قد تلقى العلاج الكيميائي أو الإشعاعي بعد الجراحة، وعدد العقد الليمفاوية التي احتوت على سرطان، والعمر، ومؤشر كتلة الجسم (BMI)، وعدد العدلات قبل العملية، وهو نوع من خلايا الدم البيضاء. كان المرضى الذين لديهم تداخل أكبر في العقد الليمفاوية وعلامات التهاب جهازي يميلون إلى الحصول على خطر متوقع أعلى. ويشدّد المؤلفون على أن المساهمات العالية للعلاج الكيميائي والإشعاعي لا تعني أن هذه العلاجات تسبب الانبثاث؛ بل هي علامات على أن الأطباء قد حكموا بالفعل بأن المرض أكثر عدائية، لذا كان هؤلاء المرضى يبدأون بخطر أعلى.
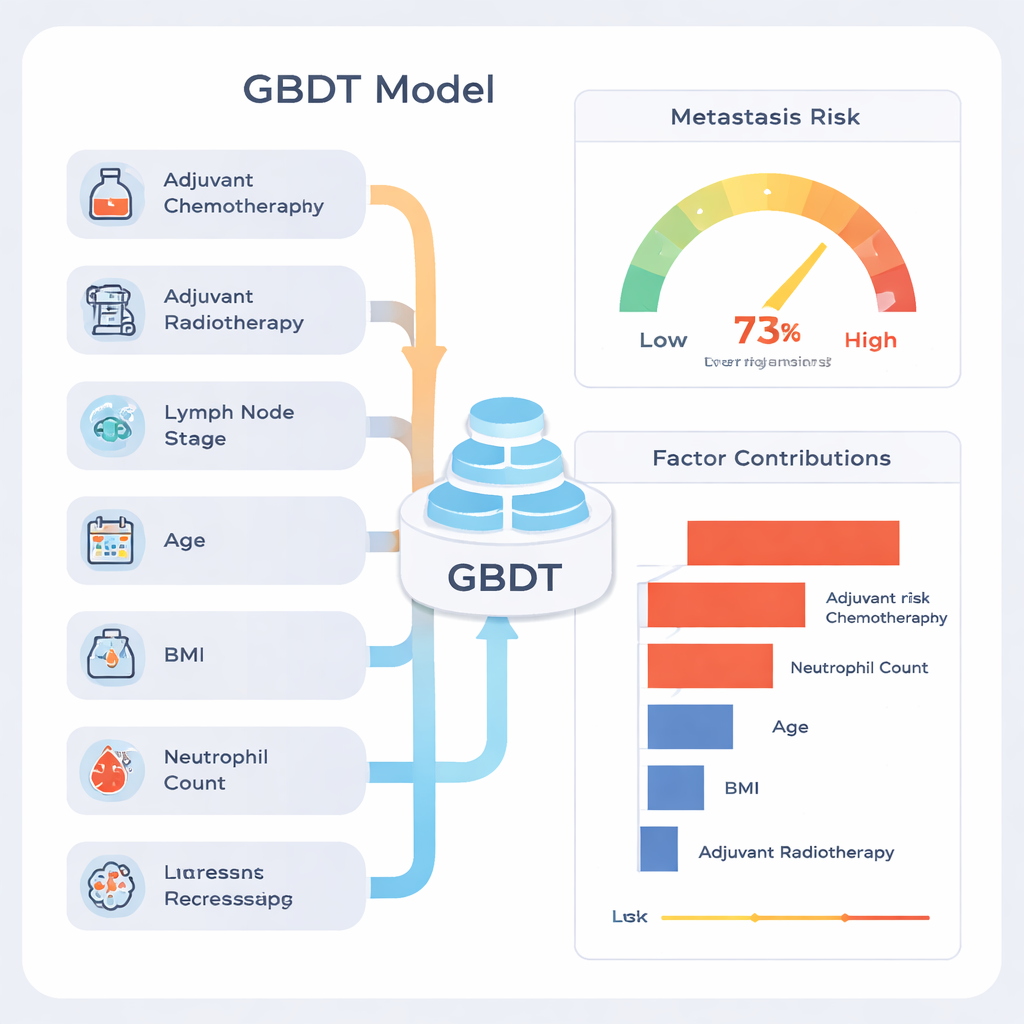
كيف يمكن أن يساعد ذلك المرضى عمليًا
نظرًا لأن النموذج يستخدم معلومات يسجلها معظم مراكز السرطان بالفعل، فقد يمكن، بعد مزيد من الاختبارات، دمجه في برمجيات المستشفيات. بالنسبة لمريض جديد أجرى للتو عملية جراحية للرئة، يمكن للنظام سحب بياناته وإخراج احتمال مخصص للانبثاث البعيد، مع شرح بسيط للعوامل التي ترفع الخطر أو تخفضه. يمكن للأطباء بعد ذلك استخدام هذا لتقرير من يحتاج لمتابعة تصويرية أقرب، أو لمزيد من الإرشاد، أو للتسجيل في تجارب سريرية، ومن يمكنه تجنب المراقبة المكثفة بأمان. أُجريت الدراسة في مستشفى واحد، لذا لا يزال من الضروري التحقق من الأداة وتعديلها في مناطق ونظم رعاية صحية أخرى. لكنها تقدم مخططًا واعدًا لدمج البيانات السريرية الروتينية مع تعلم آلة شفاف لتحسين الرعاية الطويلة الأمد لمرضى سرطان الرئة.
الاستشهاد: Guo, X., Xu, T., Luo, Y. et al. Comparative study on predicting postoperative distant metastasis of lung cancer based on machine learning models. Sci Rep 16, 6468 (2026). https://doi.org/10.1038/s41598-026-37113-w
الكلمات المفتاحية: سرطان الرئة, الانبثاث البعيد, تعلم الآلة, تنبؤ المخاطر, المتابعة بعد الجراحة